Clear Sky Science · it
RBP4 interferisce con la progressione del carcinoma squamoso della lingua inibendo la via di segnalazione PI3K/AKT e promuovendo la polarizzazione dei macrofagi in tipo M1
Perché il cancro della lingua ha bisogno di nuove idee
Il cancro della lingua può privare le persone della capacità di parlare, mangiare e percepire i sapori e, nonostante chirurgia, chemioterapia e radioterapia, la sopravvivenza a lungo termine spesso resta deludente. Questo studio esplora un alleato inatteso nel sangue, una proteina che trasporta la vitamina A chiamata RBP4, e mostra come essa possa sia rallentare la crescita dei tumori della lingua sia mobilitare i difensori immunitari dell’organismo. Svelando come questa molecola agisca all’interno delle cellule tumorali e nelle cellule immunitarie circostanti, la ricerca indica strategie nuove che potrebbero un giorno rendere i trattamenti più efficaci e meno dannosi.
Una proteina nascosta nei tumori della lingua
I ricercatori hanno iniziato setacciando grandi banche dati genomiche sul cancro per individuare quali geni legati all’immunità potessero prevedere l’andamento dei pazienti con carcinoma squamoso della lingua. Tra centinaia di candidati, RBP4, una proteina nota soprattutto per il trasporto della vitamina A nel flusso sanguigno, è emersa come particolarmente interessante. Confrontando campioni tumorali con tessuto sano adiacente alla lingua, hanno riscontrato che i livelli di RBP4 erano costantemente molto più bassi nei tumori. Questo schema è stato confermato in diversi dataset indipendenti e in campioni tissutali di 20 pazienti, suggerendo che la perdita di RBP4 sia una caratteristica comune di questa malattia.
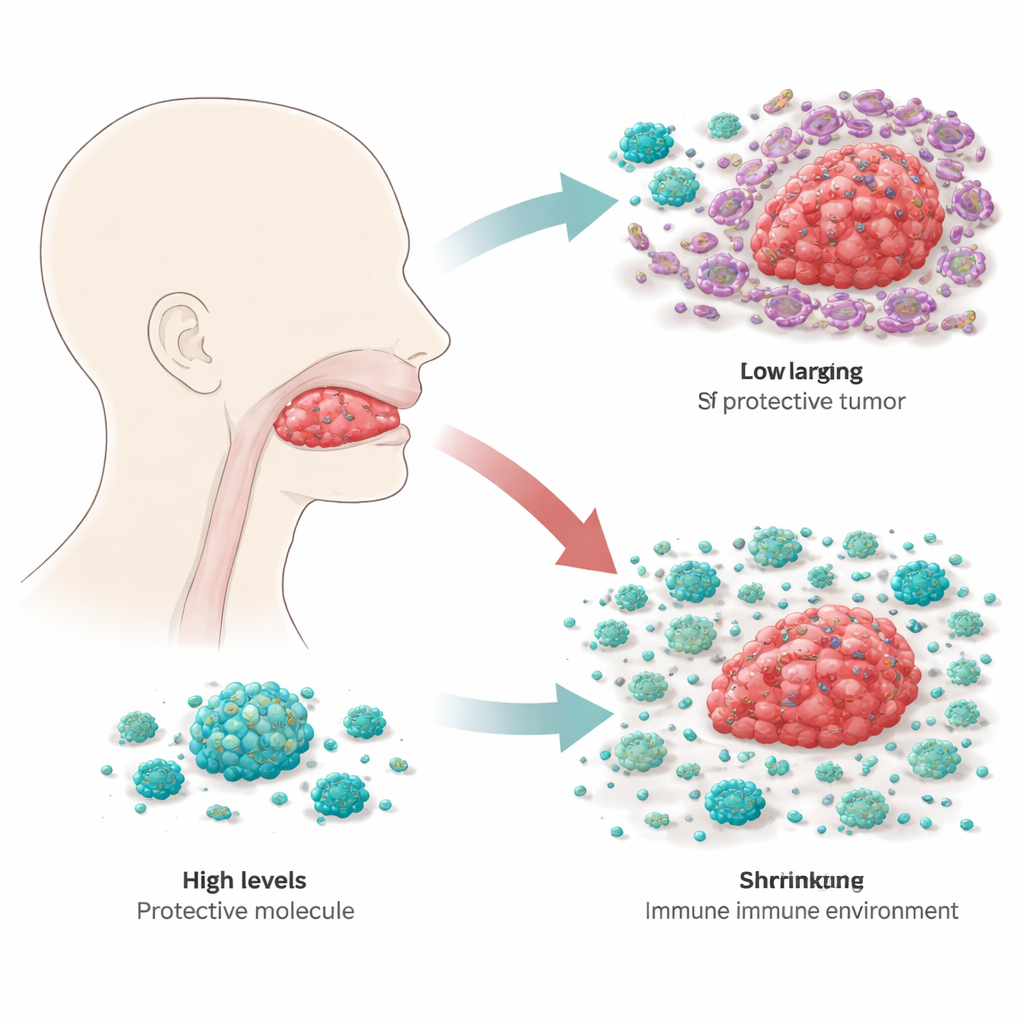
Rallentare la crescita tumorale dall’interno
Per capire cosa faccia effettivamente RBP4 nelle cellule del cancro della lingua, gli scienziati hanno modificato linee cellulari tumorali in modo che producessero RBP4 in eccesso oppure ne esprimessero molto meno. In colture cellulari, le cellule con livelli più alti di RBP4 crescevano più lentamente, mentre quelle con RBP4 ridotto si moltiplicavano più rapidamente ed erano più abili a muoversi e invadere membrane artificiali, comportamenti associati alla diffusione e alla recidiva. Quando queste cellule modificate sono state impiantate in topi, i tumori con RBP4 aggiuntivo restavano più piccoli, mentre quelli con RBP4 ridotto crescevano più aggressivi. Monitorando gli interruttori chiave del controllo della crescita all’interno delle cellule, il team ha mostrato che RBP4 attenua una via di crescita importante nota come PI3K–AKT–mTOR, che molti tumori usano come acceleratore interno. Con RBP4 elevato, questa via è meno attiva e le cellule tumorali hanno minore capacità di assumere lo stato mobile e flessibile che facilita la migrazione.
Trasformare le cellule immunitarie in combattenti del tumore
Il cancro non cresce in isolamento; vive all’interno di un vicinato di cellule immunitarie, vasi sanguigni e cellule di supporto chiamato microambiente tumorale. Qui i macrofagi—grandi cellule immunitarie che possono sia attaccare sia assistere i tumori—ricoprono un ruolo centrale. Gli investigatori hanno notato che i tumori con più RBP4 tendevano anche a contenere una maggiore quota di macrofagi di tipo “M1”, associati a infiammazione e uccisione tumorale, piuttosto che del tipo “M2”, che spesso sostiene la crescita tumorale. In coltura, quando i macrofagi venivano esposti a RBP4 purificato o a cellule del cancro della lingua ingegnerizzate per secernere più RBP4, si spostavano verso questo stato M1, combattente del tumore. Quando RBP4 veniva ridotto nelle cellule tumorali, i macrofagi tendevano invece a polarizzarsi verso il profilo più favorevole al tumore.
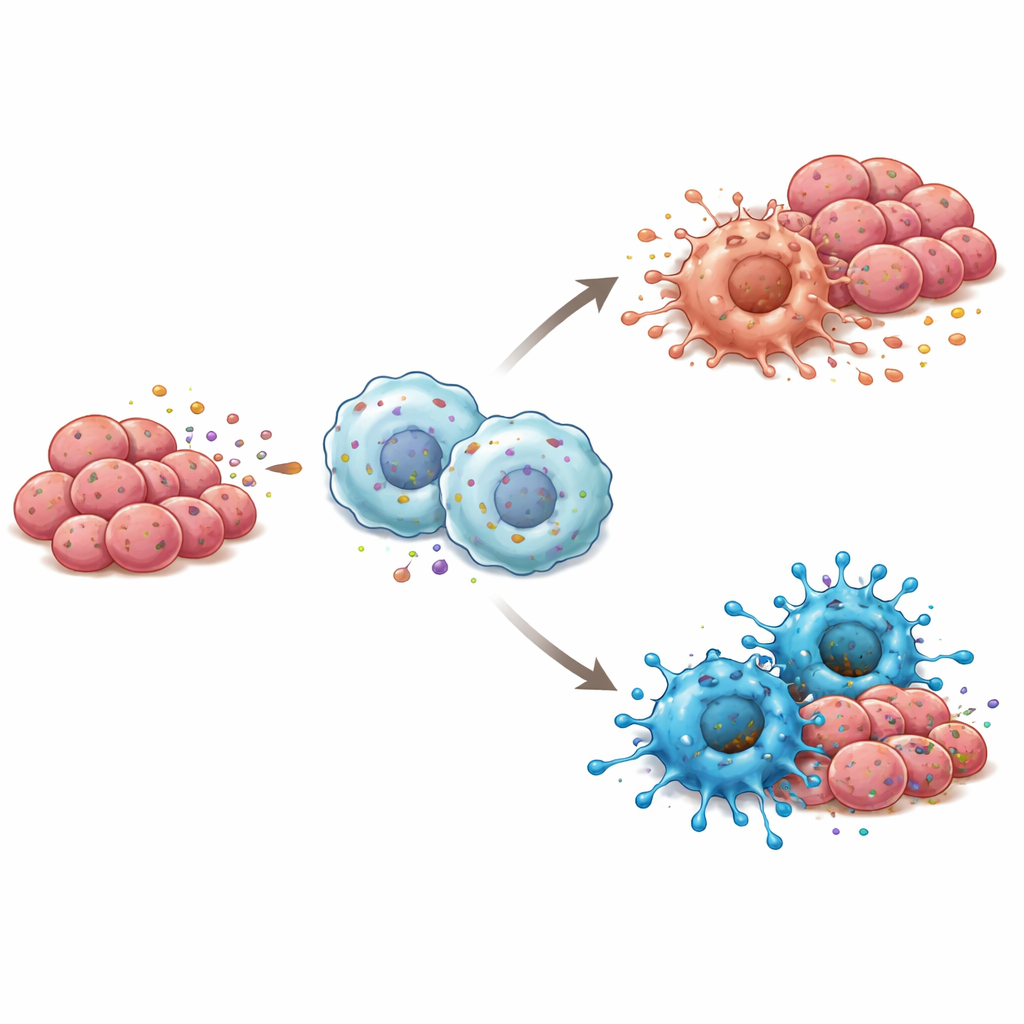
Vie di segnalazione alla base dello spostamento immunitario
Per capire come RBP4 spinga i macrofagi a diventare più ostili verso i tumori, i ricercatori hanno esaminato quali sistemi di allarme interni fossero attivati in queste cellule immunitarie. Hanno scoperto che RBP4 stimolava un sensore chiamato TLR4 sulla superficie dei macrofagi e, a sua volta, attivava NF-κB, un interruttore maestro che guida le risposte infiammatorie. Bloccare TLR4 con un inibitore chimico interrompeva questa reazione a catena e impediva ai macrofagi di assumere lo stato M1, anche in presenza di RBP4. Nei topi, i tumori formati da cellule del cancro della lingua ricche di RBP4 e miscelate con macrofagi crescevano più lentamente e contenevano più cellule di tipo M1, insieme a una maggiore attività di TLR4 e NF-κB, rafforzando l’idea che questa via sia cruciale per gli effetti immunitari di RBP4.
Cosa potrebbe significare per le cure future
Nel complesso, il lavoro dipinge RBP4 come un freno a doppia azione sul cancro della lingua: nelle cellule tumorali interne attenua un circuito di crescita iperattivo e nel quartiere del tumore aiuta a convertire i macrofagi in difensori più vigili. Sebbene permangano molte questioni—come esattamente RBP4 interagisca con i suoi bersagli e come aumentarlo in modo sicuro—lo studio suggerisce che ripristinare o mimare l’azione di RBP4 potrebbe sia rallentare l’espansione tumorale sia rafforzare la pressione immunitaria dell’organismo sul cancro. Per i pazienti, questo apre la prospettiva di terapie future che non si limitino a rimuovere i tumori, ma che rimodellino anche la loro circuiteria interna e l’“ecosistema” locale per impedirne la ricomparsa.
Citazione: Yan, Y., Miao, N. & Wang, X. RBP4 interferes with tongue squamous cell carcinoma progression by inhibiting the PI3K/AKT signaling pathway and promoting macrophage M1-type polarization. Sci Rep 16, 9375 (2026). https://doi.org/10.1038/s41598-026-39915-4
Parole chiave: cancro della lingua, RBP4, microambiente tumorale, macrofagi