Clear Sky Science · it
Un quadro sanitario intelligente per la diagnosi del carcinoma epatocellulare basato su apprenditori aggregati da dati biomedici utilizzando intelligenza artificiale spiegabile
Perché sono importanti controlli del fegato più intelligenti
Il cancro al fegato, in particolare una forma comune chiamata carcinoma epatocellulare, spesso cresce silenziosamente fino a diventare difficile da trattare. I medici raccolgono già una grande quantità di risultati di esami routinari dai pazienti, ma trasformare tutti quei numeri in un avvertimento precoce è complicato. Questo studio esplora come programmi informatici avanzati possano setacciare i dati medici di uso quotidiano per individuare i pazienti ad alto rischio, spiegando al contempo le loro ragioni in modi che i clinici possano comprendere e fidarsi.
Trasformare gli esami di routine in segnali precoci
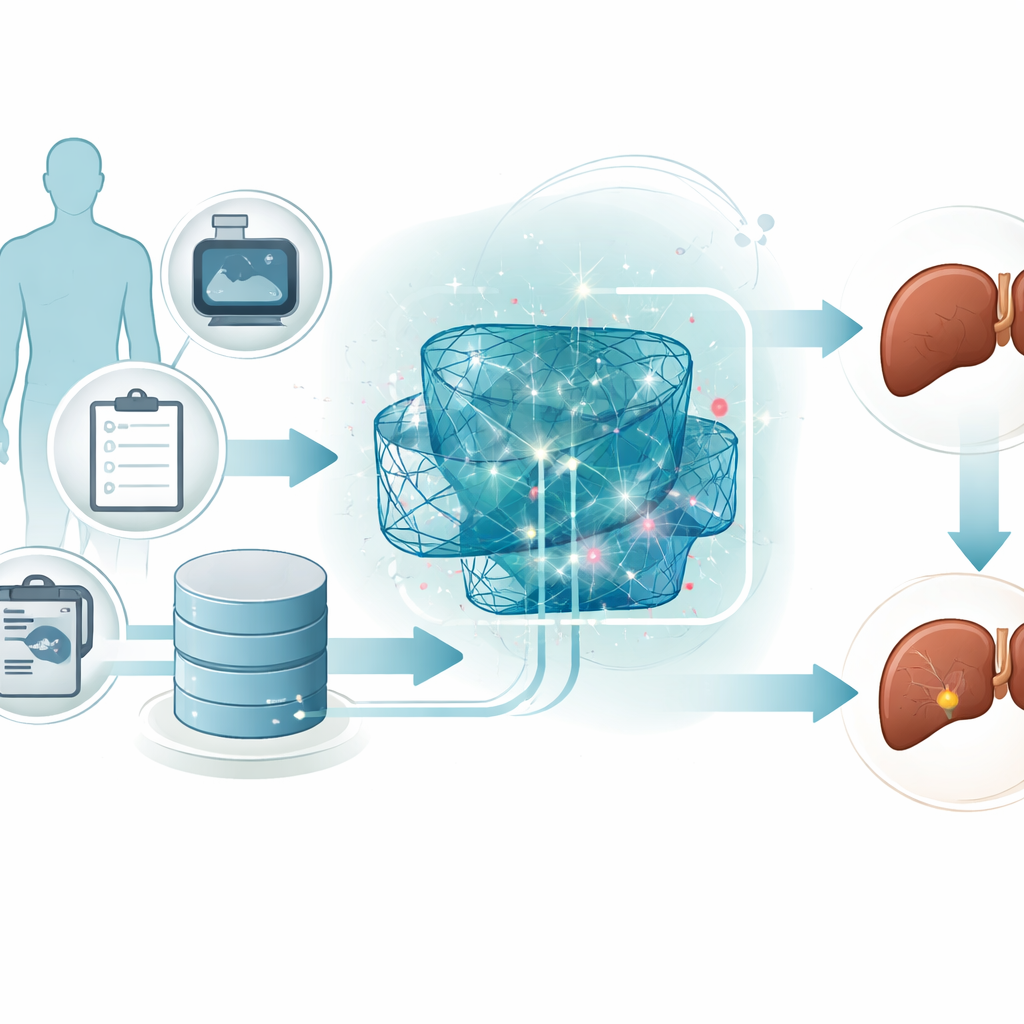
I ricercatori si concentrano su pazienti con problemi epatici cronici, che presentano una probabilità più alta di sviluppare un grave cancro al fegato. Invece di affidarsi a costose scansioni o test genetici complessi, utilizzano misurazioni cliniche di routine—come chimica del sangue, enzimi epatici e informazioni di base sullo stato di salute. Queste misurazioni vengono prima accuratamente rimappate in modo che tutte le caratteristiche rientrino nello stesso intervallo numerico. Questo semplice ma importante passaggio di pulizia aiuta i modelli informatici a imparare i pattern in modo più affidabile ed evita che un singolo valore insolitamente grande domini le previsioni.
Molti “secondi pareri” digitali che lavorano insieme
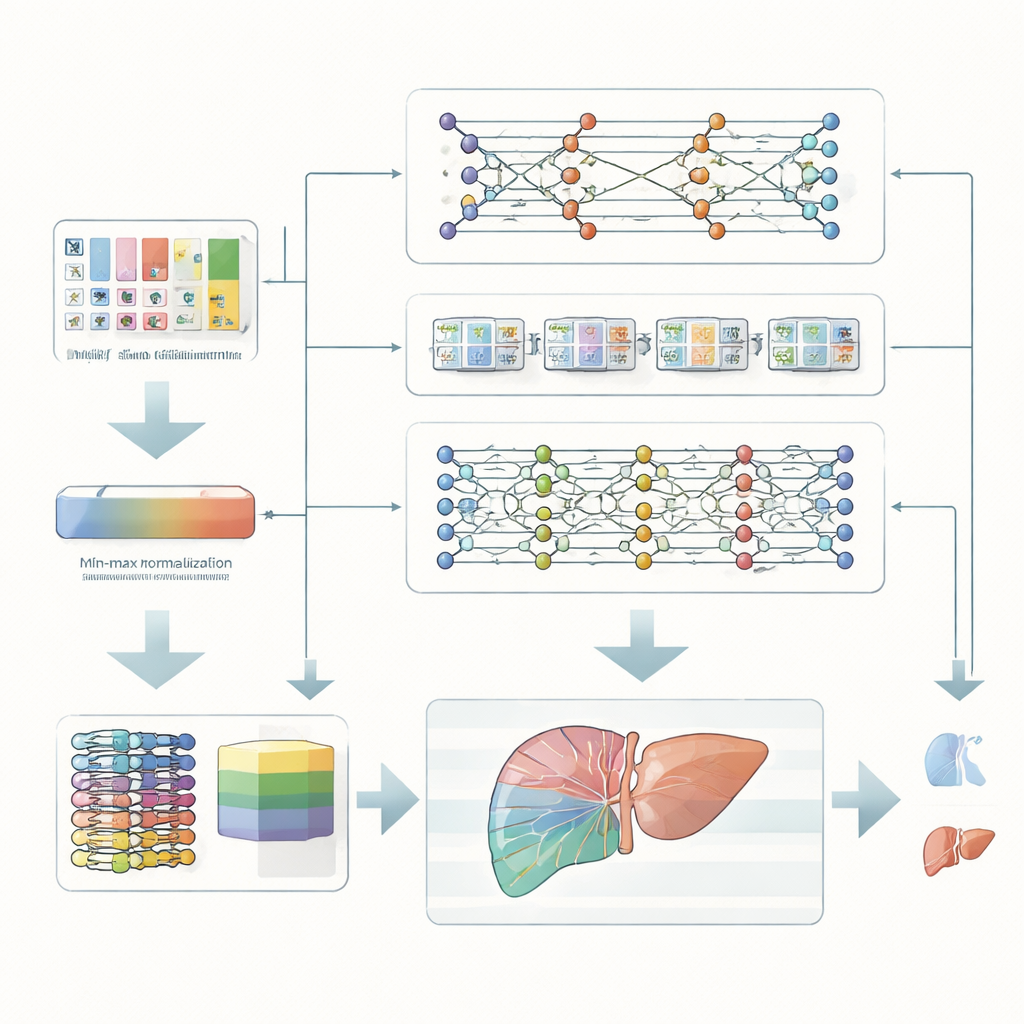
Anziché dipendere da un unico algoritmo, il team costruisce un ensemble, o squadra, di tre diversi modelli di deep learning. Un modello comprime i dati per scoprire le combinazioni di caratteristiche più informative. Un secondo modello è progettato per riconoscere pattern che si sviluppano come sequenze, catturando come più misurazioni insieme possano suggerire rischio. Un terzo modello impila diversi strati semplici per cogliere relazioni complesse e non lineari nascoste nei dati. Ogni modello esprime un proprio giudizio sull'appartenenza del paziente al gruppo ad alto o basso rischio, e un livello superiore combina e pondera queste opinioni in una decisione finale.
Aprire la scatola nera per i medici
Per quanto potenti, i sistemi di deep learning sono spesso criticati per comportarsi come misteriose “scatole nere”. Per affrontare questo problema, gli autori aggiungono uno strato di intelligenza artificiale spiegabile basato su un metodo noto come SHAP. Questa tecnica stima quanto ogni caratteristica di input spinga una predizione individuale verso un esito più sicuro o più rischioso. Per esempio, certi livelli di enzimi epatici, marcatori della funzione epatica e segni di diffusione extraepatica emergono come particolarmente influenti. I medici possono vedere non solo che il sistema segnala un paziente come ad alto rischio, ma anche quali misurazioni specifiche hanno guidato quella decisione e in quale direzione, creando una collaborazione più trasparente tra clinico e macchina.
Quanto funziona l’approccio?
Il team testa il suo quadro su un dataset pubblico di 165 pazienti seguiti per almeno un anno, ciascuno etichettato come sopravvissuto o non sopravvissuto. Nonostante la dimensione modesta del dataset, il modello combinato impara a separare i pazienti ad alto rischio da quelli a basso rischio con un'accuratezza sorprendente: classifica correttamente circa 98 casi su 100 nelle fasi finali di addestramento. Rispetto a una gamma di metodi esistenti—inclusi modelli statistici classici e diverse reti neurali moderne—questo approccio non solo eguaglia o supera la loro accuratezza, precisione e bilanciamento tra falsi negativi e falsi positivi, ma lo fa anche con tempi di calcolo relativamente ridotti. Uno studio di ablazione, in cui i tre modelli componenti sono provati singolarmente, mostra che ciascuno contribuisce valore, pur essendo la loro combinazione la più efficace.
Cosa potrebbe significare per la cura dei pazienti
Per la pratica medica di tutti i giorni, questo lavoro indica strumenti decisionali che siano al contempo efficaci e comprensibili. Un sistema costruito su queste basi potrebbe aiutare a segnalare i pazienti epatici che scivolano silenziosamente in una zona di pericolo molto prima che compaiano i sintomi, utilizzando dati già raccolti in molte cliniche. Allo stesso tempo, le sue spiegazioni—evidenziando quali esami e segni clinici contano di più per una persona—potrebbero supportare i medici nel perfezionare i piani di trattamento e nel discutere i rischi con i pazienti. Pur basandosi ancora su un dataset relativamente piccolo e di fonte unica e omettendo dati di imaging e genetici, offre una roadmap per modelli di rischio oncologico più intelligenti e trasparenti che, con dati più ampi e diversificati, potrebbero un giorno diventare alleati di routine nella lotta contro il cancro al fegato.
Citazione: Alqaralleh, B.A.Y., Alksasbeh, M.Z., Kulakli, A. et al. An intelligent healthcare framework for hepatocellular carcinoma diagnosis based on aggregated learners from biomedical data utilising explainable artificial intelligence. Sci Rep 16, 9357 (2026). https://doi.org/10.1038/s41598-026-39871-z
Parole chiave: cancro al fegato, IA medica, diagnosi precoce, IA spiegabile, supporto alle decisioni cliniche