Clear Sky Science · it
Identificazione multi-omica di bersagli chiave per la differenziazione osteogenica delle cellule stromali mesenchimali del midollo osseo umano sotto stress ossidativo
Perché le ossa stressate sono importanti
Con l’età o in presenza di malattie croniche come il diabete e l’osteoporosi, le nostre ossa perdono la capacità di ripararsi. Un grande colpevole è lo “stress ossidativo” – un accumulo di molecole reattive che danneggiano le cellule. Questo studio pone una domanda pratica dalle grandi implicazioni per fratture e impianti ossei: che cosa va esattamente storto all’interno delle cellule staminali del midollo osseo umano esposte a stress ossidativo, e possiamo trovare un interruttore molecolare che le aiuti a continuare a formare nuovo tessuto osseo?
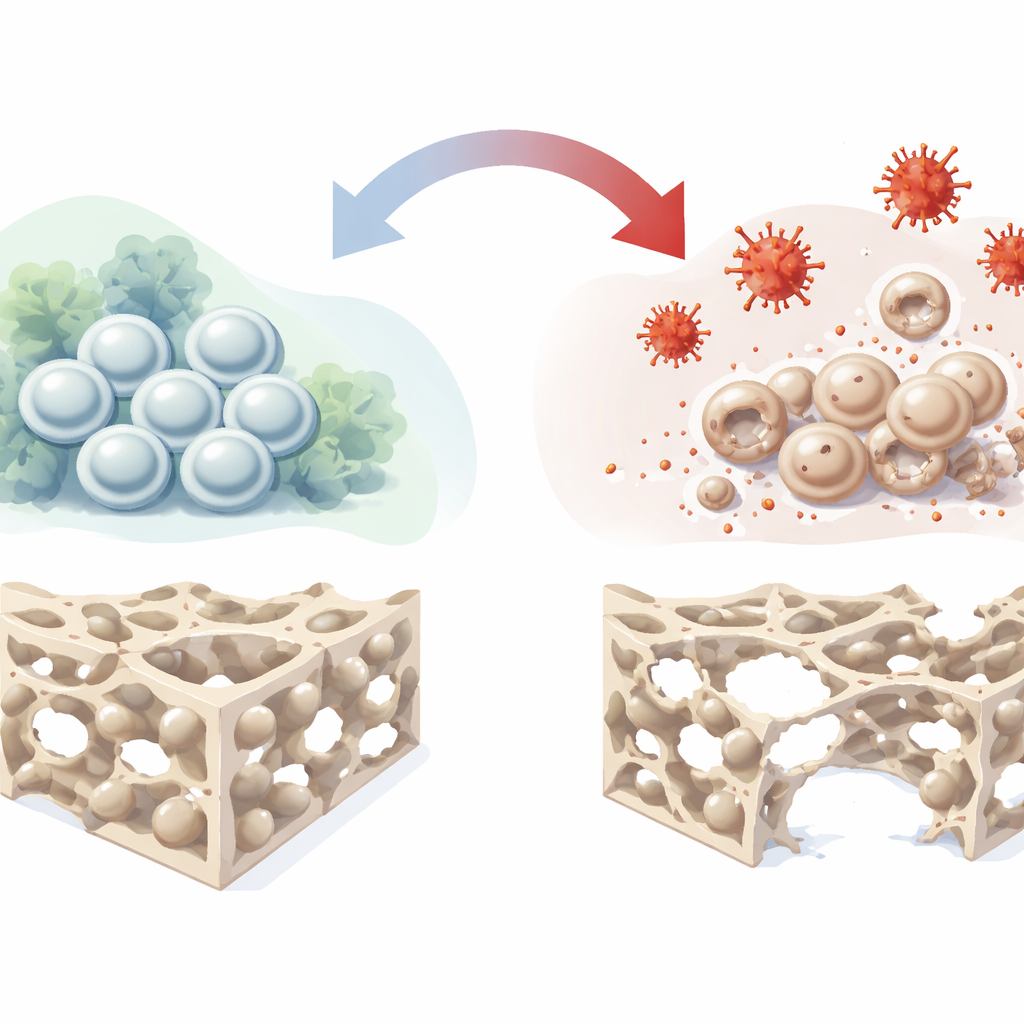
Cellule staminali che costruiscono l’osso
Nelle profondità delle nostre ossa risiedono le cellule stromali mesenchimali del midollo osseo, una popolazione versatile in grado di autorinnovarsi e maturare in osteociti (cellule che formano l’osso), condrociti (cartilagine) e adipociti (grasso). Poiché contribuiscono naturalmente alla riparazione dei tessuti danneggiati, sono un candidato di primo piano per trattamenti di nuova generazione volti a riparare difetti ossei e osteonecrosi. Tuttavia, nei pazienti reali queste cellule spesso si trovano in ambienti ostili caratterizzati da scarsa irrorazione, basso ossigeno, infiammazione e stress ossidativo. In tali condizioni la loro capacità di differenziarsi in cellule ossee viene compromessa, limitando il successo delle terapie a base di cellule staminali. Gli autori hanno quindi ricreato questo ambiente ostile in laboratorio per mappare, in dettaglio, come esso ostacoli la formazione ossea.
Ricreare un ambiente severo in laboratorio
I ricercatori hanno usato il perossido di idrogeno, una fonte comune di specie reattive dell’ossigeno, per indurre stress ossidativo su cellule staminali del midollo osseo umano coltivate in vitro. Hanno titolato con cura la dose per trovare un punto in cui le cellule fossero stressate ma non uccise. A 400 micromolari o meno, le cellule mantenevano la tipica forma allungata a fuso e restavano vitali, sebbene la loro chimica interna mostrasse cambiamenti evidenti: i livelli di specie reattive aumentavano, la funzione mitocondriale cominciava a variare e l’equilibrio tra proteine legate alla sopravvivenza e alla morte si spostava verso l’adattamento allo stress. A dosi più alte le cellule perdevan la forma e morivano in gran numero. Utilizzando la dose ben tollerata di 400 micromolari, il team ha poi indotto le cellule a differenziarsi in senso osteogenico e ha osservato cosa accadeva.
Come lo stress blocca la formazione ossea
Sotto stress ossidativo, la capacità delle cellule staminali di diventare cellule ossee diminuiva in vari test complementari. L’attività osteogenica precoce, monitorata tramite l’enzima fosfatasi alcalina, calava con l’aumentare dello stress. Più avanti, quando le cellule avrebbero dovuto depositare minerali, le piastre di coltura mostravano meno e più deboli noduli di calcio. Anche geni e proteine chiave legati all’osso, come RUNX2 e osteopontina, risultavano regolati al ribasso. Per analizzare più a fondo i meccanismi, gli scienziati hanno combinato due potenti approcci “omici”: il sequenziamento dell’RNA per profilare quali geni erano più o meno attivi e un’analisi proteomica su larga scala per vedere quali proteine cambiavano effettivamente in abbondanza. Insieme, questi dataset hanno rivelato centinaia di alterazioni nel controllo del ciclo cellulare, nel comportamento dei cromosomi, nel metabolismo e nell’organizzazione dell’impalcatura extracellulare, dipingendo il quadro di cellule staminali il cui timing interno e il supporto strutturale vengono sconvolti dallo stress ossidativo.
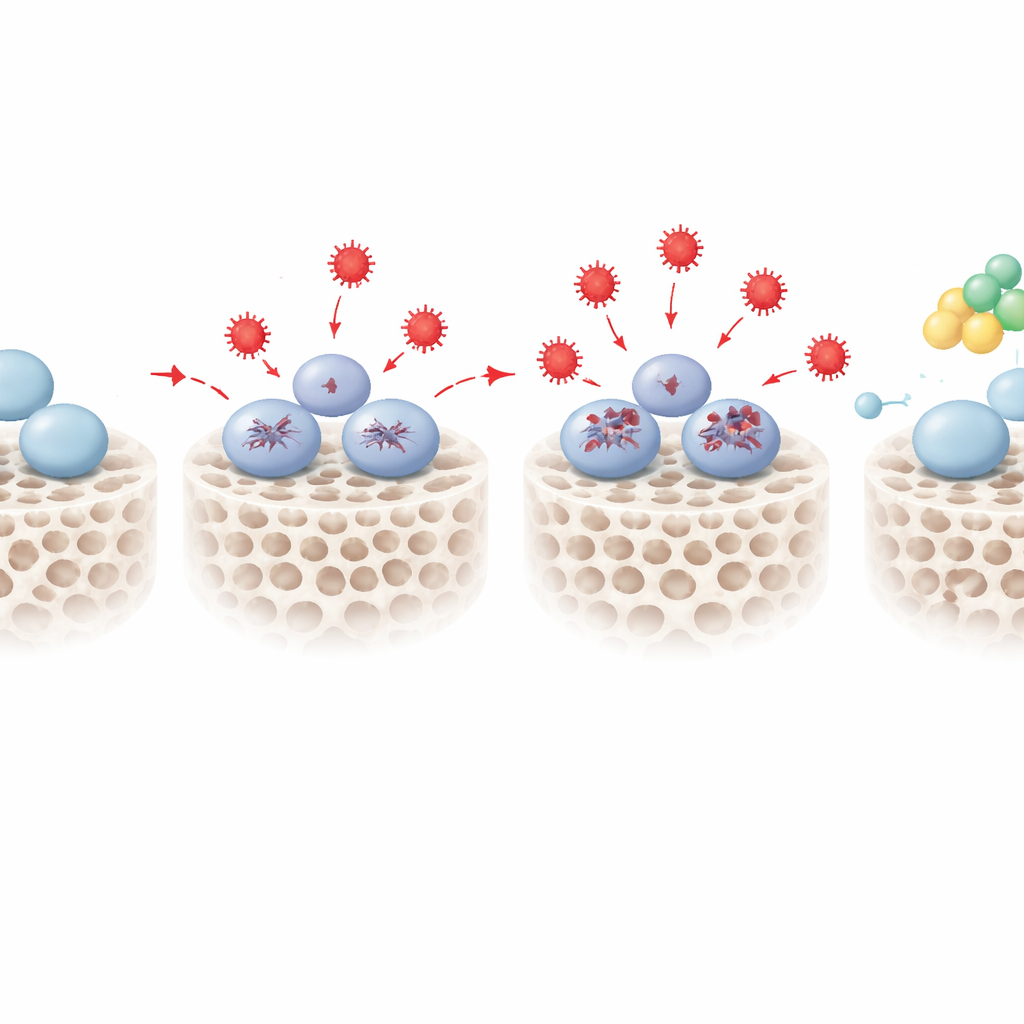
Individuazione di un interruttore protettivo chiamato PENK
Sovrapponendo le mappe di RNA e proteine, il team ha ristretto l’elenco a 18 molecole che cambiavano in modo coerente nelle cellule stressate e che risultavano collegate sia alle risposte allo stress sia alla formazione ossea. Una di queste ha spiccato: la proencefalina, o PENK, nota soprattutto come precursore di peptidi oppioidi naturali. Sotto stress ossidativo, i livelli di PENK aumentavano in modo dipendente dalla dose. Quando gli scienziati riducevano artificialmente l’espressione di PENK con strumenti genetici, le cellule staminali stressate peggioravano ulteriormente nella formazione ossea, mostrando un’attività enzimatica precoce più debole e un deposito di minerali ridotto. Quando potenziavano PENK, accadeva l’opposto: anche nelle stesse condizioni ossidative, le cellule recuperavano gran parte della capacità di costruire matrice ossea mineralizzata. Analisi di pathway aggiuntive suggerivano che PENK potrebbe agire modulando certe rotte metaboliche, incluso il metabolismo degli sfingolipidi, che collegano l’equilibrio redox alle decisioni sulla conservazione del potenziale staminale o la progressione verso il destino osteogenico.
Cosa significa per la riparazione ossea futura
Questo studio dimostra che lo stress ossidativo da solo è sufficiente a compromettere la capacità delle cellule stromali mesenchimali del midollo osseo umano di formare osso, e identifica PENK come un fattore protettivo intrinseco che le aiuta a resistere a questo danno. Per i non specialisti, il messaggio è chiaro: il successo delle terapie ossee basate su cellule staminali dipenderà non solo dalle cellule stesse, ma anche dagli ambienti stressanti in cui vengono inserite e dagli interruttori molecolari che ne facilitano la tolleranza. Evidenziando PENK come un bersaglio promettente, il lavoro indica la strada verso futuri farmaci o approcci basati sul gene che potrebbero rafforzare la riparazione ossea in pazienti i cui tessuti sono immersi in stress ossidativo, dagli anziani a chi convive con malattie metaboliche o infiammatorie croniche.
Citazione: Dong, W., Zheng, Y., Zhou, Y. et al. Multi-omics identification of key targets for the osteogenic differentiation of human bone marrow mesenchymal stromal cells under oxidative stress. Sci Rep 16, 8215 (2026). https://doi.org/10.1038/s41598-026-39818-4
Parole chiave: rigenerazione ossea, stress ossidativo, cellule staminali mesenchimali, differenziazione osteogenica, PENK