Clear Sky Science · it
Impatto dell’ossidazione degli RNA a G-quadruplex sulla dinamica conformazionale e sull’interazione con TDP-43 associato alla SLA
Perché è importante per la salute dei nervi
La sclerosi laterale amiotrofica (SLA) è una malattia fatale in cui le cellule nervose che controllano il movimento muoiono lentamente, ma le cause alla base di questo danno selettivo restano misteriose. Questo studio pone una domanda semplice ma cruciale: con l’invecchiamento e l’aumento del «corrosivo» danno chimico nelle nostre cellule, questo logorio sull’RNA — la copia operativa dei nostri geni — compromette i segnali vitali che mantengono i motoneuroni in vita? Focalizzandosi su una forma ripiegata speciale dell’RNA e su una proteina chiave legata alla SLA chiamata TDP-43, il lavoro mette in luce come piccole cicatrici chimiche possano contribuire a creare le condizioni favorevoli alla malattia. 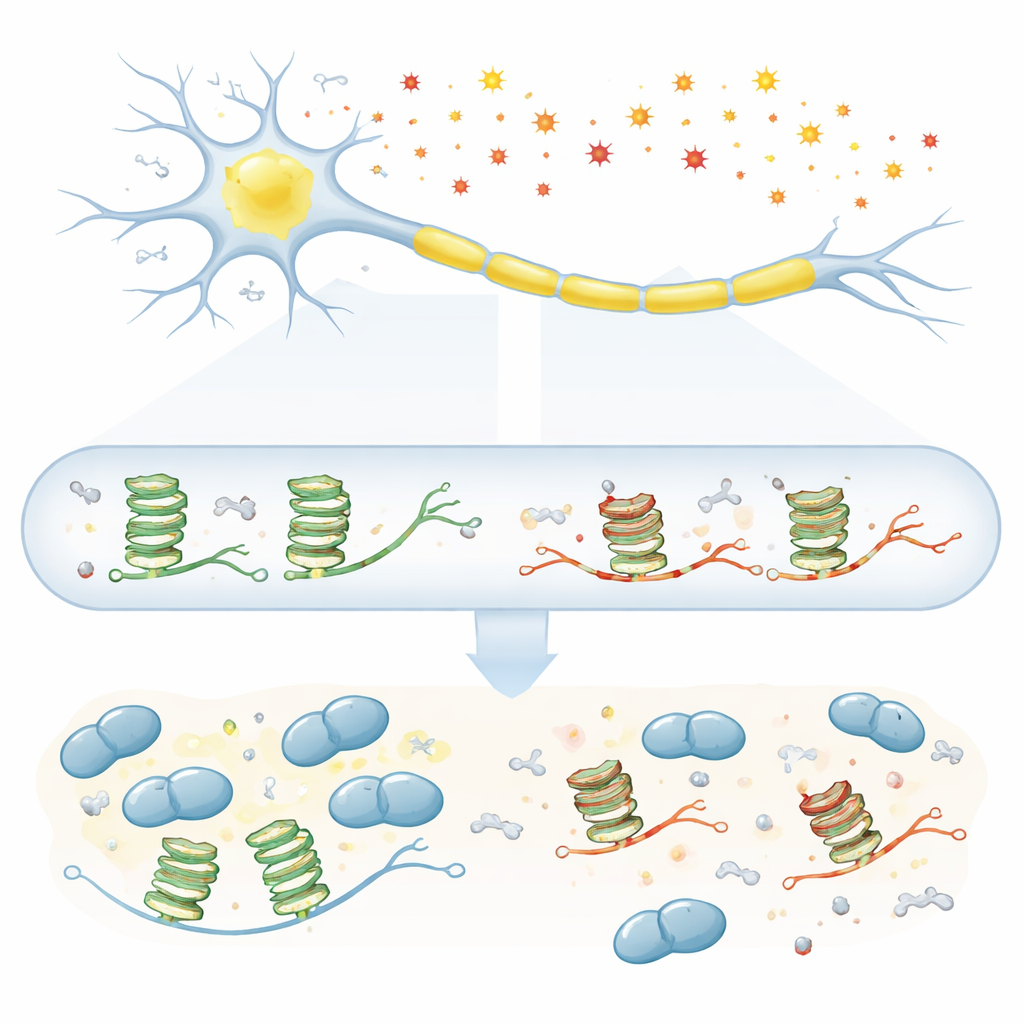
Un nodo fragile dell’RNA nel cuore dei motoneuroni
I motoneuroni dipendono dal trasporto a lunga distanza dei messaggi di RNA lungo gli assoni affinché le proteine possano essere sintetizzate in loco, vicino alle connessioni con i muscoli. Molti di questi messaggi portano un «nodo» strutturale speciale chiamato G-quadruplex, formato da tratti ricchi della base guanina. Proteine come TDP-43 riconoscono questo nodo e agganciano l’RNA a granuli di trasporto che si muovono lungo l’assone. Il problema è che la guanina è anche la base più facile da ossidare quando le cellule sono sotto stress da specie reattive dell’ossigeno, che si accumulano con l’età. Indizi precedenti suggerivano che i G-quadruplex e TDP-43 siano centrali nella SLA, ma non era chiaro in che modo l’ossidazione di questi nodi dell’RNA potesse interferire con la loro collaborazione.
Osservare lo stress ossidativo che deforma le forme dell’RNA
I ricercatori hanno prima esposto cellule neuroblastoma umane al perossido di idrogeno, un comune agente ossidante, e poi hanno esaminato lo stato delle strutture a G-quadruplex. I segnali da una sonda sensibile ai G-quadruplex sono diminuiti all’aumentare dello stress ossidativo, indicando che questi compatti nodi dell’RNA stavano perdendo la loro forma normale. Per definire la chimica coinvolta, il gruppo ha quindi costruito RNA sintetici capaci di formare G-quadruplex e ha introdotto intenzionalmente diverse quantità di 8-oxoguanina, una nota forma ossidata della guanina riscontrata nei neuroni invecchiati e nei tessuti di SLA. Utilizzando una serie di strumenti biofisici, hanno mostrato che anche livelli modesti di questa modifica allentano l’impilamento ordinato del G-quadruplex, sebbene l’esito esatto dipenda dalla sequenza di RNA circostante. 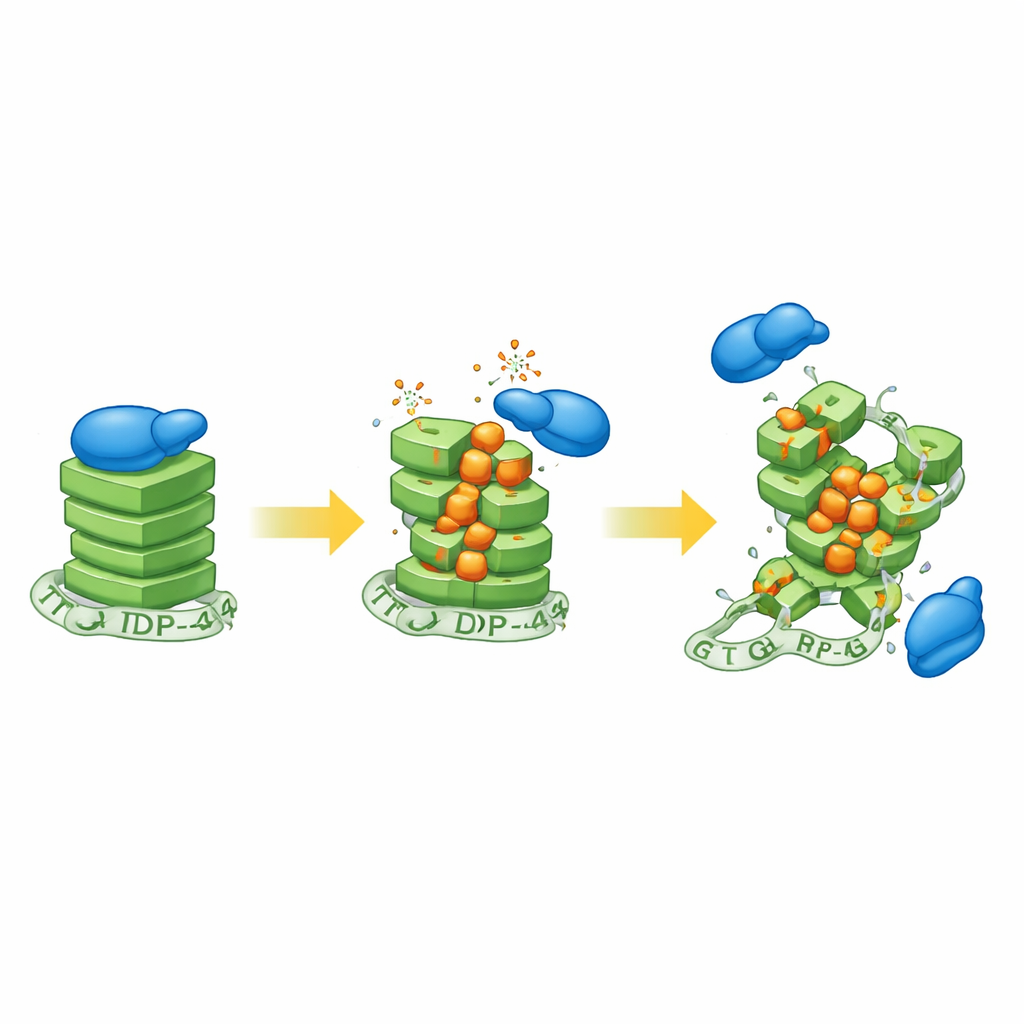
Nuovi difetti: basi non corrispondenti e filamenti mal appaiati
Un’analisi più approfondita ha rivelato due tipi distinti di problemi strutturali. In un G-quadruplex derivato dal messaggio PSD-95, le guanine ossidate tendevano a appaiarsi in modo inappropriato con adenine vicine, formando «mismatch» che deformano sottilmente il ripiegamento. Questi mismatch apparivano più facilmente a livelli intermedi di ossidazione, quando l’RNA poteva ancora assemblarsi in maniera transitoria in un G-quadruplex che metteva in contatto partner sbagliati. In un altro G-quadruplex tratto dal messaggio CaMKIIα, un’ossidazione intensa destabilizzava così fortemente il nodo intramolecolare abituale che le guanine rimaste intatte cercavano partner su altri filamenti di RNA, promuovendo G-quadruplex anomali intermolecolari. Strutture così mal cablate potrebbero aggrovigliare diversi RNA tra loro e interferire con il normale traffico di RNA all’interno dei neuroni.
Quando l’RNA danneggiato perde il suo partner proteico
Lo studio ha poi chiesto come questi nodi deformati interagiscono con TDP-43. Usando saggi di legame su gel, i ricercatori hanno mostrato che TDP-43 preferisce nettamente i G-quadruplex intatti e paralleli e che fallisce sempre più nel legarli man mano che vengono introdotte basi ossidate. La struttura di CaMKIIα, già molto compatta, si è rivelata particolarmente sensibile: anche una bassa ossidazione quasi aboliva il legame con TDP-43. Una seconda proteina, FUS — anch’essa collegata alla SLA — ha mostrato una perdita di affinità simile ma leggermente meno grave, suggerendo che l’ossidazione indebolisce in generale la presa delle proteine che legano i G-quadruplex. È interessante che, quando TDP-43 è stato miscelato con RNA moderatamente ossidati, i dati indicavano che la proteina si legava a una forma intermedia instabile del G-quadruplex piuttosto che a un nodo completamente ripiegato, suggerendo una lotta dinamica tra stabilizzazione e disgregazione.
Vulnerabilità aggiuntiva nelle proteine mutate associate alla SLA
Il lavoro ha inoltre esaminato dieci varianti di TDP-43 trovate in pazienti con SLA, la maggior parte con modifiche in una coda flessibile ricca di glicina che regola finemente il riconoscimento dell’RNA. Tutti questi mutanti legavano già i G-quadruplex normali più debolmente rispetto alla proteina wild-type. Quando sono stati introdotti come competitori G-quadruplex di RNA ossidati, i mutanti sono risultati ancora meno capaci della proteina normale nel riconoscere e legare le strutture danneggiate. Alcune varianti localizzate in regioni particolarmente predisposte al disordine sono state le più colpite. Ciò suggerisce un doppio colpo negli individui anziani che portano tali mutazioni: non solo il loro TDP-43 è intrinsecamente meno efficace, ma l’ossidazione legata all’età ne erode ulteriormente la capacità di accompagnare messaggi cruciali lungo gli assoni dei motoneuroni.
Cosa significa per la comprensione della SLA
In sintesi, questo studio mostra che il danno chimico guidato dall’età rimodella nodi delicati dell’RNA che guidano il trasporto dei messaggi nei motoneuroni, e questi nodi deformati non collaborano più efficacemente con TDP-43 o proteine correlate. Il risultato è una maggiore probabilità di carico di RNA mal indirizzato o bloccato, proprio negli assoni lunghi e vulnerabili che mantengono il controllo dei muscoli. Per le persone che ereditano anche mutazioni in TDP-43, questo indebolimento indotto dall’ossidazione delle interazioni RNA–proteina può spingere neuroni già sotto stress più vicino al cedimento. Illuminando questa catena di eventi sottile ma potente — dallo stress ossidativo all’alterazione dell’architettura dell’RNA fino al trasporto compromesso — il lavoro evidenzia l’ossidazione degli RNA a G-quadruplex come un promettente collegamento molecolare tra invecchiamento e SLA e come potenziale bersaglio per future terapie protettive.
Citazione: Ishiguro, A. Impact of G-quadruplex RNA oxidation on its conformational dynamics and interaction with ALS-associated TDP-43. Sci Rep 16, 8802 (2026). https://doi.org/10.1038/s41598-026-39767-y
Parole chiave: sclerosi laterale amiotrofica, ossidazione dell'RNA, G-quadruplex, TDP-43, degenerazione dei motoneuroni