Clear Sky Science · it
Identificazione di biomarcatori correlati al danno della barriera emato-encefalica nell’infarto cerebrale mediante analisi trascrittomica
Perché è importante per l’ictus e la salute cerebrale
Quando una persona subisce un ictus causato dall’ostruzione di un vaso nel cervello, le immagini possono mostrare il danno ma resta difficile prevedere chi svilupperà edema peggiore, sanguinamento o disabilità a lungo termine. Gran parte di quel danno avviene presso il guardiano protettivo del cervello, la barriera emato‑encefalica, che normalmente impedisce alle sostanze nocive nel sangue di fuggire nel delicato tessuto nervoso. Questo studio pone una domanda semplice ma cruciale: esistono segnali molecolari che rivelano quando questa barriera si sta rompendo, e potrebbero tali segnali in futuro guidare diagnosi e terapie migliori per i pazienti colpiti da ictus?
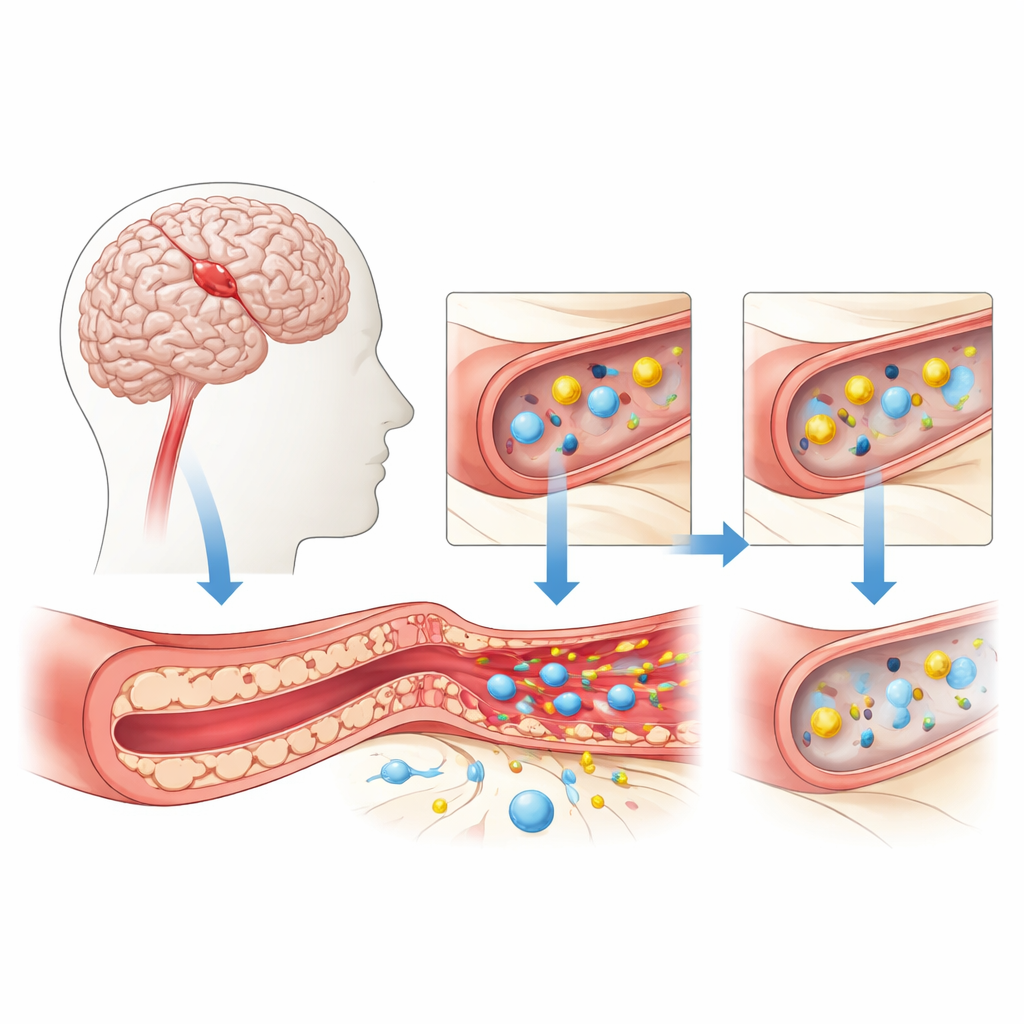
Il cancello protettivo del cervello sotto stress
La barriera emato‑encefalica è formata da cellule compattamente disposte che rivestono i piccoli vasi cerebrali. Queste cellule controllano con attenzione cosa può passare dal sangue al cervello, lasciando entrare nutrienti vitali come ossigeno e glucosio e bloccando tossine e cellule immunitarie che potrebbero danneggiare il tessuto. Durante un infarto cerebrale, o ictus ischemico, il flusso sanguigno diminuisce bruscamente. In assenza di ossigeno e zuccheri le cellule che rivestono i vasi si stressano e iniziano a perdere il loro sigillo stretto. Si aprono spazi tra di esse, liquidi filtrano nel tessuto circostante e messaggeri chimici dell’infiammazione invadono l’area, fenomeni che possono peggiorare l’edema e il danno cerebrale.
Ricreare il danno da ictus in laboratorio
Per indagare cosa accade dentro queste cellule di barriera, i ricercatori hanno usato una linea cellulare umana ben nota che imita il rivestimento dei vasi cerebrali. Hanno esposto queste cellule a un ambiente a basso ossigeno e privo di glucosio — chiamato deprivazione di ossigeno‑glucosio — per imitare le condizioni di un ictus, per poi ripristinare le condizioni normali a simulare trattamento e recupero. Hanno misurato la sopravvivenza cellulare, la fuoriuscita di un enzima indicatore di danno cellulare e la quantità di molecole infiammatorie rilasciate. Come previsto, il trattamento stressante ha ridotto la salute cellulare, aumentato segnali infiammatori quali IL‑1β, IL‑6 e TNF‑α e incrementato la fuoriuscita di un marcatore di danno chiamato LDH. Con il ripristino di ossigeno e nutrienti molte di queste alterazioni dannose si sono attenuate e le cellule hanno recuperato parte della loro capacità di formare tubi simili a vasi in un test di crescita.
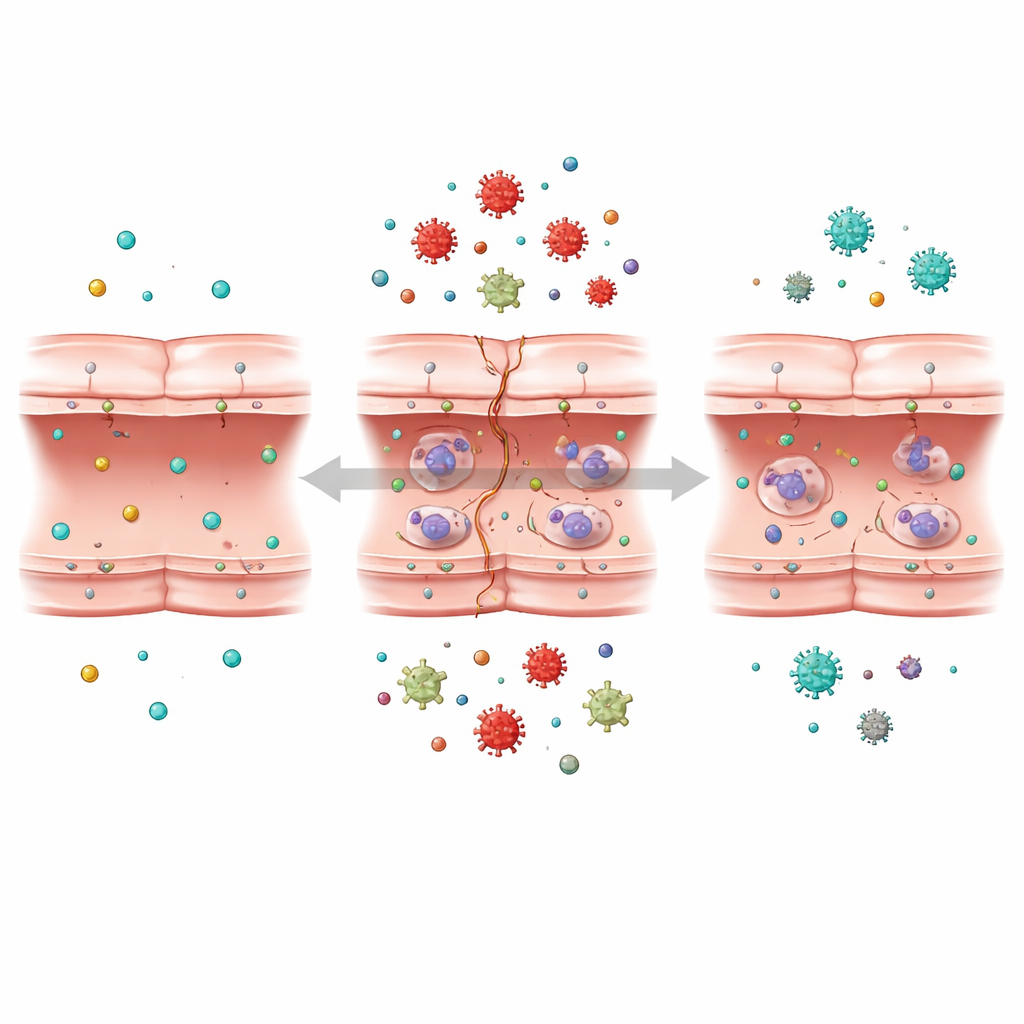
Ascoltare la conversazione molecolare della cellula
Il gruppo ha poi utilizzato una tecnica potente nota come trascrittomica, che legge i livelli di attività di migliaia di geni contemporaneamente. Confrontando cellule normali, cellule sottoposte a deprivazione di ossigeno‑glucosio e cellule lasciate recuperare, hanno identificato oltre mille geni la cui attività cambiava in risposta allo stress simile all’ictus. Usando strumenti di analisi avanzati e apprendimento automatico, hanno raggruppato i geni che si comportavano in modo simile e cercato quelli più strettamente legati al danno della barriera. Hanno scoperto che molti dei geni maggiormente coinvolti erano associati a tre strutture chiave all’interno della cellula: il ribosoma, che costruisce le proteine; il reticolo endoplasmatico, che le ripiega e le elabora; e i mitocondri, le piccole centrali energetiche che forniscono energia.
I ribosomi emergono come segnali rivelatori
Da questo ampio insieme di geni, i ricercatori hanno impiegato un algoritmo random forest — un tipo di apprendimento automatico basato su alberi decisionali — per restringere la lista a pochi geni particolarmente informativi. Hanno quindi ricostruito come le proteine corrispondenti interagiscono tra loro. Questa analisi ha evidenziato sei geni core, la maggior parte legati al ribosoma, la fabbrica proteica della cellula. Nella condizione simile all’ictus questi geni correlati al ribosoma risultavano più attivati, mentre la loro attività tornava verso livelli normali quando ossigeno e glucosio venivano ripristinati. Questo schema suggerisce che le modifiche nella macchina di produzione proteica della cellula possano essere un segnale precoce sensibile del danno e del recupero della barriera emato‑encefalica.
Cosa potrebbe significare per le cure future
Per il lettore non specialistico, il messaggio principale è che questo studio indica una nuova classe di “spie” molecolari che si attivano quando la barriera protettiva del cervello è lesa durante un ictus. Piuttosto che concentrarsi solo su noti colpevoli come gli enzimi che degradano la parete vascolare, il lavoro mostra che le stesse fabbriche proteiche della cellula rispondono vigorosamente al danno e si calmano quando le condizioni migliorano. Se ricerche future confermeranno che questi marcatori legati ai ribosomi possono essere rilevati in campioni di pazienti, ad esempio nel sangue, i medici potrebbero un giorno usarli per valutare l’entità del danno alla barriera, per tempificare interventi che riducono infiammazione ed edema e per testare nuovi farmaci volti a preservare questo cruciale guardiano della salute cerebrale.
Citazione: Liu, X., He, Y., Zhang, N. et al. Identification of blood-brain barrier injury-related biomarkers in cerebral infarction using transcriptomic analysis. Sci Rep 16, 8119 (2026). https://doi.org/10.1038/s41598-026-39763-2
Parole chiave: ictus ischemico, barriera emato-encefalica, biomarcatori, geni ribosomiali, cellule endoteliali