Clear Sky Science · it
Ridondanza criptica tra PAR1b e PAR1a, due membri della famiglia di chinasi PAR1, nella sopravvivenza dei topi knockout per PAR1b
Come le cellule trovano piani di riserva per il DNA danneggiato
Le nostre cellule affrontano costantemente danni al DNA e, quando i sistemi di riparazione falliscono, il risultato può essere il cancro o la morte durante lo sviluppo. Questo studio esplora un sorprendete meccanismo di salvataggio nei topi: quando manca una proteina chiave che aiuta il noto gene legato al cancro BRCA1 a svolgere il suo ruolo, un parente stretto interviene silenziosamente. Il lavoro rivela come gli embrioni precoci possano riorganizzare i loro sistemi di controllo genico per sopravvivere, offrendo nuovi spunti sul perché alcuni difetti genetici siano letali mentre altri sono inaspettatamente tollerati.
Una famiglia di organizzatori cellulari con un ruolo nascosto
I ricercatori si sono concentrati su una famiglia di enzimi chiamati chinasi PAR1, che aiutano le cellule a mantenere la loro organizzazione interna. Un membro della famiglia, PAR1b, era stato in precedenza mostrato guidare BRCA1 nel nucleo cellulare, dove BRCA1 sovrintende alla riparazione accurata del DNA e protegge siti fragili della replicazione. La rimozione completa di BRCA1 nei topi è fatale nelle prime fasi dello sviluppo embrionale, a sottolinearne l’importanza. Eppure, in modo sconcertante, i topi privi completamente di PAR1b sopravvivono fino all’età adulta, nonostante PAR1b si trovi a monte di BRCA1. Questa discrepanza suggeriva che un’altra chinasi PAR1 potesse sostituire silenziosamente PAR1b in certe condizioni.
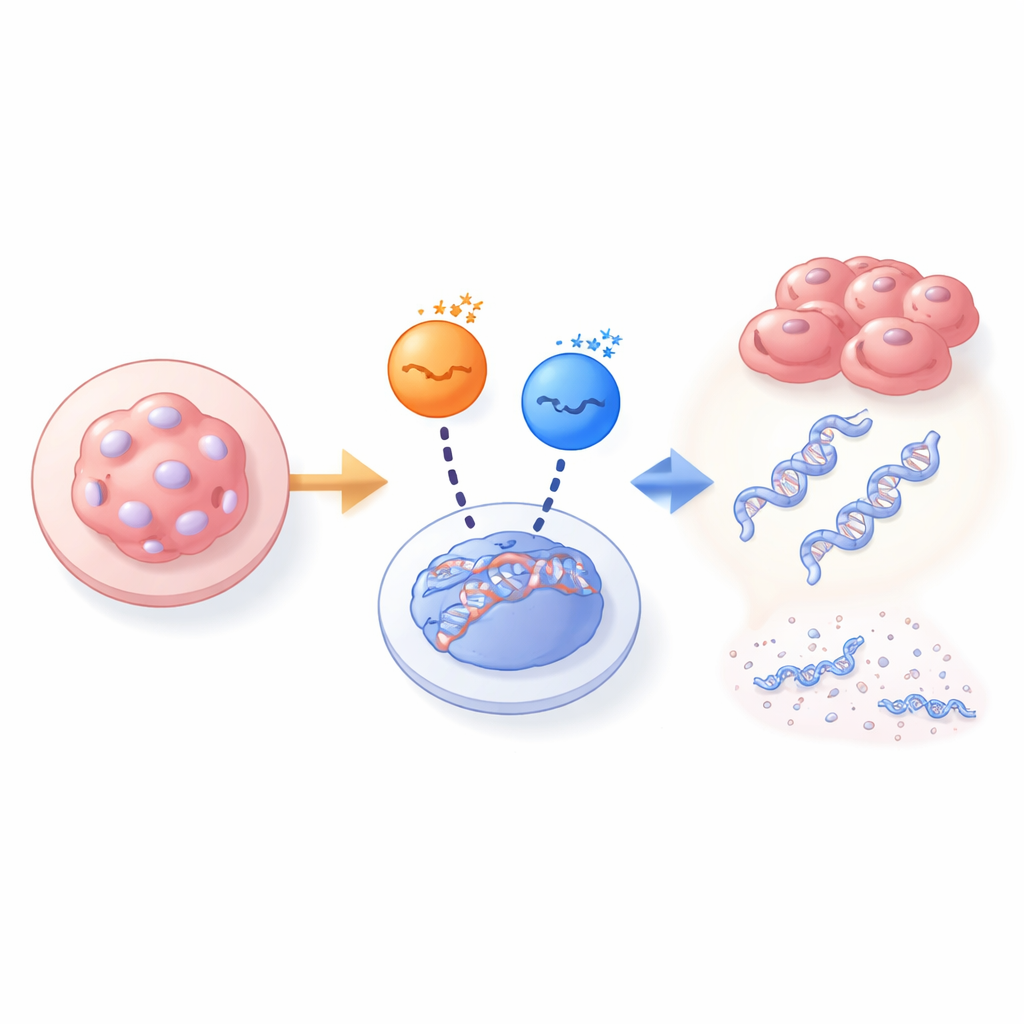
Quando una chinasi fallisce, un’altra interviene
Per indagare questo mistero, il team ha confrontato fibroblasti embrionali di topo derivati da embrioni normali con quelli provenienti da embrioni completamente privi di PAR1b. Nelle cellule normali, l’inibizione di PAR1b riduceva nettamente BRCA1 nel nucleo e provocava un’esplosione di marcatori di rotture del DNA, che a sua volta bloccava la crescita cellulare. L’abbattimento di altre chinasi PAR1 (PAR1a, PAR1c, PAR1d) aveva scarso effetto. Tuttavia, nelle cellule derivate da embrioni knockout per PAR1b, BRCA1 era ancora presente nel nucleo e il DNA rimaneva relativamente intatto, nonostante l’assenza di PAR1b. In queste cellule prive di PAR1b, la rimozione di PAR1a divenne ora letale, mentre la rimozione di PAR1c o PAR1d no. Questo cambio di dipendenza mostrava che PAR1a aveva assunto il ruolo di PAR1b nel guidare BRCA1, ma solo negli embrioni privi di PAR1b fin dall’inizio.
Rimodellamento epigenetico precoce come strategia di sopravvivenza
I ricercatori sospettavano che questo sistema di riserva nascosto fosse legato all’epigenetica — il modo in cui il DNA è impacchettato e chimicamente marcato per attivare o disattivare geni senza cambiare il codice genetico. Usando un’analisi genome‑wide dell’apertura della cromatina, hanno trovato migliaia di regioni in cui l’accessibilità del DNA differiva tra cellule normali e cellule prive di PAR1b. Molti cambiamenti riguardavano geni che controllano come i cromosomi sono avvolti e modificati, suggerendo una vasta riprogrammazione della rete di controllo genico. Un effetto di spicco riguardava il gene per 53BP1, una proteina che normalmente spinge le cellule verso una forma di riparazione del DNA rapida e imprecisa che si oppone al metodo più accurato di BRCA1. Nelle cellule senza PAR1b, il corpo del gene 53BP1 era più compattato e i suoi livelli di RNA e proteina erano molto più bassi.
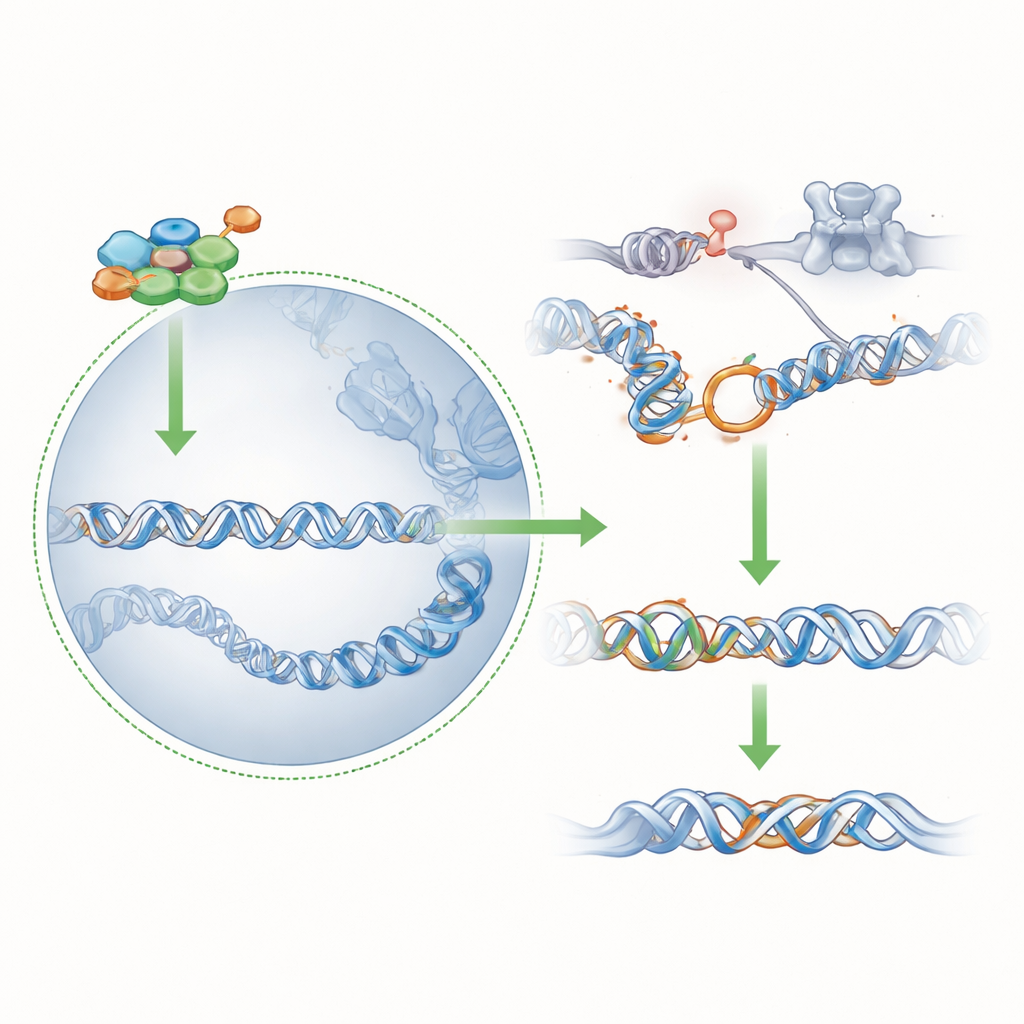
Inclinare l’equilibrio tra i percorsi di riparazione
Abbassando i livelli di 53BP1, l’embrione riduce efficacemente la sua dipendenza dalla piena attività di BRCA1: anche una quantità modesta di BRCA1 nucleare, portata da PAR1a invece che da PAR1b, può ora sostenere una riparazione sufficientemente accurata per mantenere le cellule in vita. Esperimenti che utilizzavano una proteina batterica in grado di spegnere tutte le chinasi PAR1 hanno confermato che la presenza nucleare di BRCA1 nelle cellule prive di PAR1b dipende ancora dall’attività della famiglia PAR1, in particolare da PAR1a. Nel complesso, i risultati disegnano uno scenario in cui la perdita precoce di PAR1b innesca un rapido rimodellamento della cromatina e delle reti di riparazione del DNA, silenziando un antagonista di BRCA1 (53BP1) e facendo emergere la capacità di PAR1a di sostituire PAR1b.
Cosa significa per malattie e terapie
Questo lavoro introduce il concetto di “ridondanza criptica”: una funzione di riserva che esiste ma è normalmente dormiente e diventa evidente solo quando un componente chiave viene perso molto precocemente nello sviluppo. Nei topi, questo permette agli embrioni di sopravvivere alla perdita di PAR1b, diversamente da quanto avviene con la perdita di BRCA1 stessa. I risultati suggeriscono anche che alcune persone con varianti dannose di PAR1b potrebbero sopravvivere perché meccanismi di riserva simili si attivano, sebbene non senza possibili conseguenze per la funzione cerebrale, il metabolismo o il rischio di cancro. A lungo termine, capire come gli aggiustamenti epigenetici precoci silenzino 53BP1 e spostino il controllo di BRCA1 da PAR1b a PAR1a potrebbe ispirare strategie per imitare deliberatamente questi cambiamenti — sia per proteggere cellule che hanno perso PAR1b sia per modulare i percorsi di riparazione del DNA nella terapia del cancro.
Citazione: Murata-Kamiya, N., Del Valle Lazarte, A.A., Kikuchi, I. et al. Cryptic redundancy between PAR1b and PAR1a, two members of the PAR1 kinase family, in the survival of PAR1b-knockout mice. Sci Rep 16, 5971 (2026). https://doi.org/10.1038/s41598-026-39737-4
Parole chiave: BRCA1, riparazione del DNA, ridondanza delle chinasi, regolazione epigenetica, sviluppo embrionale