Clear Sky Science · it
La variante p.Arg676Cys di Sema5A associata al disturbo dello spettro autistico attiva la via Arf6/FE65 e provoca una morfogenesi cellulare aberrante
Come una piccola modifica può disturbare il cablaggio cerebrale
Il disturbo dello spettro autistico influisce su come le persone comunicano, interagiscono e rispondono al mondo circostante, ma i passaggi biologici che portano da una modifica del DNA a una funzione cerebrale alterata sono spesso misteriosi. Questo studio approfondisce una di queste variazioni genetiche in una proteina «guida» del cervello chiamata Sema5A e mostra, con dettaglio insolito, come un singolo blocco costitutivo scambiato in quella proteina possa spingere i neuroni in fase di sviluppo a far crescere rami eccessivamente lunghi e aggrovigliati. Capire questo errore microscopico nel cablaggio potrebbe alla fine aiutare gli scienziati a progettare terapie che riportino le cellule cerebrali verso una forma più sana.
Cellule cerebrali che crescono troppo
Durante lo sviluppo cerebrale, i neuroni giovani inviano lunghe e sottili estensioni che cercano i partner giusti, formando i circuiti alla base del pensiero e del comportamento. Questa crescita deve essere strettamente controllata: troppo poco ramificarsi e le cellule non si connettono; troppo e i circuiti possono diventare rumorosi o mal cablati. Lavori precedenti avevano mostrato che una versione di Sema5A legata all’autismo, in cui un amminoacido alla posizione 676 è cambiato da arginina a cisteina, induce i neuroni in coltura a sviluppare processi insolitamente lunghi. Il nuovo studio si è proposto di scoprire quali interruttori interni e proteine ausiliarie questo Sema5A mutato utilizzi per guidare una crescita così sfrenata.
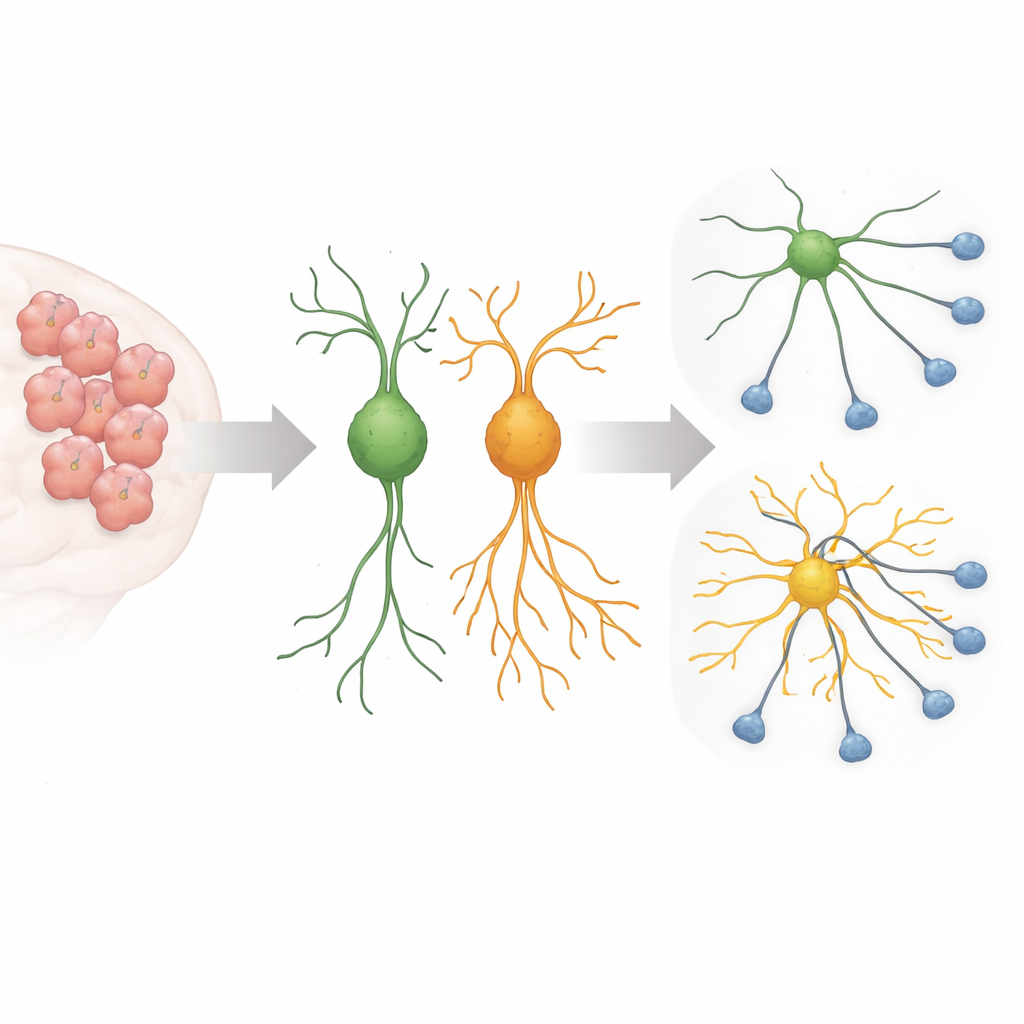
Un segnale fuorviante all’interno della cellula
I ricercatori si sono concentrati su un piccolo interruttore molecolare chiamato Arf6 e su una proteina impalcatura detta FE65, entrambe note per contribuire a modellare le membrane cellulari e lo scheletro interno che sostiene le estensioni cellulari. Utilizzando un sistema CRISPR–Cas13 per ridurre selettivamente queste proteine in cellule murine neuronali e in neuroni primari di topo, hanno scoperto che abbassare Arf6 o FE65 riduceva nettamente la crescita eccessiva indotta dalla Sema5A mutata. I processi lunghi e filamentosi si accorciavano verso lunghezze più tipiche e i marcatori di maturazione neuronale diminuivano, suggerendo che l’effetto della mutazione dipende fortemente da questa specifica via di segnalazione.
Collegarsi al motore della forma cellulare
All’interno dei neuroni, una famiglia di molecole agisce come un «motore» della forma controllando l’actina, il filamento strutturale principale nei rami cellulari. Un componente chiave di questa famiglia, Rac1, normalmente si attiva per favorire l’estensione dei neuriti, ma un’attività eccessiva può provocare crescita incontrollata. Il gruppo ha dimostrato che nelle cellule con Sema5A normale, Arf6 è necessario per l’attivazione ordinaria di Rac1 durante una crescita sana, mentre FE65 non è essenziale. Con la Sema5A mutata, tuttavia, sia Arf6 sia FE65 diventano critici: ridurre ciascuno di essi, o sovraccaricare la cellula con la sola regione di FE65 che lega il suo partner ELMO2, riportava l’attività anormalmente alta di Rac1 verso livelli normali. Ciò implica che la versione dannosa di Sema5A sfrutta specificamente un complesso Arf6–FE65–ELMO2–DOCK5 per sovrastimolare Rac1 e spingere i neuriti a crescere troppo.
Un hub affollato di partner di segnalazione
Per capire come questi elementi si assemblano, gli scienziati hanno anche osservato i «signalosomi» a base ELMO2—aggregati di proteine che si formano per trasmettere segnali di crescita. Quando Arf6 o FE65 venivano ridotti, le cellule che esprimevano la Sema5A mutata formavano meno di questi complessi ELMO2 nei loro corpi e nelle punte in crescita, coerente con l’idea che Arf6 e FE65 aiutino a costruire la macchina che trasforma la mutazione di Sema5A in un cambiamento fisico della forma cellulare. Il lavoro si inserisce in un quadro più ampio in cui piccoli interruttori molecolari come Arf6 e Rac1, aiutati da impalcature come FE65, fungono da hub centrali che collegano molti geni associati all’autismo all’architettura finale dei circuiti cerebrali.
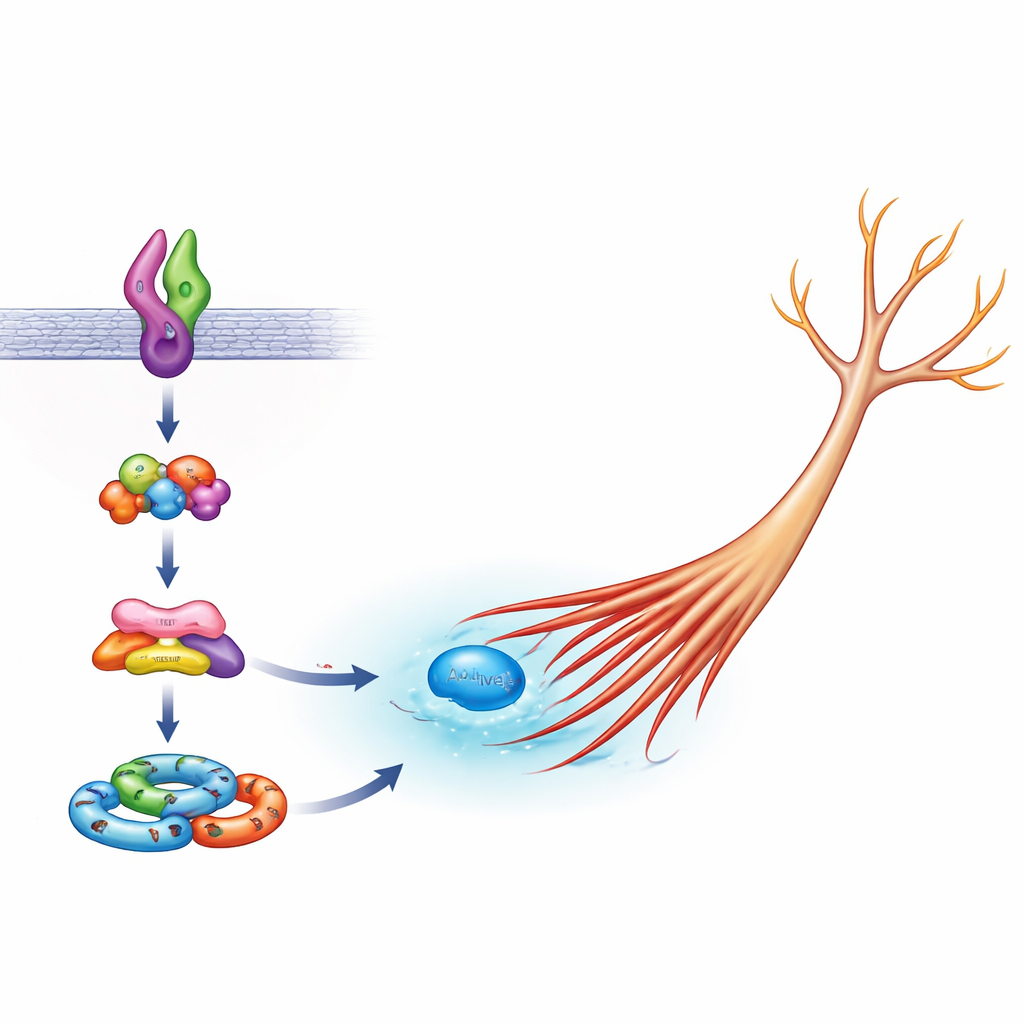
Perché questa catena microscopica è importante
Per un non specialista, l’alfabeto di nomi proteici può sembrare lontano dall’esperienza vissuta dell’autismo. Eppure questo studio offre un ponte concreto: traccia come una precisa modifica genetica in Sema5A può iperattivare una catena specifica di molecole ausiliarie, inducendo i neuroni a estendere i propri rami troppo oltre e potenzialmente a cablare il cervello in modi atipici. Identificando Arf6, FE65 e il complesso di segnalazione ELMO2 come anelli cruciali di questa catena, il lavoro evidenzia potenziali bersagli farmacologici futuri. In linea di principio, farmaci che modulino delicatamente questa via iperattiva potrebbero un giorno contribuire a correggere i cambiamenti di forma cellulare alla base delle forme di autismo legate a Sema5A, aggiungendo un tassello importante al più ampio puzzle dei disturbi dello sviluppo neurocomportamentale.
Citazione: Takahashi, M., Yako, H., Miyamoto, Y. et al. Autism spectrum disorder-associated Sema5A p.Arg676Cys drives Arf6/FE65 signaling and aberrant cell morphogenesis. Sci Rep 16, 9423 (2026). https://doi.org/10.1038/s41598-026-39722-x
Parole chiave: disturbo dello spettro autistico, mutazione Sema5A, morfogenesi neuronale, segnalazione Rac1, via Arf6 FE65