Clear Sky Science · it
L’esposizione al cadmio induce fibrosi renale inibendo la via di segnalazione hsa_circ_0075684/miR-363-3p/KLF4
Perché una minaccia metallica nascosta conta
Il cadmio è un metallo tossico che si insinua nella nostra vita attraverso il cibo, il fumo di sigaretta e l’inquinamento industriale. Una volta nell’organismo, persiste per decenni, con una particolare tendenza ad accumularsi nei reni. Questo studio esplora come l’esposizione cronica al cadmio danneggi il tessuto renale e individua un piccolo circuito molecolare che potrebbe segnalare il problema precocemente—offrendo la speranza di prevenire la malattia renale cronica anziché limitarci a trattarla in fase avanzata.
Il lento logoramento del rene
I reni fungono da filtri del corpo, eliminando i rifiuti dal sangue. Il cadmio, tuttavia, si accumula in questi filtri nel corso di molti anni ed è fortemente associato alla malattia renale cronica. Gli autori osservano che i casi globali di malattia renale cronica sono in aumento e che non esiste un modo efficace per rimuovere il cadmio una volta che si è depositato nei reni. Piuttosto che concentrarsi sulla bonifica, sostengono che sia necessario trovare metodi per rilevare e interrompere il danno in fase iniziale—in particolare il processo noto come fibrosi, in cui il tessuto sano viene gradualmente sostituito da tessuto cicatriziale rigido che compromette la funzione renale.
Piccoli messaggi di RNA e un interruttore protettivo
I ricercatori si sono concentrati su una piccola molecola regolatoria chiamata miR-363-3p, parte di una famiglia di brevi frammenti di RNA che modulano finemente l’attività genica. Lavori precedenti avevano mostrato che questo RNA risultava aumentato in operai con avvelenamento da cadmio di lunga durata. Utilizzando grandi banche dati genomiche pubbliche, hanno cercato un circuito di controllo più ampio attorno a miR-363-3p nel tessuto renale esposto al cadmio. Hanno identificato una via in tre componenti: un RNA circolare (hsa_circ_0075684) che può “assorbire” miR-363-3p, la molecola miR-363-3p stessa e una proteina chiamata KLF4 che contribuisce a proteggere le cellule renali dalla cicatrizzazione. Insieme, questo trio sembra funzionare come un interruttore molecolare che mantiene la fibrosi sotto controllo.
Dalle colture cellulari ai topi in laboratorio
Per mettere alla prova questa ipotesi, il team ha esposto cellule tubolari renali umane a dosi crescenti di cadmio. Con l’aumentare dei livelli di cadmio, le cellule hanno mostrato segni classici di fibrosi: le proteine associate alla cicatrizzazione aumentavano, mentre una proteina che aiuta le cellule a mantenere adesione e struttura normale diminuiva. Allo stesso tempo, i livelli di miR-363-3p salivano, mentre sia KLF4 sia l’RNA circolare diminuivano. Esperimenti genetici hanno dimostrato che miR-363-3p si lega direttamente a KLF4 e ne riduce la produzione, e che l’RNA circolare normalmente sequestra miR-363-3p, impedendogli di silenziare KLF4. Quando gli scienziati hanno aumentato miR-363-3p, le proteine della cicatrizzazione sono esplose e KLF4 è calato; quando hanno bloccato miR-363-3p o aumentato l’RNA circolare, KLF4 è risalito e i marcatori di fibrosi si sono attenuati, anche in presenza di cadmio.
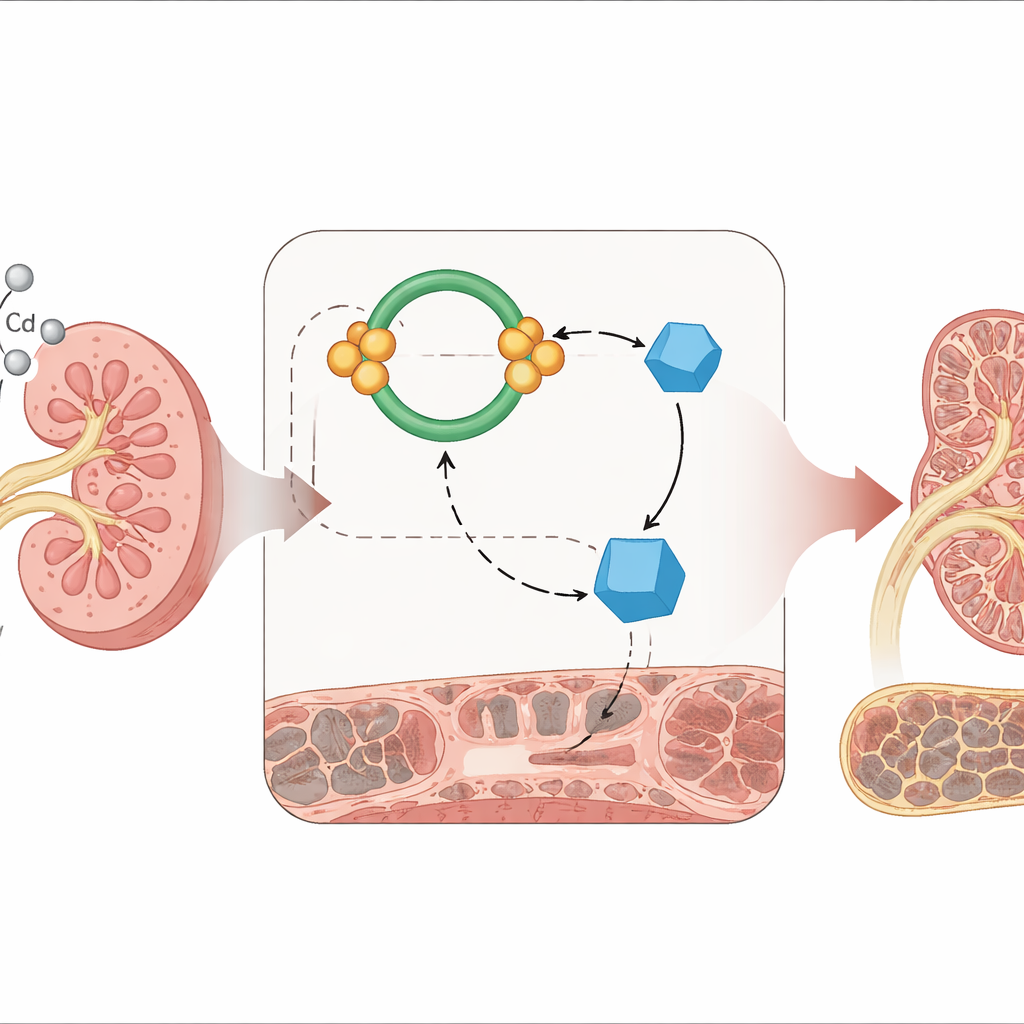
Confermare il danno nei reni viventi
I ricercatori hanno quindi utilizzato un modello murino per verificare se questo schema molecolare si manifestasse anche in animali vivi. I topi hanno ricevuto cadmio per via orale per tre mesi a dosi scelte per imitare un’esposizione ambientale prolungata. Al microscopio, i reni dei topi trattati con cadmio mostravano chiare alterazioni fibrotiche—fibre di collagene colorate in blu che riempivano gli spazi tra i tubuli. I test biochimici rispecchiavano i risultati delle colture cellulari: le proteine della cicatrizzazione aumentavano, la proteina protettiva KLF4 diminuiva e i livelli di miR-363-3p aumentavano nei reni, sostenendo l’idea che questa via sia attiva durante il lento danno da cadmio nel mondo reale.
Cosa significa per la protezione dei reni
Nel loro complesso, i risultati suggeriscono che il cadmio promuove la cicatrizzazione renale perturbando un delicato equilibrio tra un RNA circolare, un microRNA e una proteina protettiva. Quando il cadmio riduce l’RNA circolare e KLF4, miR-363-3p è libero di spingere le cellule verso la fibrosi. Per i non specialisti, il messaggio chiave è che spostamenti molecolari precoci—molto prima della comparsa dei sintomi—potrebbero un giorno fungere da segnali di allarme in esami del sangue o delle urine per persone a rischio di esposizione al cadmio. Sebbene siano necessari ulteriori studi clinici, soprattutto nei pazienti umani, questa via appena mappata indica strumenti futuri per rilevare e forse attenuare il danno renale indotto dal cadmio prima che si instauri una cicatrizzazione irreversibile.
Citazione: Zhou, J., Huang, Y., Li, G. et al. Cadmium exposure induces renal fibrosis by inhibiting hsa_circ_0075684/miR-363-3p/KLF4 signaling pathway. Sci Rep 16, 8754 (2026). https://doi.org/10.1038/s41598-026-39715-w
Parole chiave: esposizione al cadmio, fibrosi renale, microRNA, tossicologia ambientale, malattia renale cronica