Clear Sky Science · it
Efficacia letale delle strutture dell’ivermectina sui vettori della malaria e analisi in silico delle interazioni con i loro canali ionici per cloruro regolati dal glutammato
Trasformare un farmaco anti-parassiti in un killer di zanzare
L’ivermectina è nota soprattutto come medicinale contro i vermi parassiti negli esseri umani e negli animali, ma ha un effetto collaterale sorprendente: le zanzare che si nutrono di sangue trattato spesso muoiono. Questo solleva un’idea interessante per il controllo della malaria—somministrare ivermectina a persone o animali potrebbe ridurre le popolazioni locali di zanzare abbastanza da diminuire la trasmissione? Questo studio esplora in profondità come l’ivermectina e molecole correlate uccidono le zanzare Anopheles che trasmettono la malaria e quali cambiamenti potrebbero un giorno consentire alle zanzare di sfuggire ai suoi effetti.
Perché uccidere le zanzare tramite il sangue è importante
Il controllo tradizionale della malaria si basa su zanzariere e spray insetticidi, che colpiscono le zanzare dall’esterno. L’ivermectina offre una strategia diversa: quando persone o animali assumono il farmaco, il loro sangue diventa letale per le zanzare emofaghe. I ricercatori si sono concentrati su due importanti vettori della malaria nel Sud-Est asiatico, Anopheles dirus e Anopheles minimus, che mostrano grandi differenze nella suscettibilità all’ivermectina. Confrontando queste specie, il team sperava di capire perché il farmaco sia più letale in alcune zanzare rispetto ad altre e come la sua struttura chimica influenzi questo potere letale.
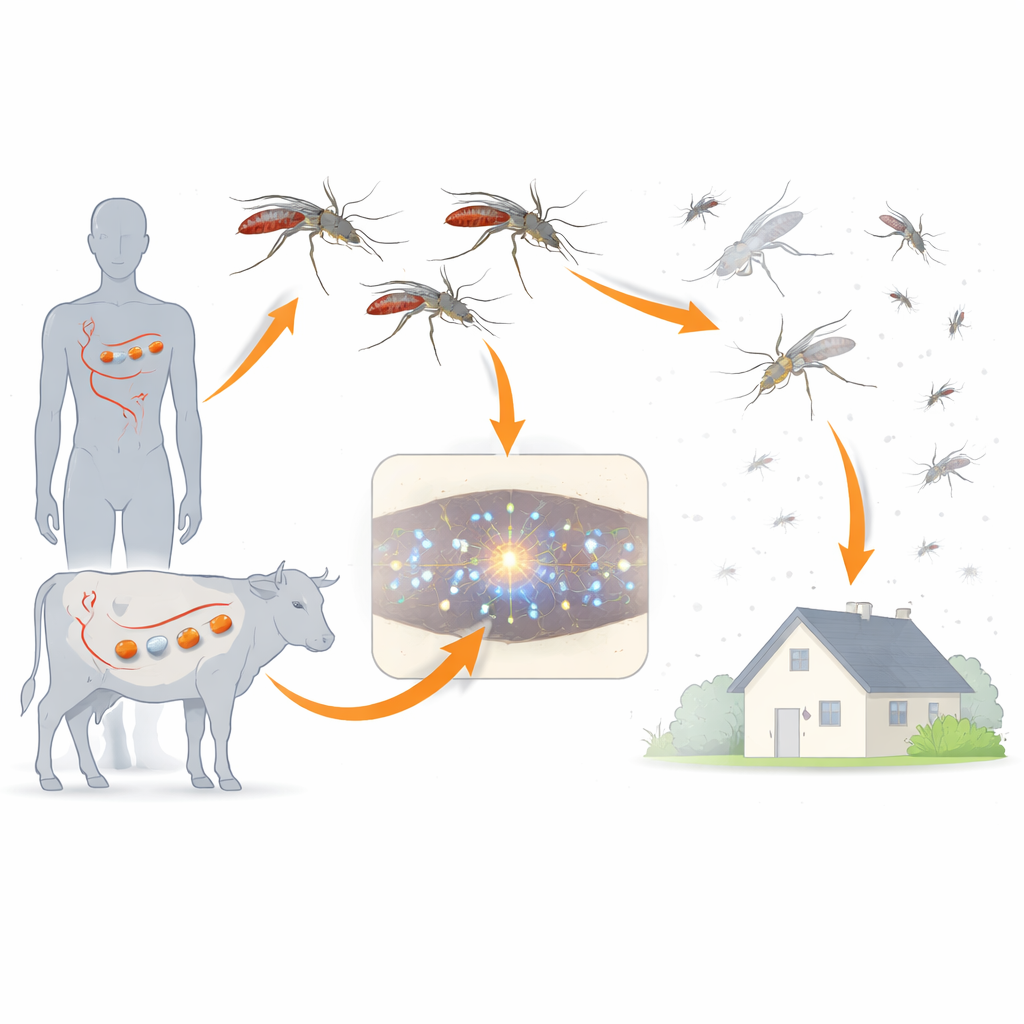
Testare quali parti del farmaco contano
L’ivermectina è una molecola ingombrante costruita attorno a un grande anello con due anelli zuccherini collegati. Il team ha confrontato l’ivermectina completa (con entrambi gli zuccheri) con una versione con un solo anello zuccherino (chiamata monosaccaride) e con un nucleo spogliato senza zuccheri (aglicone). Hanno somministrato questi composti, a diverse concentrazioni, a migliaia di zanzare in pasti di sangue e ne hanno seguito la sopravvivenza per dieci giorni. L’ivermectina completa è risultata altamente letale, soprattutto per An. minimus, mentre il monosaccaride era molto meno efficace e l’aglicone aveva quasi nessuna capacità letale a dosi realistiche. In altre parole, rimuovere un anello zuccherino ha trasformato un potente killer di zanzare in uno molto più blando, e rimuovere entrambi ha quasi annullato l’effetto.
Uno sguardo all’interno della porta nervosa della zanzara
L’ivermectina agisce su una piccola porta nelle cellule nervose e muscolari chiamata canale per cloruro regolato dal glutammato (GluCl). Quando questa porta viene forzata ad aprirsi, gli ioni cloruro entrano in massa, l’attività elettrica collassa e la zanzara diventa paralizzata fino alla morte. Utilizzando avanzate previsioni di struttura proteica e docking computerizzato, i ricercatori hanno costruito modelli tridimensionali del canale GluCl di Anopheles e hanno simulato come l’ivermectina e le sue varianti si inseriscano nel canale. Hanno scoperto che, nelle zanzare, una specifica porzione dell’anello proteico vicino al poro—contenente un aminoacido chiamato treonina nella posizione 304—può formare un legame a idrogeno con il secondo anello zuccherino dell’ivermectina. Questo legame, insieme ad attrazioni deboli nelle vicinanze, sembra stabilizzare una conformazione legata al farmaco che mantiene il canale aperto.
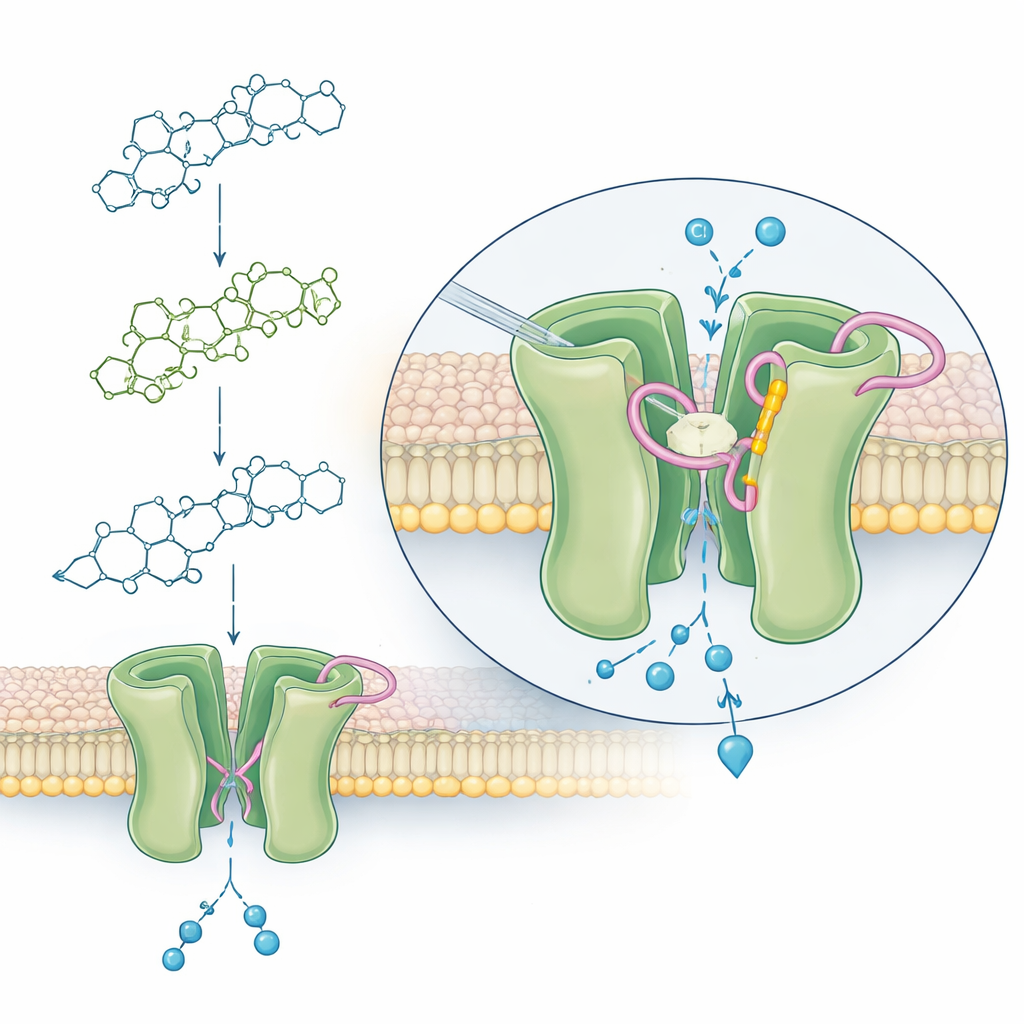
Perché alcune versioni uccidono e altre no
Le simulazioni hanno mostrato un modello coerente: l’ivermectina completa e tre principali prodotti di degradazione dell’ivermectina presenti negli esseri umani si estendono in profondità nel canale, permettendo al loro secondo anello zuccherino di interagire da vicino con l’anello chiave. Queste forme hanno tutte prodotto un forte legame predetto e, in lavori precedenti, si sono dimostrate altrettanto letali per le zanzare quanto il composto parentale. Il monosaccaride, privo di quel secondo anello zuccherino, poteva comunque toccare l’anello in modo debole ma non poteva formare lo stesso legame stabilizzante, coerente con la sua minore capacità letale. L’aglicone non entrava in contatto con l’anello, in linea con la sua incapacità di uccidere le zanzare nei test di alimentazione. Tra tutte le strutture, è emersa anche un’interazione condivisa con un’altra parte del canale (nella subunità opposta) come importante, suggerendo che diversi punti di contatto cooperano per bloccare la porta aperta.
Prospettive su resistenza e strumenti migliori
I risultati suggeriscono che il secondo anello zuccherino dell’ivermectina—e la sua capacità di legarsi a uno specifico anello del canale GluCl della zanzara—è centrale per il suo effetto letale sulle zanzare. Questa immagine più chiara di come il farmaco si adatti al canale evidenzia punti deboli potenziali dove future mutazioni potrebbero ridurre il legame e portare a resistenza. Indica anche come i chimici potrebbero modificare molecole simili all’ivermectina per mantenere o aumentare la loro efficacia contro le zanzare. Pur basandosi su modelli computerizzati che richiedono ancora conferme sperimentali, lo studio rafforza l’argomento a favore di strategie basate sull’ivermectina come parte dell’arsenale per il controllo della malaria e indica caratteristiche molecolari che sarà cruciale monitorare man mano che tali strategie vengono implementate.
Citazione: Nguyen, M.N., Jones, A.K., Hotwagner, D. et al. Lethal effects of ivermectin structures on malaria vectors and in silico analysis of interactions with their glutamate-gated chloride ion channels. Sci Rep 16, 8141 (2026). https://doi.org/10.1038/s41598-026-39698-8
Parole chiave: ivermectina, vettori della malaria, zanzare Anopheles, canali ionici, resistenza agli insetticidi