Clear Sky Science · it
Indirizzamento di tipi neuronali specifici nel cervello di primati non umani usando un immunotossina ricombinante specifica per CD25 murino
Perché questo studio cerebrale è importante
Capire come gruppi specifici di cellule cerebrali controllino il movimento, l’emozione e il comportamento è fondamentale per curare disturbi come la malattia di Parkinson e l’autismo. Ma il cervello è una foresta densa di cellule intrecciate, e la maggior parte degli strumenti abbatte molti alberi insieme. Questo studio presenta un modo per rimuovere solo un tipo scelto di neurone nel cervello di una scimmia, con danni collaterali minimi, aprendo la strada a esperimenti molto più precisi su come particolari circuiti modellano comportamento e malattia.
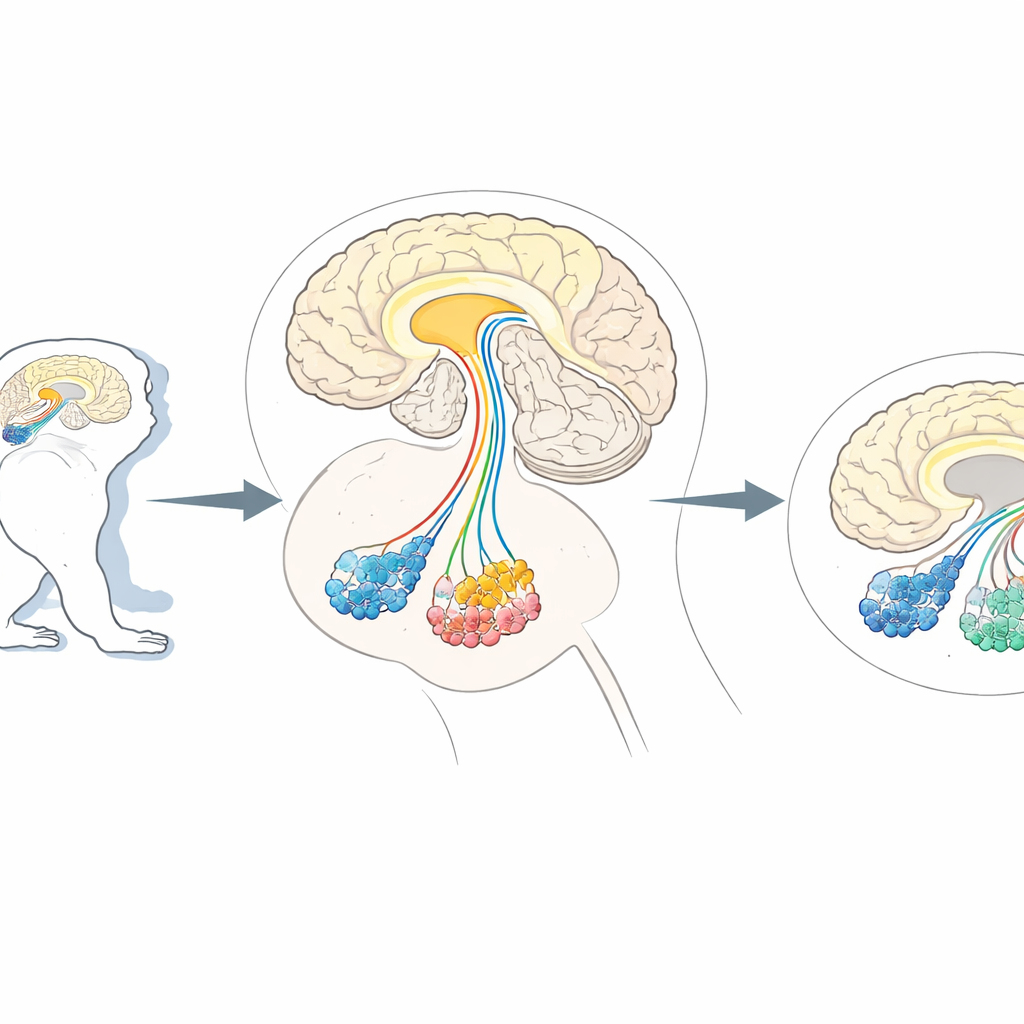
La necessità di una "potatura" cellulare precisa
I ricercatori ricorrono spesso a primati non umani, come marmoset e macachi, perché i loro cervelli sono organizzati in modo molto simile al nostro. Questi animali sono modelli preziosi per condizioni che colpiscono funzioni cerebrali superiori, dai problemi motori parkinsoniani ai cambiamenti del comportamento sociale simili all’autismo. I metodi esistenti possono silenziare o stimolare vie specifiche, ma rimuovere effettivamente solo un tipo di neurone in questi cervelli complessi senza danneggiarne altri è rimasto difficile. Lavori precedenti nei topi usavano un trucco: neuroni selezionati venivano ingegnerizzati per esprimere un marcatore di superficie cellulare chiamato CD25, riconosciuto da una tossina progettata che uccideva solo quelle cellule marcate. Tuttavia, lo stesso marcatore si trova naturalmente nelle cellule immunitarie e forse in alcune cellule cerebrali dei primati, aumentando il rischio che la tossina attacchi bersagli sbagliati nelle scimmie.
Progettare un bisturi molecolare più sicuro
Gli autori si sono posti l’obiettivo di costruire un nuovo bisturi molecolare pensato per l’uso nei primati. Invece di mirare alla versione umana di CD25, si sono concentrati sulla versione murina, molto meno simile al CD25 naturale presente nelle scimmie. Hanno prima immunizzato un coniglio con la proteina CD25 murina e usato un metodo su chip per selezionare singole cellule del coniglio che producevano anticorpi che si legavano fortemente al CD25 murino ma non alla forma umana. Da questi hanno identificato un anticorpo di spicco, chiamato RMAb-52, con un’affinità molto elevata. Hanno quindi unito le parti chiave di questo anticorpo con un frammento tossico del batterio Pseudomonas per creare una singola proteina ingegnerizzata, un’"immunotossina" denominata anti-mCD25-PE38.
Mettere lo strumento alla prova
In esperimenti in provetta, la nuova immunotossina si è legata al CD25 murino molto più saldamente che al CD25 umano, confermandone la selettività. Applicata a cellule coltivate ingegnerizzate per esprimere CD25 murino, la tossina ha ridotto drasticamente la loro sopravvivenza a dosi molto basse, lasciando invece intatte le cellule che esprimevano CD25 umano. Successivamente, il gruppo ha lavorato su marmoset vivi. Usando un vettore virale speciale che viaggia retrogradamente lungo le fibre nervose, hanno introdotto il gene del CD25 murino nei neuroni dopaminergici che inviano segnali da una regione profonda del cervello, la substantia nigra, allo striato, una via cruciale per il controllo del movimento. Dopo aver dato al virus il tempo di attivare il marcatore in questi neuroni, hanno iniettato la proteina anti-mCD25-PE38 direttamente nell’area midbrain bersaglio.
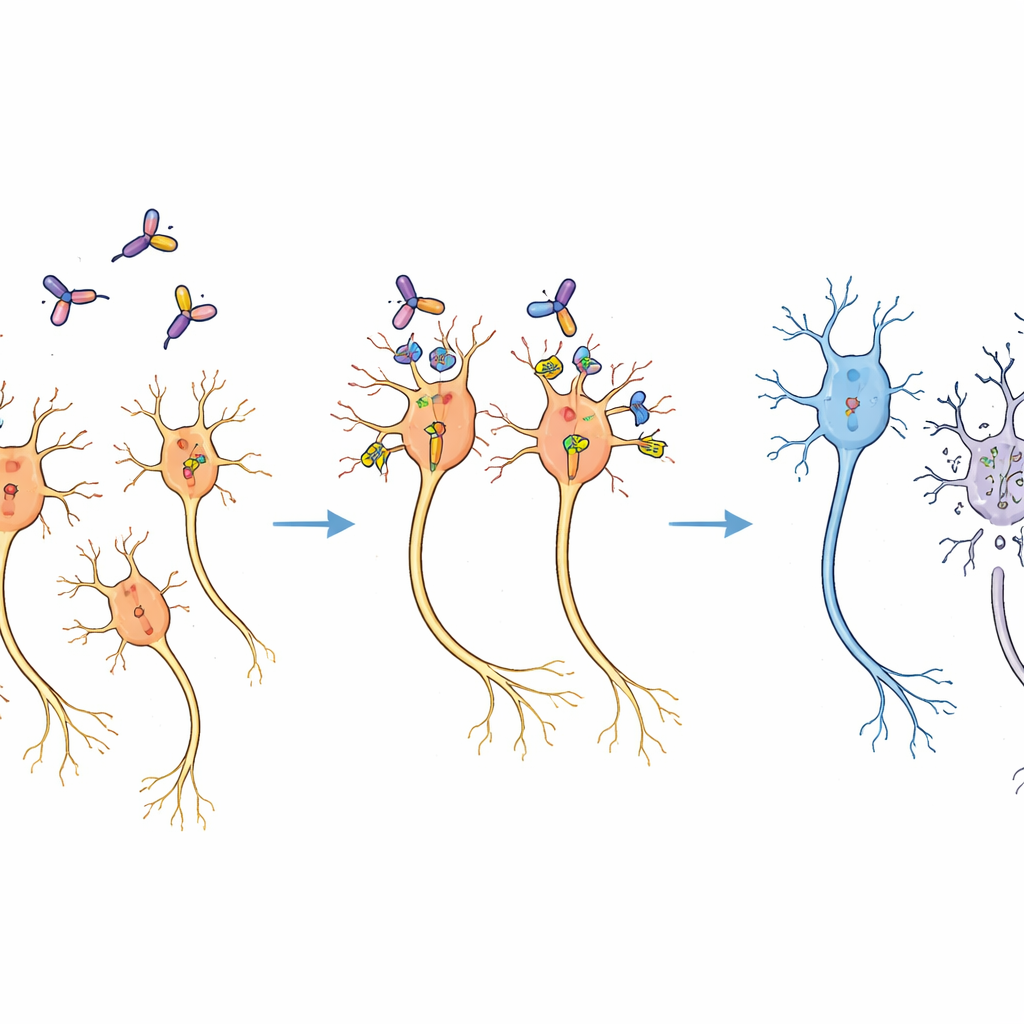
Perdita selettiva senza danni diffusi
Dopo due settimane dal trattamento, le sezioni cerebrali dei marmoset hanno raccontato una storia chiara. Sul lato che aveva ricevuto l’immunotossina, il numero di neuroni dopaminergici era ridotto a circa due terzi rispetto al lato non trattato, come mostrato dalla colorazione per un enzima che produce dopamina. Tuttavia il tessuto cerebrale circostante appariva normale al microscopio, e altre regioni cerebrali che avevano ricevuto il vettore virale non mostravano una perdita evidente di cellule. Esperimenti pilota avevano già stabilito un intervallo di dosi che evitava danni tissutali non specifici, e la dose scelta rientrava ampiamente in questa finestra di sicurezza. Il pattern di perdita corrispondeva alla diffusione prevista di virus e tossina, indicando che i neuroni erano stati eliminati specificamente perché erano stati ingegnerizzati per esprimere CD25 murino, non perché la tossina stesse danneggiando le cellule in modo indiscriminato.
Cosa significa per la ricerca cerebrale futura
Per un lettore non specialista, il messaggio chiave è che i ricercatori hanno costruito un pulsante di cancellazione altamente selettivo per popolazioni neuronali scelte nei cervelli dei primati. Combinando un sistema di consegna virale retrogrado con un’immunotossina specifica per il topo, possono rimuovere vie definite — per esempio circuiti dopaminergici implicati nella malattia di Parkinson — risparmiando le cellule vicine. Questa strategia evita reazioni crociate pericolose con il CD25 endogeno dell’animale e dovrebbe essere particolarmente utile quando quel recettore naturale è presente o aumentato nella malattia. A lungo termine, questo approccio aiuterà gli scienziati a mappare come singole rotte nel cablaggio cerebrale contribuiscono al movimento, al processo decisionale e ai sintomi psichiatrici, avvicinandoci a terapie mirate che regolano circuiti malfunzionanti anziché influenzare ampiamente l’intero cervello.
Citazione: Kobayashi, T., Kato, S., Kimura, S. et al. Targeting of specific neuronal types in the non-human primate brain by using a murine CD25-specific recombinant immunotoxin. Sci Rep 16, 8247 (2026). https://doi.org/10.1038/s41598-026-39662-6
Parole chiave: neuroscienze nei primati non umani, indirizzamento con immunotossina, neuroni dopaminergici, circuiti cerebrali del marmoset, modelli della malattia di Parkinson