Clear Sky Science · it
Una cassetta degli attrezzi multimodale nel pesce zebra per studiare la barriera emato‑encefalica in salute e malattia
Perché i vasi cerebrali che perdono sono importanti
Quando i vasi sanguigni nel cervello o nell'occhio iniziano a perdere, liquidi e proteine filtrano nel tessuto nervoso circostante causando edema che può offuscare la vista o compromettere le funzioni cognitive. Questo tipo di «inondazione»—nota come edema vasogenico—contribuisce alla perdita della vista nei diabetici, all'ictus, al trauma cerebrale e ad alcune forme di demenza. Tuttavia gli scienziati non hanno ancora metodi semplici ed economici per osservare in tempo reale il cedimento di questa barriera protettiva. Questo studio presenta un modello versatile nel pesce zebra che permette ai ricercatori di vedere, misurare e sondare come l'iperglicemia indebolisca la barriera dei vasi cerebrali, accelerando potenzialmente la ricerca di nuovi trattamenti.
Un pesciolino con un vantaggio chiaro
Le larve di pesce zebra offrono una finestra unica sul cervello vivo. A differenza dei mammiferi, il loro corpo è trasparente nelle prime fasi di vita e i vasi sanguigni cerebrali possono essere resi fluorescenti al microscopio. Gli autori hanno sfruttato questo aspetto concentrandosi sulla barriera emato‑encefalica, il sigillo stretto tra sangue e tessuto cerebrale che somiglia alla barriera emato‑retinica interna che protegge i nostri occhi. Poiché gli stessi tipi cellulari e molti dei medesimi proteini protettivi sono condivisi tra cervello e retina, il gruppo ha usato la barriera cerebrale nel pesce zebra come surrogato per studiare malattie come l’edema maculare diabetico e altri disturbi neurovascolari, in un sistema più rapido, più etico e meno costoso rispetto ai modelli murini tradizionali.
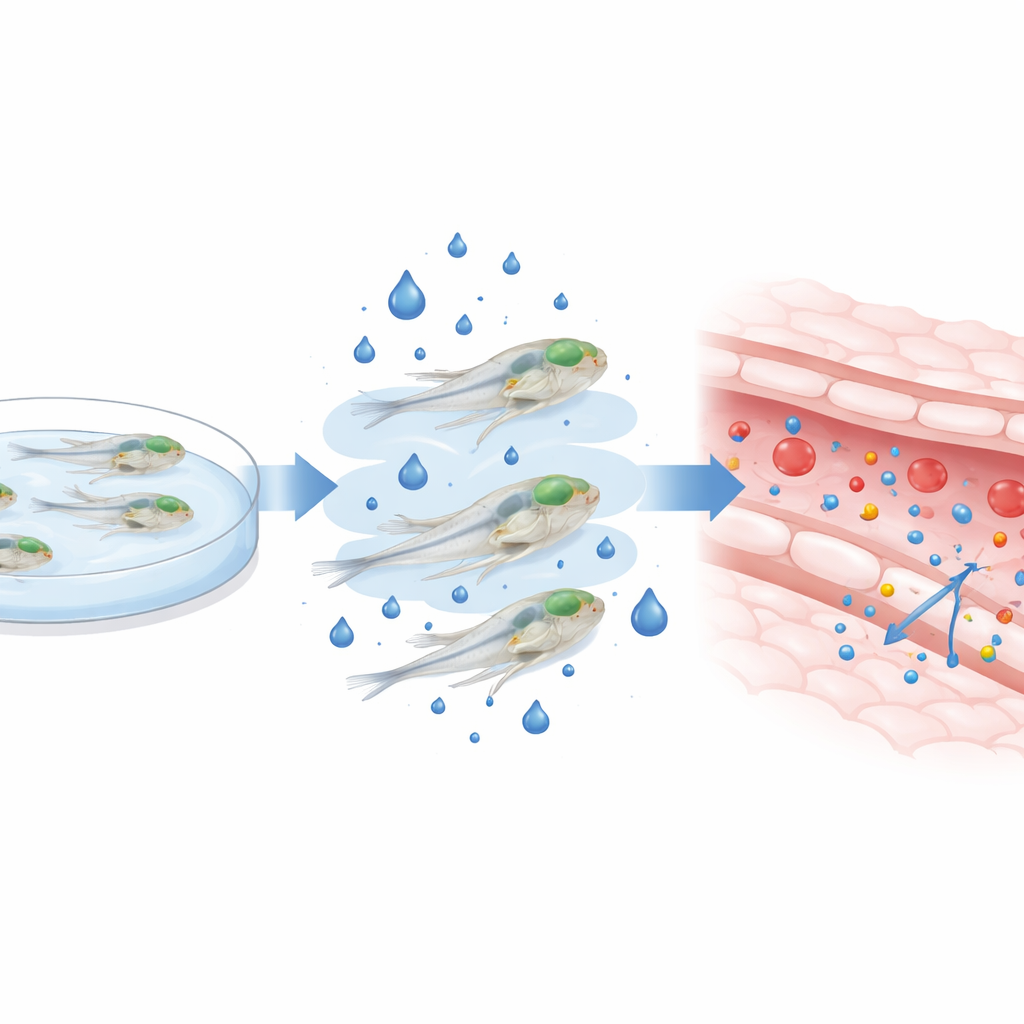
Aumentare lo zucchero nel sangue nei pesciolini
Per riprodurre l'iperglicemia tipica del diabete, i ricercatori hanno allevato le larve di pesce zebra in acqua contenente glucosio aggiunto tra il terzo e il quinto giorno dopo la fecondazione—una finestra critica in cui la barriera cerebrale è ancora in maturazione. Hanno confermato che questo bagno esterno di zucchero aumentava i livelli interni di glucosio di diverse volte senza uccidere le larve o alterarne la morfologia complessiva. Con i pesci ancora vivi e nuotanti, hanno iniettato nel circolo coloranti fluorescenti di diverse dimensioni e usato microscopi confocali ad alta risoluzione per tracciare quanto colorante fuoriusciva dai vasi cerebrali nel tessuto circostante. Dopo due giorni di esposizione ad alto glucosio, sia molecole coloranti piccole sia grandi sono fuoriuscite di più nel cervello, specialmente alla dose più elevata, indicando che la barriera era diventata più permeabile.
Cosa succede alla parete vascolare
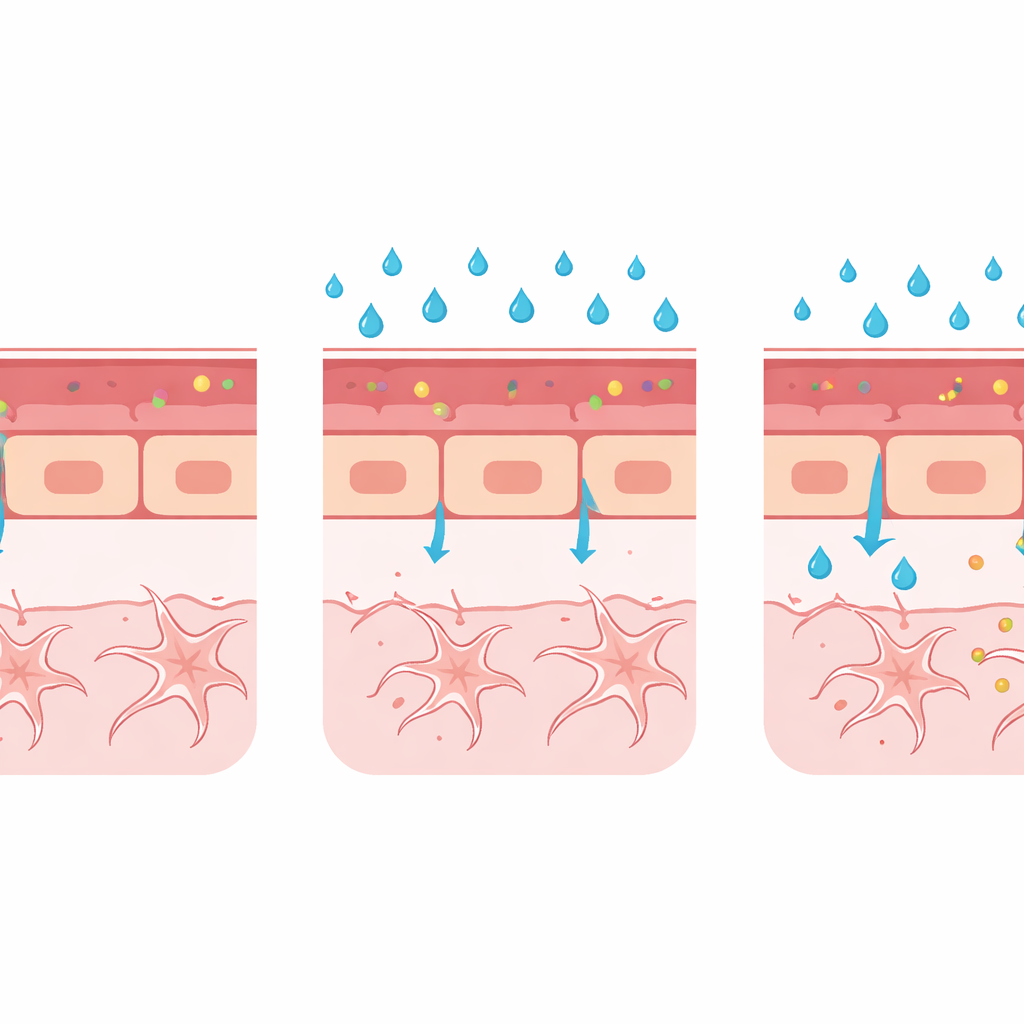
Oltre a misurare la perdita, il gruppo ha costruito una «cassetta degli attrezzi» multimodale per esaminare cosa non funzionava nella parete vascolare. Hanno misurato il diametro di una arteria cerebrale chiave e riscontrato che l'iperglicemia causava dilatazione del vaso—un cambiamento precoce osservato anche nelle persone con retinopatia diabetica. Utilizzando pesci zebra ingegnerizzati per evidenziare specifiche proteine, hanno mostrato che l'alto glucosio riduceva i livelli di claudina‑5, un componente principale delle giunzioni strette tra cellule vascolari adiacenti, e aumentava i livelli di PLVAP, una proteina associata a vasi immaturi e inclini alla perdita che facilitano il trasporto attraverso lo strato cellulare. La microscopia elettronica, che rivela strutture a scala nanometrica, ha confermato un lieve allargamento delle giunzioni tra le cellule, sebbene le piccole cavità di trasporto chiamate caveole fossero troppo rare per essere quantificate in modo affidabile in questa prima analisi.
Una piattaforma flessibile per la ricerca sulle malattie future
Complessivamente, questi cambiamenti—maggiore fuoriuscita di colorante, vasi più larghi, giunzioni cellulari indebolite e aumento di PLVAP—disegnano un quadro coerente: l'alto zucchero nel sangue può ritardare o compromettere la corretta formazione della barriera nel cervello in sviluppo. Il modello non riproduce ancora la rottura di una barriera pienamente matura, com’è nelle malattie croniche umane, ma eccelle nel mostrare come condizioni dannose durante lo sviluppo possano impedire alla barriera di sigillarsi adeguatamente. Poiché le tecniche sono compatibili con una gamma di linee reporter fluorescenti e con imaging avanzato, la stessa piattaforma può essere ampliata per studiare altri fattori scatenanti del cedimento della barriera, come molecole infiammatorie, alterazioni delle cellule di supporto come periciti e glia, o perturbazioni in vie di segnalazione chiave.
Cosa significa per i pazienti
Per i non specialisti, il messaggio principale è che questo lavoro fornisce una piattaforma pratica e vivente per osservare la perdita della parete protettiva del cervello sotto stress, usando pesci piccoli e trasparenti invece di mammiferi di maggiori dimensioni. Seguendo in tempo reale come l'iperglicemia rimodella struttura e funzione dei vasi, i ricercatori possono più rapidamente individuare quali molecole e tipi cellulari mirare per mantenere la barriera intatta. In ultima istanza, tali intuizioni potrebbero guidare lo sviluppo di nuovi farmaci o strategie terapeutiche per prevenire o ridurre la fuoriuscita di liquidi negli occhi e nel cervello—aiutando a preservare la vista e a proteggere le funzioni cognitive nelle persone con diabete e altre malattie neurovascolari.
Citazione: Bakker-van Bugnum, N., Snijders, E.E., Hogendorp, E.F. et al. A zebrafish multimodal toolbox to study the blood-brain barrier in health and disease. Sci Rep 16, 9422 (2026). https://doi.org/10.1038/s41598-026-39616-y
Parole chiave: barriera emato‑encefalica, modello pesce zebra, complicanze diabetiche, perdita vascolare, malattia neurovascolare