Clear Sky Science · it
Modellazione strutturale e analisi di docking di mutazioni missenso canoniche e nuove associate alla resistenza in Escherichia coli sudanese
Perché questo è importante per la salute quotidiana
Le infezioni resistenti agli antibiotici non sono più curiosità mediche rare; minacciano sempre più i trattamenti di routine per le infezioni delle vie urinarie, gli interventi chirurgici e le terapie intensive. Questo studio esamina in dettaglio ceppi di Escherichia coli dal Sudan e pone una domanda molto specifica: come riorganizzano le piccole variazioni genetiche nelle proteine batteriche il modo in cui funzionano gli antibiotici comuni? Usando modellazione strutturale al computer invece di costosi esperimenti di laboratorio, gli autori scoprono schemi di resistenza nascosti che i test standard e i database globali possono non rilevare—soprattutto in contesti a risorse limitate dove la resistenza sta crescendo più rapidamente. 
Dentro la cassetta degli attrezzi del batterio
I ricercatori si sono concentrati sulle mutazioni “missenso”—cambiamenti di una singola lettera del DNA che sostituiscono un mattoncino della proteina con un altro. Hanno analizzato sequenze di genomi completi di 55 isolati di E. coli raccolti in Sudan e si sono focalizzati sulle proteine batteriche che sono bersagli diretti delle principali classi di antibiotici, incluse fluorchinoloni, macrolidi e rifampicina. Questi bersagli comprendono enzimi che agiscono sul DNA (girasia e topoisomerasi IV), il ribosoma che produce proteine e l’enzima RNA polimerasi. Delle 71 mutazioni trovate in queste proteine, 19 sono state segnalate da diversi strumenti predittivi come probabilmente dannose per la funzione proteica e, in modo significativo, la maggior parte di queste sembrava essere variazioni nuove non ancora catalogate nei database globali della resistenza.
Nuove criticità in bersagli noti
Alcuni dei cambiamenti più rilevanti si sono raggruppati in una proteina ribosomiale chiamata L22, che contribuisce a formare il tunnel attraverso il quale le proteine appena sintetizzate escono dal ribosoma. Questa regione funge anche da sito di ancoraggio per i macrolidi come l’eritromicina. Lo studio ha identificato un insieme denso di mutazioni di L22 precedentemente non segnalate, molte presenti in un singolo ceppo, che si trovano proprio lungo questo tunnel e nei punti di contatto con l’RNA ribosomiale. Le analisi computazionali suggeriscono che diverse di queste variazioni destabilizzano la struttura locale o ne aumentano la flessibilità, rimodellando potenzialmente il tunnel in modo che le molecole di macrolide si adattino meno saldamente. Allo stesso tempo, mutazioni di resistenza più note e “canoniche” sono apparse nelle proteine che processano il DNA, ParC e ParE, e nell’RNA polimerasi, confermando che i ceppi sudanesi condividono alcuni segni globali di resistenza pur conservando varianti locali proprie.
Come i cambiamenti di forma indeboliscono la presa dell’antibiotico
Il gruppo non si è limitato alle liste di sequenze e ha indagato come queste mutazioni possano modificare l’adattamento tridimensionale tra antibiotici e bersagli. Utilizzando simulazioni di docking molecolare, hanno confrontato come diversi farmaci si legano a proteine normali e mutate. Per la topoisomerasi IV ParC, mutazioni chiave vicino al sito di contatto con il farmaco hanno indebolito sostanzialmente il legame previsto con il fluorchinolone trovafloxacina, riflettendo una presa più allentata nel punto di giunzione enzima–DNA–farmaco. Nella proteina correlata ParE, le mutazioni hanno ridotto modestamente il legame con la novobiocina. Al contrario, una mutazione nuova nella girasi GyrA sembra destabilizzare la struttura dell’enzima senza alterare in modo evidente l’affinità di legame del fluorchinolone moxifloxacina, suggerendo che la resistenza può emergere talvolta alterando sottilmente le prestazioni enzimatiche piuttosto che espellere semplicemente il farmaco. 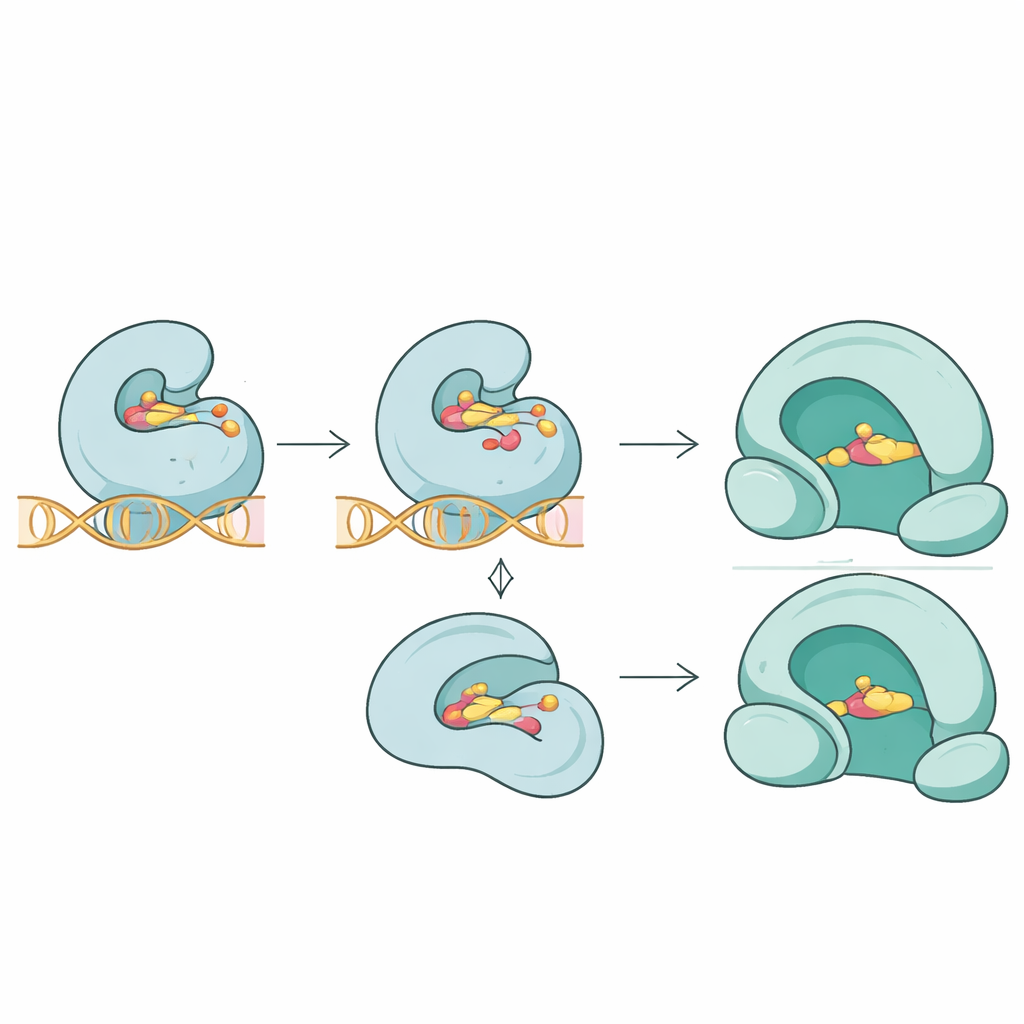
Effetti misti su farmaci diversi
Non tutte le mutazioni hanno avuto lo stesso impatto. Le modifiche classiche associate alla resistenza alla rifampicina nella proteina RNA polimerasi RpoB hanno prodotto scarsi effetti sul legame con un inibitore più recente e strutturalmente distinto che colpisce un sito vicino, suggerendo che farmaci futuri potrebbero essere progettati per aggirare i pattern di resistenza esistenti. Per la proteina ribosomiale L22, gli studi di docking con l’eritromicina hanno mostrato un mosaico di risultati: alcune mutazioni hanno indebolito il legame, altre hanno avuto poco effetto e una persino migliorato leggermente l’adattamento previsto. Questi risultati sottolineano che la resistenza raramente è bianca o nera; piuttosto, ogni mutazione sposta la stabilità della proteina, la sua flessibilità e il legame col farmaco in direzioni diverse, e l’effetto complessivo sul trattamento dipende da come questi cambiamenti si combinano all’interno di una cellula batterica vivente.
Cosa significa per i pazienti e la sorveglianza
Dal punto di vista non specialistico, il messaggio chiave è che i batteri in luoghi come il Sudan stanno evolvendo la resistenza sia attraverso vie ben note sia tramite percorsi meno noti. Le vie note coinvolgono mutazioni classiche già monitorate da programmi internazionali, ma questo studio mostra che molte mutazioni aggiuntive, arricchite localmente, possono anch’esse indebolire gli antibiotici in modi più sottili. Mappando questi cambiamenti su strutture proteiche dettagliate, gli autori forniscono una lista ristretta di mutazioni che andrebbero testate in laboratorio e considerate nei pannelli diagnostici regionali. In termini pratici, il loro lavoro sostiene che la modellazione computazionale intelligente può aiutare i paesi con capacità di laboratorio limitata a monitorare meglio la resistenza emergente, favorendo scelte terapeutiche più affidabili e ispirando progetti di farmaci che restino un passo avanti all’evoluzione batterica.
Citazione: Sage, E.E., Ibrahim, S.A.E., Firdaus-Raih, M. et al. Structural modeling and docking analysis of canonical and novel resistance-associated missense mutations in Sudanese Escherichia coli. Sci Rep 16, 8995 (2026). https://doi.org/10.1038/s41598-026-39491-7
Parole chiave: resistenza antimicrobica, Escherichia coli, mutazioni missenso, bioinformatica strutturale, Sudan