Clear Sky Science · it
Integrare il deep learning con la modellizzazione basata sulla fisica permette una previsione ad alta precisione dell’interfaccia antigene-anticorpo
Perché questo è importante per i farmaci del futuro
Gli anticorpi sono i missili guidati del nostro sistema immunitario e di molti farmaci moderni. Per progettare anticorpi migliori, gli scienziati devono sapere con precisione come un anticorpo afferra la sua molecola bersaglio, o antigene. Misurare queste strutture sperimentalmente è lento e costoso. Questo studio mostra come combinare il deep learning con la modellizzazione classica in stile fisico possa migliorare nettamente le previsioni al computer di dove anticorpo e antigene entrano in contatto, accelerando potenzialmente progettazione e screening degli anticorpi.
Trovare la zona di contatto
Gli anticorpi riconoscono i loro bersagli usando piccoli anelli flessibili alle loro estremità, detti regioni di legame, che si riuniscono a formare una patch di contatto. Questi anelli possono piegarsi e torcersi, e la zona corrispondente sull’antigene è spesso estesa e superficiale anziché formare una tasca profonda. Questa flessibilità e sottigliezza rendono il problema del docking — capire come le due forme si incastrano — estremamente difficile per i computer. I programmi di docking tradizionali provano molte posizioni relative delle due proteine e le valutano con regole fisiche come l’attrazione elettrostatica e lo spostamento dell’acqua, ma senza suggerimenti biologici spesso convergono su soluzioni errate.
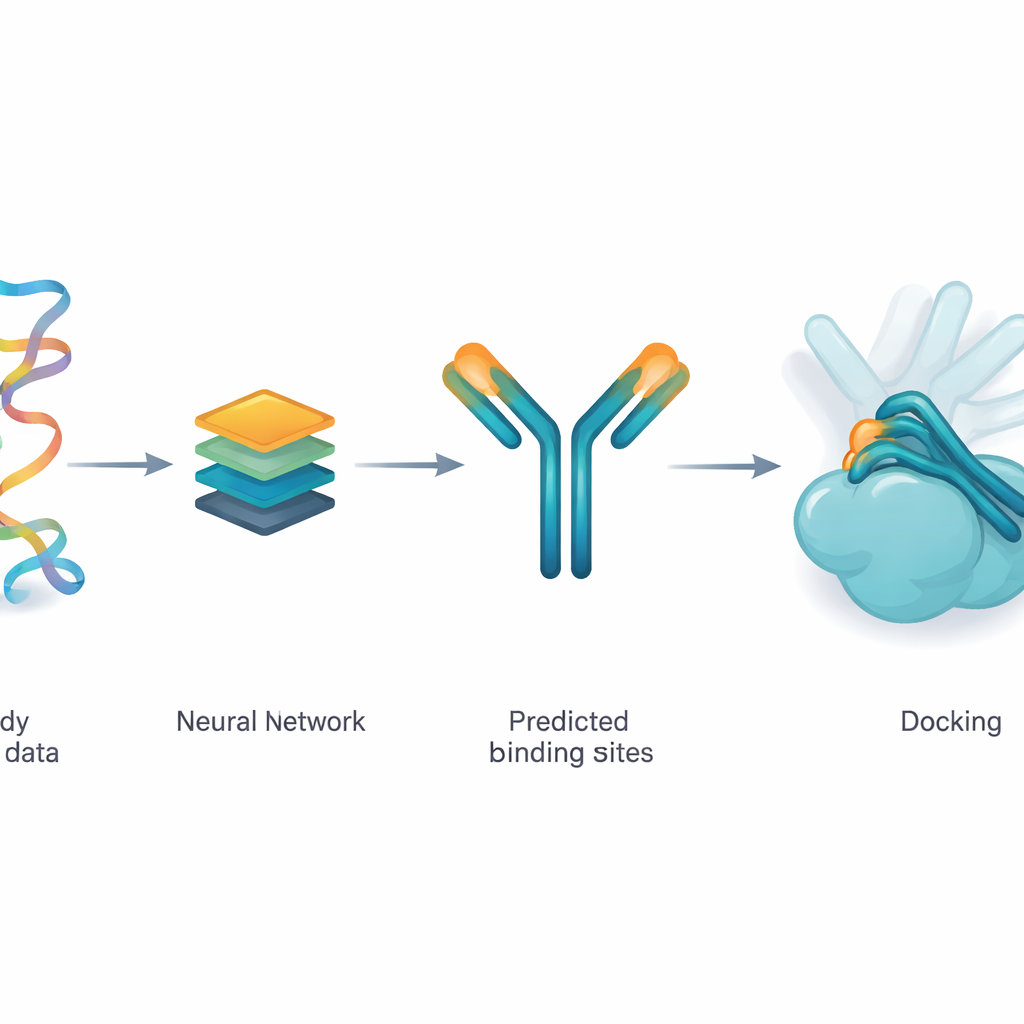
Insegnare a una rete a suggerire i punti di contatto probabili
Gli autori usano un modello di deep learning chiamato ParaDeep per indovinare quali aminoacidi su un anticorpo sono più probabili toccare l’antigene. ParaDeep fa questo usando solo la sequenza dell’anticorpo — l’ordine dei suoi mattoni costitutivi — senza necessitare della struttura 3D completa. Legge insieme le sequenze delle catene pesante e leggera, codifica le caratteristiche chimiche e posizionali e utilizza meccanismi di attenzione per evidenziare residui che sembrano buoni candidati al legame. Ogni posizione riceve un punteggio di probabilità; quelle sopra una soglia vengono trattate come una zona di contatto predetta che può essere riportata sulla struttura dell’anticorpo.
Guidare un motore fisico invece di sostituirlo
Invece di usare il deep learning per generare da zero complessi anticorpo–antigene, il team fornisce i residui di contatto predetti da ParaDeep a un motore di docking basato sulla fisica esistente chiamato PyDockWEB. Questo programma di docking campiona migliaia di modi possibili in cui anticorpo e antigene possono incontrarsi e li valuta con una funzione di energia. Nel nuovo framework, i residui di contatto predetti agiscono come vincoli morbidi: indirizzano la ricerca in modo che molte delle orientazioni campionate portino quei residui vicini alla superficie dell’antigene. È importante sottolineare che la valutazione fisica sottostante e il trattamento come corpi rigidi delle proteine rimangono immutati, rendendo il processo trasparente e relativamente leggero da eseguire.
Quanto migliorano le previsioni?
I ricercatori hanno testato il loro approccio ibrido su 50 complessi anticorpo–antigene noti presi da un database curato. Per ogni caso, hanno confrontato il docking “alla cieca” standard con il docking guidato dai vincoli di ParaDeep. Hanno misurato la precisione locale dell’interfaccia (quanto la regione di contatto predetta corrispondeva alla realtà), la somiglianza complessiva delle forme e un punteggio di qualità combinato ampiamente usato per valutare i modelli di docking. Su questo insieme, il metodo guidato ha ridotto notevolmente gli errori nel sito di legame, ha avvicinato le strutture complessive ai complessi reali e ha spostato molte predizioni da chiaramente sbagliate a categorie di qualità media o alta. Quasi la metà dei modelli guidati è finita nella fascia di alta qualità, contro circa un quarto per il docking alla cieca.
Cosa rende alcuni incastri più facili di altri
Il team ha anche esaminato perché alcuni complessi hanno beneficiato più di altri. Hanno scoperto che prevedere semplicemente più residui di contatto non garantiva il successo; ciò che contava era posizionare i vincoli nell’area giusta, non la loro quantità. Le interfacce più idrofile e con più segmenti di bobina flessibili tendevano a darsi meglio nel docking, probabilmente perché si accordavano con l’enfasi di PyDockWEB sull’elettrostatica e risultavano più facili da allineare senza grandi cambiamenti di forma. Quando i ricercatori hanno ripetuto alcuni casi falliti usando informazioni di contatto “oracle” estratte direttamente dalle strutture sperimentali, la maggior parte di quei casi è migliorata, confermando che la localizzazione accurata della patch di contatto è un ingrediente chiave — ma il docking come corpo rigido ha comunque limiti quando sono necessari ampi adattamenti conformazionali.
Cosa significa per il futuro
In termini pratici, questo lavoro dimostra che fornire a un programma di docking basato sulla fisica un suggerimento intelligente su dove un anticorpo è probabile che afferri il suo bersaglio può migliorare notevolmente la mira, senza trasformare il processo in una scatola nera opaca. La pipeline combinata ParaDeep–PyDockWEB non sostituisce metodi più avanzati flessibili o generativi, ma offre un modo pratico per usare segnali di deep learning a livello di sequenza per guidare strumenti di docking familiari e interpretabili. Man mano che gli sforzi di scoperta e ingegneria degli anticorpi generano librerie di sequenze sempre più grandi, approcci ibridi di questo tipo potrebbero aiutare i ricercatori a filtrare rapidamente candidati strutturalmente coerenti con un bersaglio desiderato, rendendo il percorso dalla sequenza a un anticorpo utilizzabile più rapido e meglio informato.
Citazione: Kodchakorn, K., Udomwong, P., Pamonsupornwichit, T. et al. Integrating deep learning with physics based modeling enables high precision antibody antigen interface prediction. Sci Rep 16, 8134 (2026). https://doi.org/10.1038/s41598-026-39466-8
Parole chiave: docking di anticorpi, deep learning, predizione del paratope, interazioni proteina-proteina, progettazione di anticorpi