Clear Sky Science · it
l'isoforma fln-2 regola in modo specifico la durata della salute di Caenorhabditis elegans influenzando la funzione faringea
Perché gli apparati boccalo-contano per vivere più a lungo
Di solito pensiamo all’invecchiamento come a qualcosa che avviene in profondità nelle nostre cellule, ma questo studio mostra che il modo in cui un animale mastica il cibo — e i microbi che porta con sé — può influenzare anche quanto a lungo resta in buona salute. Usando il piccolo verme tondo Caenorhabditis elegans, un modello classico per la ricerca sull’invecchiamento, gli autori hanno scoperto che versioni specifiche di un singolo gene strutturale possono modulare quanto efficacemente la “bocca” del verme macina i batteri. Una macinazione migliore significa meno infezioni batteriche, un intestino più robusto e infine una vita più lunga e sana, il tutto senza mangiare di meno.
Un gene dalle molte facce
Il lavoro è incentrato su un gene chiamato fln-2, l’omologo del verme della filamina A umana, una proteina che aiuta a dare forma alle cellule e a collegarle all’ambiente circostante. Il gene fln-2 è insolitamente complesso: può produrre fino a 27 forme proteiche leggermente diverse, o isoforme, dallo stesso tratto di DNA. Studi precedenti avevano suggerito che una mutazione naturale in fln-2 potesse estendere la durata di vita del verme riducendo le infezioni letali nell’organo di alimentazione, la faringe. Tuttavia, non era chiaro quali delle molte isoforme fossero importanti e perché la loro perdita potesse talvolta accorciare la vita anziché allungarla.
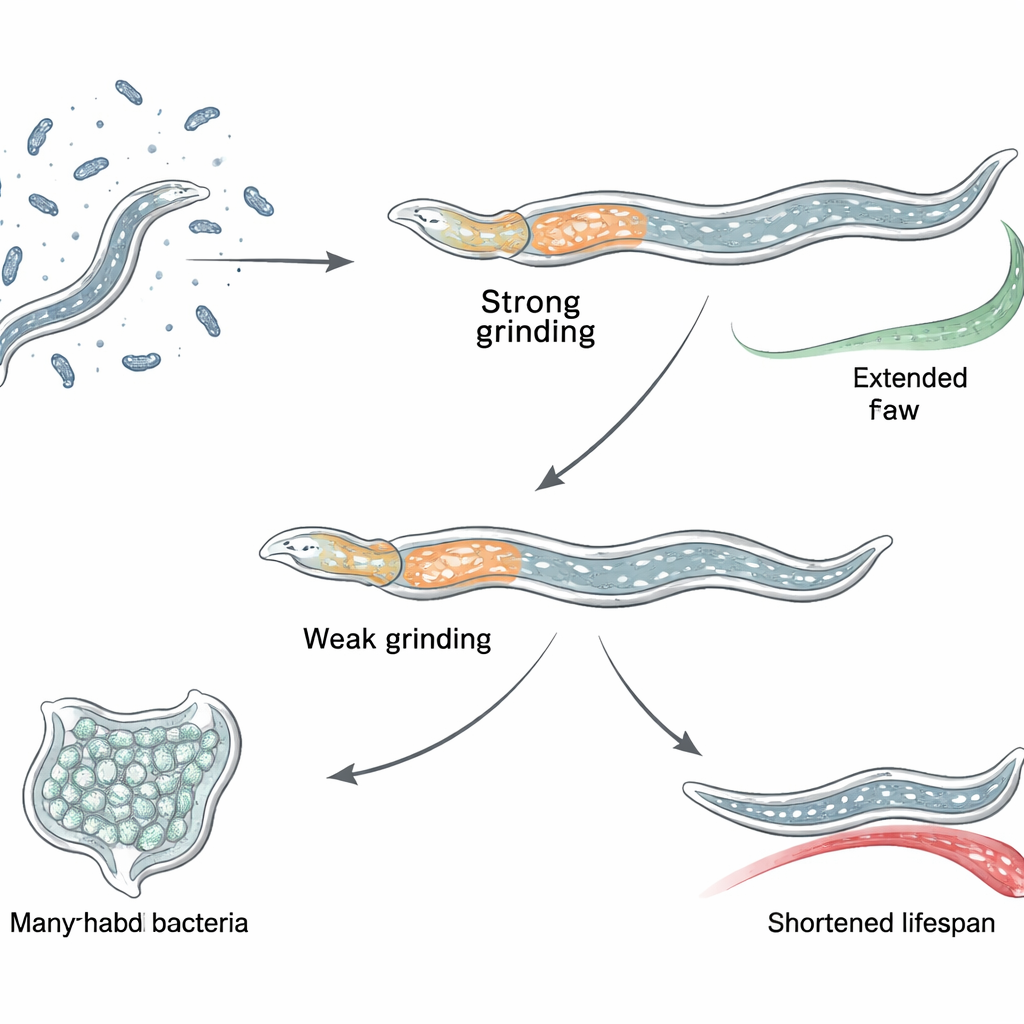
Le isoforme lunghe aiutano, quelle corte fanno male se perse
Usando un editing genomico preciso, i ricercatori hanno creato una serie di ceppi di verme in cui gruppi selezionati di isoforme di fln-2 sono stati disattivati. Hanno osservato uno schema sorprendente: quando sono state interrotte solo le isoforme più lunghe, i vermi vivevano più a lungo e restavano più sani; ma quando tutte le isoforme sono state rimosse, comprese quelle più corte espresse più diffusamente nel corpo, la durata di vita è in realtà diminuita. Le immagini hanno mostrato che le isoforme lunghe sono concentrate lungo la superficie interna della faringe, in particolare in una struttura dentata chiamata grinder. Questa disposizione suggerisce che le diverse isoforme svolgano ruoli opposti: perdere le versioni lunghe, focalizzate sulla faringe, aumenta la sopravvivenza, mentre perdere le isoforme corte e ampiamente usate provoca effetti collaterali dannosi che sovrastano qualsiasi beneficio.
Macinazione più efficace, meno germi, intestini più forti
Il gruppo ha quindi indagato come la perdita delle isoforme lunghe potesse rendere i vermi più robusti. Hanno dimostrato che i vermi privi di queste isoforme macinano il loro cibo batterico in modo più completo, lasciando meno microbi intatti che possano passare nell’intestino. Con l’età, i vermi normali accumulano batteri vivi nell’intestino e possono sviluppare un’infezione diffusa nella faringe, entrambe condizioni che limitano la durata di vita. Al contrario, i mutanti per le isoforme lunghe di fln-2 mostravano un accumulo batterico molto inferiore in entrambe le regioni. La microscopia con batteri fluorescenti e l’ibridazione dell’RNA hanno confermato una colonizzazione sostanzialmente ridotta. Questi vermi mantenevano anche una barriera intestinale più salda, come testato con un colorante che si infiltra nella cavità corporea quando la parete intestinale è danneggiata. Questa protezione dipendeva da un processo interno di riciclo chiamato autofagia: se venivano disattivati geni chiave dell’autofagia, sia l’allungamento della vita sia i benefici sulla barriera scomparivano.
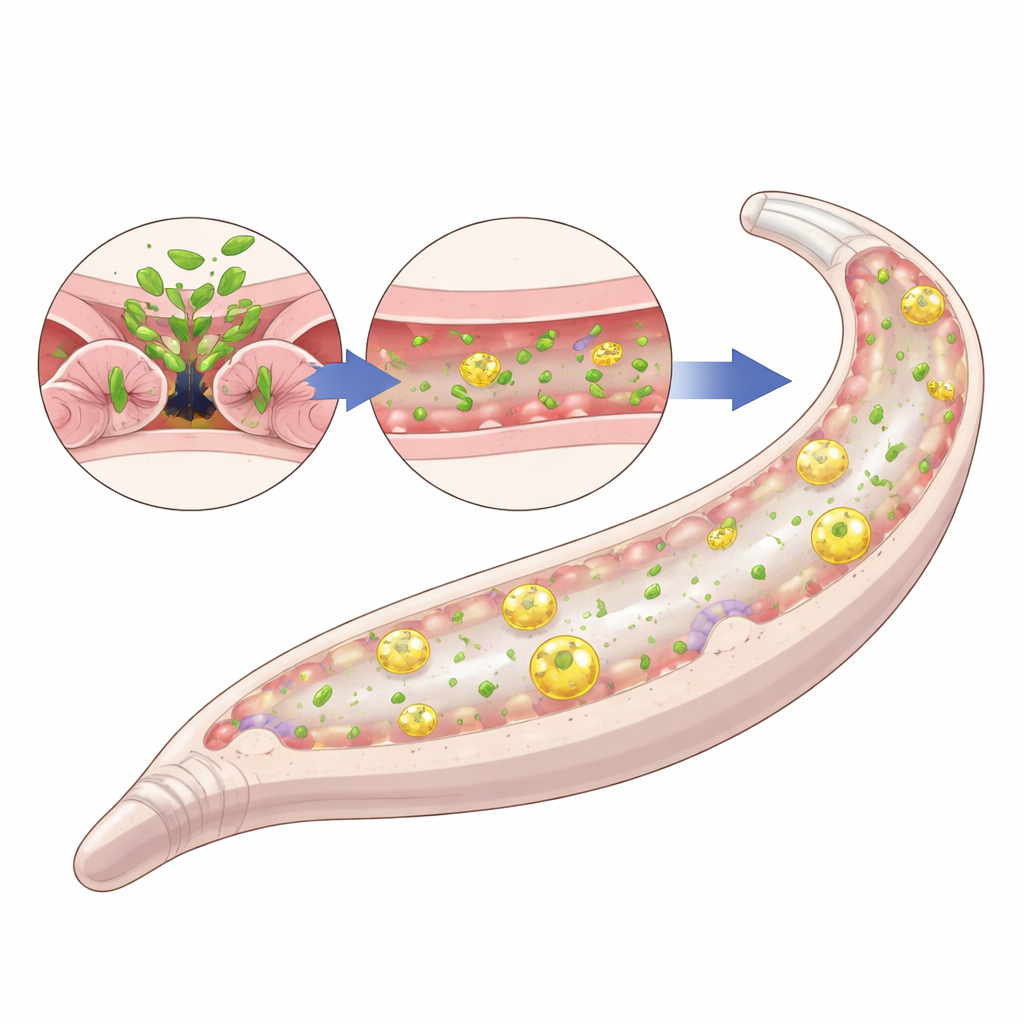
Non solo mangiare meno: il ruolo dei batteri vivi
Molti mutanti di vermi a vita lunga agiscono mangiando meno calorie, ma non era questo il caso. I mutanti fln-2 pompavano il cibo attraverso la faringe a ritmi normali e consumavano quantità di batteri simili ai vermi standard. Test genetici hanno mostrato che la loro longevità non dipendeva nemmeno da note vie ormonali legate all’invecchiamento. Invece, i benefici svanivano quando i vermi venivano nutriti con batteri uccisi dal calore. Senza microbi vivi in grado di infettarli, i mutanti fln-2 non vivevano più a lungo dei vermi normali, anche se entrambi i gruppi mostravano alti livelli di autofagia. Ciò indica che il vantaggio chiave della perdita delle isoforme lunghe è dipendente dal contesto: è utile solo quando i vermi devono affrontare la sfida costante di batteri vivi e replicanti.
Cosa significa per invecchiamento e infezione
In termini semplici, questo studio rivela una lotta interna in un solo gene tra diverse versioni proteiche. Rimuovere le isoforme lunghe affina le parti boccalo-faringee del verme in modo che schiaccino i batteri più efficacemente, riducendo la pressione infettiva e attivando una pulizia protettiva all’interno delle cellule intestinali. Ma rimuovere ogni versione del gene destabilizza tessuti vitali e accorcia la vita. Nel complesso, i risultati sottolineano come l’invecchiamento possa essere guidato non solo da interruttori molecolari profondi ma anche dal disegno fisico degli organi che interagiscono con i microbi. Pur essendo i vermi molto diversi dagli umani, il lavoro suggerisce che cambiamenti sottili nelle proteine strutturali correlate alla filamina A — e nel modo in cui i nostri corpi gestiscono il flusso continuo di microbi attraverso il tratto digestivo — potrebbero svolgere un ruolo più ampio nel determinare quanto a lungo e quanto bene viviamo.
Citazione: Chang, YH., Chi, AQ., Ren, YC. et al. fln-2 isoform-specifically regulates Caenorhabditis elegans health span by affecting pharyngeal function. Sci Rep 16, 8363 (2026). https://doi.org/10.1038/s41598-026-39461-z
Parole chiave: invecchiamento, C. elegans, microbiota intestinale, autofagia, funzione faringea