Clear Sky Science · it
Impatto della chemioterapia neoadiuvante sulla funzionalità delle cellule stromali mesenchimali derivate dal tessuto adiposo e sui loro effetti modulatori sui fibroblasti in pazienti oncologici
Perché questo è importante per i sopravvissuti al cancro
Molte persone che ricevono trattamenti oncologici affrontano in seguito ferite che guariscono lentamente e complicazioni post-operatorie. Allo stesso tempo, i medici stanno esplorando sempre più l’uso delle cellule riparatrici derivate dal grasso del paziente per favorire il recupero dei tessuti. Questo studio pone una domanda pratica e urgente: dopo la chemioterapia, quelle cellule riparatrici sono ancora sufficientemente valide per essere utilizzate e, in caso contrario, quali cellule sono maggiormente compromesse?
Gli aiutanti nascosti del corpo
Il tessuto adiposo è più di una riserva di energia. Ospita una popolazione ricca di cellule riparatrici polivalenti chiamate cellule stromali mesenchimali derivate dal tessuto adiposo, o AD-MSC. Queste cellule non sono passive: rilasciano un cocktail di segnali molecolari che possono attenuare l’infiammazione, stimolare la formazione di nuovi vasi e incoraggiare le cellule vicine a proliferare e ricostruire il tessuto danneggiato. Appena sopra il tessuto adiposo, nella pelle, vivono i fibroblasti—cellule operative che migrano nelle ferite e depositano collagene, la proteina che costituisce l’impalcatura che conferisce forza al tessuto nuovo. Insieme, AD-MSC e fibroblasti contribuiscono a determinare quanto bene la pelle si riprende dopo un danno o un intervento chirurgico.
Testare le cellule riparatrici del grasso prima e dopo il trattamento
I ricercatori hanno raccolto piccoli campioni di pelle e grasso da 66 pazienti sottoposti a intervento chirurgico, alcuni dei quali avevano ricevuto chemioterapia in precedenza e altri no. Dal tessuto adiposo hanno isolato le AD-MSC e confermato che queste cellule mantenevano le caratteristiche tipiche delle cellule riparatrici: esibivano i marcatori di superficie attesi e potevano differenziarsi in cellule simili a osso, cartilagine e tessuto adiposo in coltura. Dalla pelle hanno isolato i fibroblasti. Il gruppo ha quindi confrontato come AD-MSC e fibroblasti provenienti da pazienti esposti o non esposti alla chemioterapia crescessero, si dividessero, rilasciassero molecole segnale ed esprimessero geni correlati alla guarigione delle ferite e alla rigenerazione.
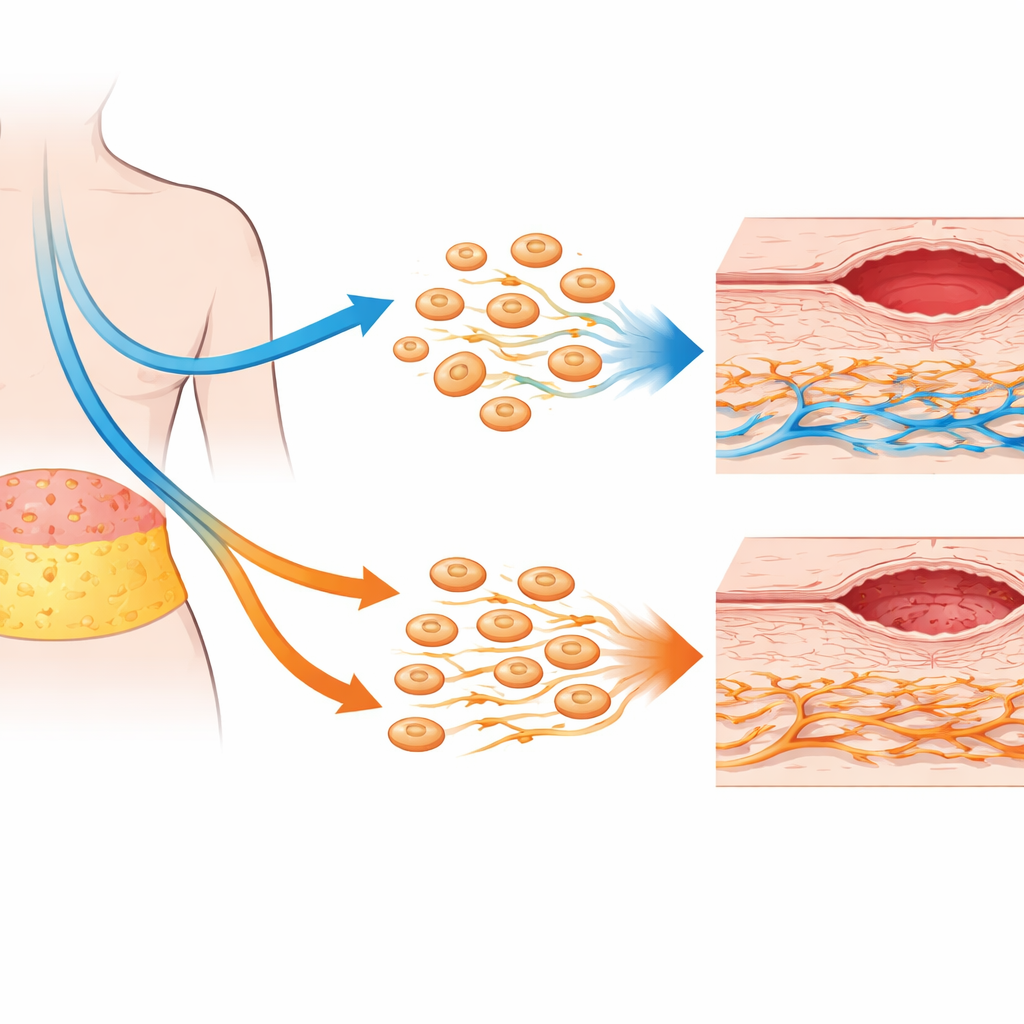
Le cellule riparatrici del grasso restano sorprendentemente robuste
Contrariamente ai timori che la chemioterapia potesse indebolire le AD-MSC, lo studio ha rilevato che queste cellule derivate dal grasso sono risultate notevolmente resilienti. I loro marcatori identitari di base, il modello di crescita e il profilo delle proteine segnale secrete sono risultati in gran parte invariati dopo la chemioterapia. L’attività genica legata alla crescita, all’auto-rinnovamento e alla riparazione delle ferite ha mostrato solo piccole variazioni non significative. In realtà, le AD-MSC provenienti da pazienti trattati con chemioterapia hanno mostrato un’attività mitocondriale leggermente maggiore, suggerendo un metabolismo più attivo piuttosto che un danno. Negli esperimenti in co-coltura—dove AD-MSC e fibroblasti condividevano lo stesso mezzo senza contatto diretto—le AD-MSC hanno comunque potenziato alcuni comportamenti dei fibroblasti, come la migrazione direzionale verso segnali di riparazione, soprattutto nei campioni di pazienti non sottoposti a chemioterapia.
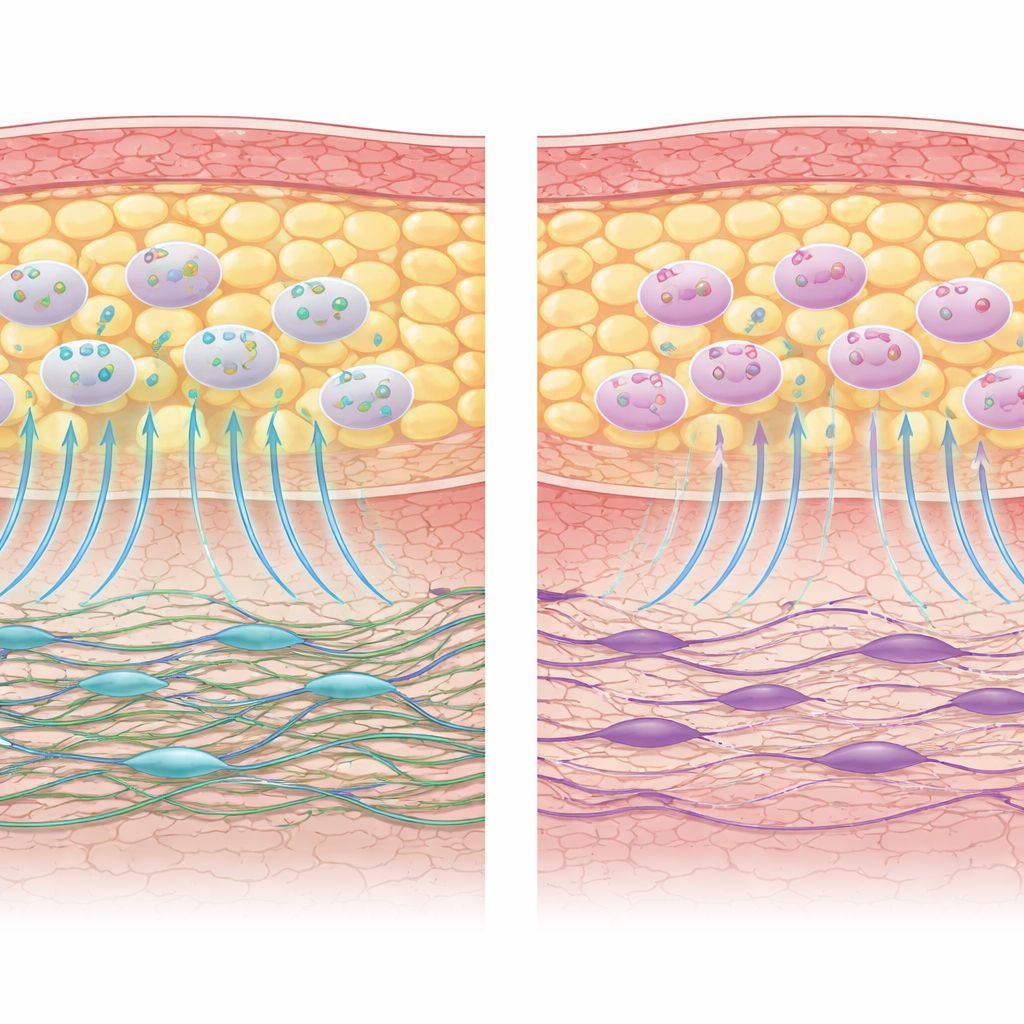
I costruttori della pelle subiscono il peso della chemioterapia
Il quadro è risultato molto diverso per i fibroblasti. Le cellule prelevate dalla pelle di pazienti trattati con chemioterapia hanno mostrato segni chiari di ridotta vitalità biologica. La loro capacità di migrare in una “ferita” simulata su piastra di coltura era significativamente compromessa e la produzione di collagene tendeva a essere inferiore. Il profilo delle molecole segnale rilasciate si è spostato verso un assetto più infiammatorio e meno rigenerativo, e molti geni associati ai segnali di crescita, ai loro recettori e al potenziale rigenerativo risultavano attenuati. Anche quando questi fibroblasti venivano co-coltivati con le proprie AD-MSC, la maggior parte delle loro funzioni—migrazione, produzione di collagene e attività genica benefica—rimaneva ridotta rispetto ai fibroblasti di pazienti non sottoposti a chemioterapia.
Cosa significa per le terapie future della guarigione
In termini semplici, il messaggio di questo lavoro è che la chemioterapia non sembra distruggere la riserva di cellule riparatrici di origine adiposa dell’organismo, ma indebolisce i costruttori di prima linea della pelle—i fibroblasti—rendendoli meno capaci di intervenire rapidamente nelle ferite e ricostruire un tessuto solido. Poiché le AD-MSC restano funzionalmente intatte, rimangono candidate promettenti per l’impiego in procedure ricostruttive, cura delle ferite e innesti di grasso dopo il trattamento oncologico. Tuttavia, lo stato compromesso dei fibroblasti potrebbe limitare il beneficio che queste cellule simili a staminali possono fornire da sole. Gli autori suggeriscono che le terapie future dovranno probabilmente sostenere entrambe le componenti della partnership riparativa: preservare o ristabilire la salute dei fibroblasti mentre si sfruttano AD-MSC robuste, idealmente in modelli più complessi e simili al corpo che catturino meglio l’ambiente reale della guarigione nei sopravvissuti al cancro.
Citazione: Skoniecka, A., Słonimska, P., Tymińska, A. et al. Impact of neoadjuvant chemotherapy on the functionality of adipose-derived mesenchymal stromal cells and their modulatory effects on fibroblasts in oncology patients. Sci Rep 16, 8614 (2026). https://doi.org/10.1038/s41598-026-39457-9
Parole chiave: chemioterapia, guarigione delle ferite, cellule staminali derivate dal grasso, fibroblasti, medicina rigenerativa