Clear Sky Science · it
Ruolo della microscopia a forza atomica nella caratterizzazione di sfere tumorali eterotipiche e della loro interazione con particelle di microplastica
Perché la consistenza dei tessuti tumorali conta
Il cancro viene solitamente descritto in termini di geni e cellule anomale, ma anche la sua sensazione fisica — quanto il tessuto è morbido o rigido — influenza il modo in cui un tumore cresce e risponde all’ambiente circostante. Questo studio esamina piccoli ammassi tridimensionali di cellule di cancro polmonare, chiamati sfere, e pone due domande pratiche: possiamo usare un microscopio a contatto ad alta risoluzione per misurare in modo affidabile la rigidità di questi mini‑tumori, e tale rigidità influenza il loro comportamento di interazione con particelle di microplastica trasportate dall’aria che possono raggiungere i polmoni?
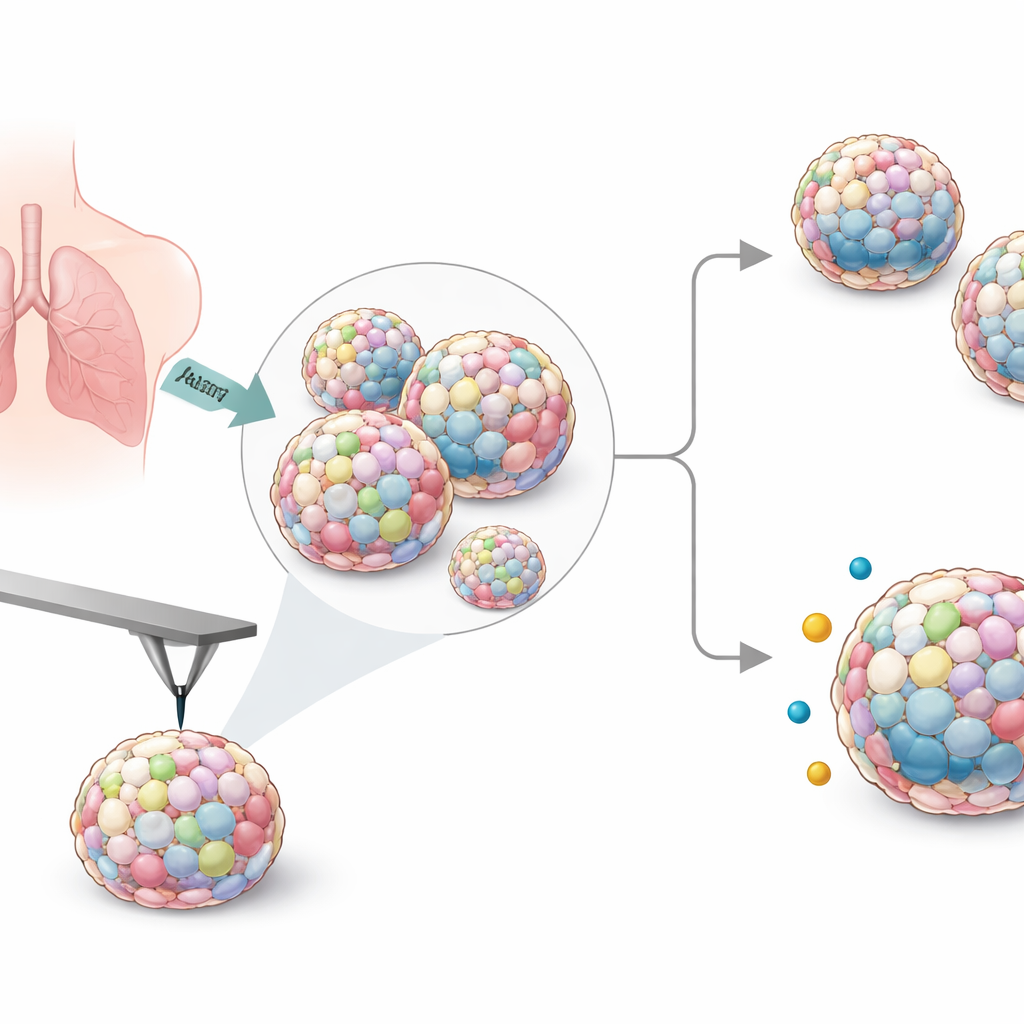
Costruire mini tumori polmonari in laboratorio
Per imitare la composizione complessa dei tumori reali, i ricercatori hanno coltivato sfere miste a partire da sei linee cellulari umane di cancro polmonare insieme a cellule di supporto chiamate fibroblasti, e talvolta con macrofagi di tipo immune. Hanno testato diversi metodi per formare questi aggregati e hanno scelto piastre a bassa adesione che producevano in modo affidabile sfere rotonde e stabili, sufficientemente grandi da essere maneggiate. Regolando il numero e le proporzioni di cellule, hanno creato sfere sia piccole sia più grandi, quindi hanno adottato una ricetta standard che funzionasse in modo coerente per tutti i tipi cellulari tumorali.
Sbirciare all’interno e verificare lo stato delle cellule
Una volta formate le sfere, il gruppo ha esaminato la loro struttura interna e il comportamento cellulare usando varie colorazioni e metodi di sezione. Le fette sottili hanno mostrato che alcune combinazioni di cellule tumorali formavano sfere molto compatte, mentre altre erano più lasse con spazi più aperti. I fibroblasti tendevano a localizzarsi verso il centro, specialmente nella maggior parte delle combinazioni cellulari, mentre le cellule tumorali si concentravano più verso l’esterno. Colorazioni per cellule vive e morte hanno rivelato un pattern familiare nei tumori reali: cellule vitali ben nutrite al margine e cellule più danneggiate o morenti nel nucleo povero di ossigeno. Un test con marcatura del DNA per la divisione cellulare ha mostrato che, per la maggior parte delle sfere, le cellule in tutta la struttura erano ancora in grado di proliferare, sebbene una linea cellulare tumorale (Calu‑3) si dividesse principalmente al bordo esterno.
Misurare la rigidità con una sonda su scala nanometrica
Per tradurre la consistenza in numeri, gli scienziati hanno utilizzato la microscopia a forza atomica, in cui una piccola punta affilata preme delicatamente sulla superficie della sfera e registra quanto si deforma. Da questi dati hanno calcolato il modulo di Young, una misura standard della rigidità. Pur essendo simili per dimensioni, le sfere variavano notevolmente in rigidità a seconda della linea di cancro polmonare presente. Le sfere con cellule A549 erano tra le più morbide, mentre quelle contenenti cellule H23 o HCC827 risultavano chiaramente più rigide. L’aggiunta di macrofagi ha generalmente aumentato la rigidità per diversi tipi tumorali. Quando il gruppo ha confrontato questi valori con la rapidità di crescita delle cellule tumorali originali in coltura piana, ha scoperto che le cellule a divisione più lenta tendevano a formare sfere più rigide, collegando il comportamento di crescita alle proprietà meccaniche.
Testare il contatto con le microplastiche
Poiché frammenti di plastica microscopici sono stati rilevati nei tumori polmonari, i ricercatori hanno esposto le loro sfere a particelle fluorescenti di polistirene di circa un micrometro di diametro, a concentrazioni simili a quelle misurate nel sangue umano. In condizioni statiche, le particelle si aggregavano e si attaccavano in modo disomogeneo a un lato delle sfere, così il gruppo ha optato per un lieve movimento oscillatorio dei campioni per meglio imitare i fluidi corporei in movimento. In queste condizioni dinamiche, solo poche particelle individuali si sono attaccate o sono penetrate negli strati cellulari esterni, troppo poche per un conteggio preciso. Perciò il team è tornato alle misurazioni della rigidità. Dopo l’esposizione, molti tipi di sfere sono diventati leggermente più rigidi, coerente con perline di plastica rigide che si attaccano o si incastrano sulla superficie, ma questa variazione non ha mostrato una dipendenza chiara e semplice dalla rigidità iniziale della sfera.
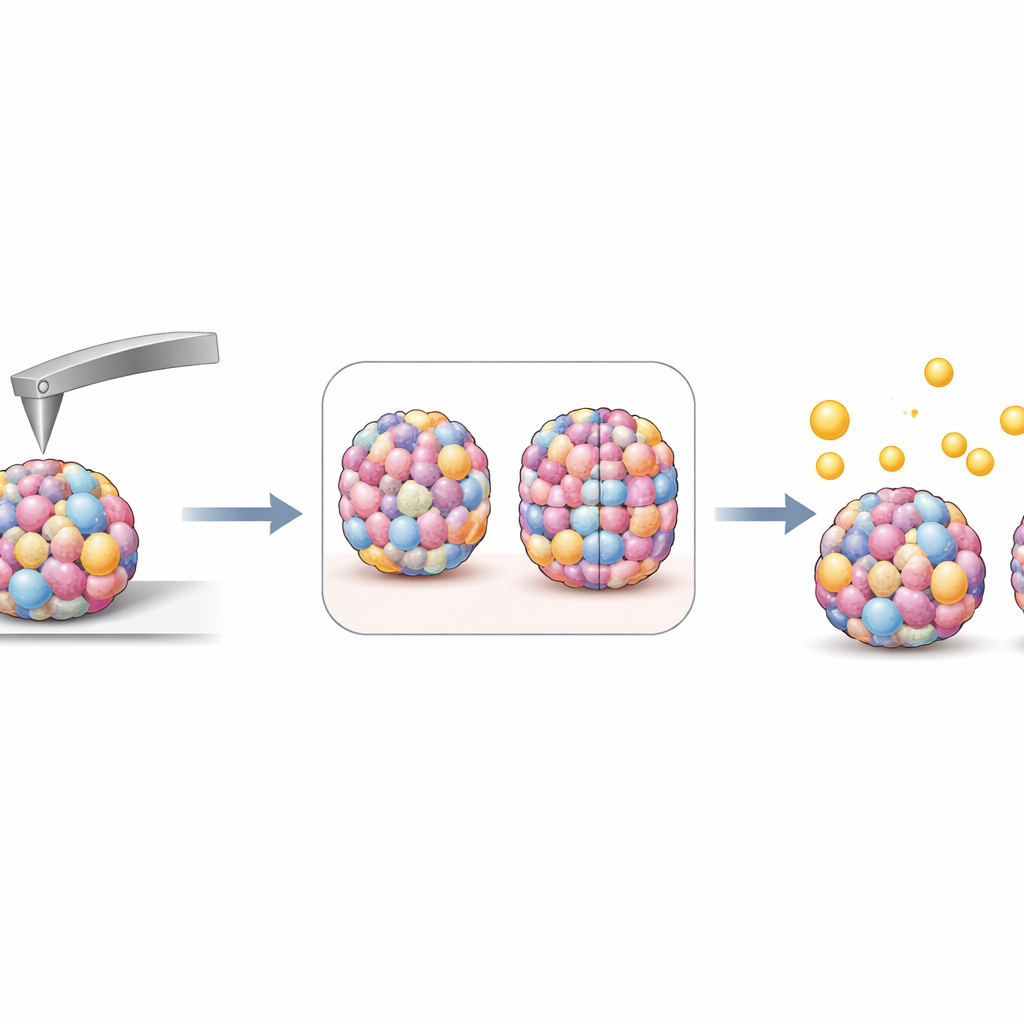
Cosa significa per futuri studi su cancro e inquinamento
Il lavoro dimostra che la rigidità è un parametro informativo in più per descrivere modelli tumorali tridimensionali che altrimenti appaiono simili per dimensioni e forma. Il modo in cui le cellule si dispongono all’interno della sfera e la velocità con cui si dividono spiegano solo in parte queste differenze meccaniche, suggerendo che la rigidità cattura aspetti nascosti della biologia tumorale. Sebbene questo studio non abbia trovato una regola semplice che leghi la rigidità delle sfere all’assorbimento di microplastiche a livelli realistici, evidenzia che in condizioni lievi e in movimento solo un numero ridotto di tali particelle è probabile che aderisca a tessuti simili a tumori. A lungo termine, combinare misurazioni dettagliate di rigidità con metodi più sensibili di tracciamento delle particelle potrebbe aiutare i ricercatori a prevedere meglio come i tumori rispondono sia ai farmaci antitumorali sia agli inquinanti ambientali che raggiungono i polmoni.
Citazione: Kolesnik, T., Öhlinger, K., Absenger-Novak, M. et al. Role of atomic force microscopy in characterization of heterotypic cancer spheroids and their interaction with microplastic particles. Sci Rep 16, 8303 (2026). https://doi.org/10.1038/s41598-026-39445-z
Parole chiave: sfere di cancro polmonare, microscopia a forza atomica, rigidità cellulare, microplastiche, microambiente tumorale