Clear Sky Science · it
Valutazione completa delle prestazioni del BMIA-12A: un sistema per la quantificazione delle cellule del midollo osseo in campioni normali e con neoplasie ematologiche
Perché contare le cellule del midollo osseo è importante
Quando i medici diagnosticano tumori del sangue come la leucemia o il mieloma multiplo, osservano attentamente gli strisci di midollo osseo al microscopio e contano migliaia di cellule a mano. Questo lavoro lento e laborioso influenza decisioni che cambiano la vita riguardo a diagnosi, trattamento e prognosi. L’articolo presenta e testa in modo rigoroso un nuovo sistema basato sull’intelligenza artificiale, BMIA-12A, progettato per automatizzare gran parte di questa conta—potenzialmente rendendo i risultati più rapidi, coerenti e meno dipendenti dall’esperto che interpreta il vetrino.
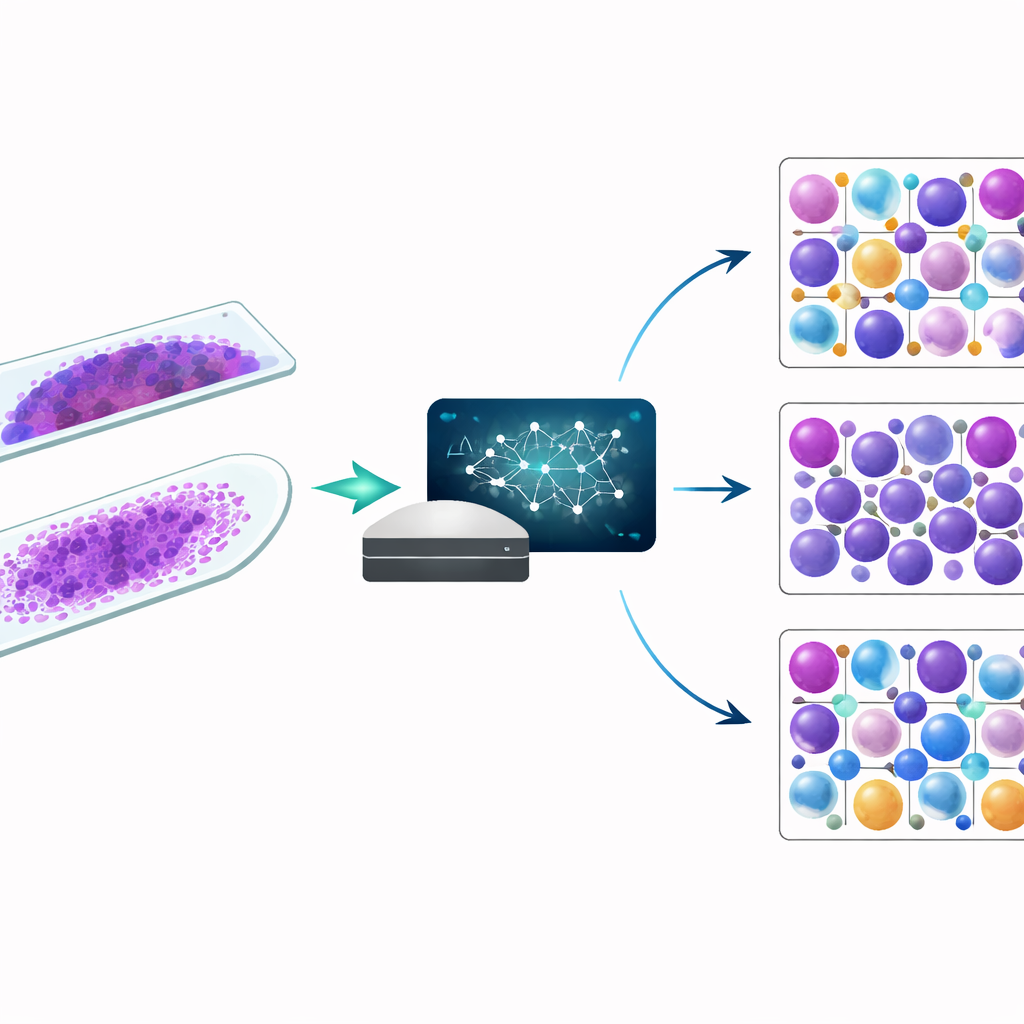
Un nuovo aiuto digitale per il microscopio
Il sistema BMIA-12A acquisisce immagini digitali degli strisci di midollo osseo e utilizza algoritmi di deep learning per riconoscere e categorizzare le cellule in 16 tipi principali, includendo i primi “blasti” che aiutano a definire le leucemie e le plasmacellule, centrali nel mieloma multiplo. In questo studio i ricercatori hanno analizzato 298 strisci di midollo osseo provenienti da 149 persone, comprendendo campioni normali, disordini delle plasmacellule e diverse forme di leucemia acuta. Per ciascuno striscio hanno confrontato tre approcci: conteggi completamente automatizzati con l’IA, conteggi IA revisionati e corretti da specialisti e conteggi manuali tradizionali con il microscopio ottico. Hanno inoltre esaminato due tecniche comuni di preparazione del vetrino, dette strisci a cuneo (wedge) e a schiacciamento (squash), per vedere come la qualità del vetrino influenzi le prestazioni dell’IA.
Quanto bene il sistema riconosce le cellule normali
Nel midollo di persone senza neoplasia, il sistema IA ha dato prestazioni impressionanti. Ha classificato correttamente circa il 95% di quasi 38.000 cellule sia nelle preparazioni a cuneo sia in quelle a schiacciamento, con 14 dei 16 tipi cellulari che hanno mostrato recall superiore al 90%. I vetrini a cuneo—dove il campione è distribuito uniformemente sul vetro—hanno fornito una precisione leggermente migliore per le cellule diagnostiche chiave come plasmacellule, blasti e rari basofili. La maggior parte degli errori dell’IA si è verificata tra tipi cellulari dall’aspetto molto simile, come stadi contigui della maturazione dei globuli bianchi o linfociti reattivi che somigliano ai blasti. Quando i ricercatori hanno confrontato la frequenza con cui ciascun tipo cellulare appariva attraverso campioni interi, i risultati dell’IA e quelli revisionati dagli esperti sono risultati molto simili, mentre i conteggi manuali tradizionali sono risultati visibilmente più variabili, riflettendo la soggettività e il campionamento limitato della conta umana.
Cosa succede nel mieloma e nella leucemia
Le prestazioni del sistema negli stati morbosi sono state più eterogenee. Nei disordini delle plasmacellule l’IA è stata molto precisa nell’identificare le plasmacellule ma ne ha mancato circa un quarto, soprattutto nel mieloma multiplo dove il midollo è saturo di plasmacellule anomale che differiscono nella forma dagli esempi tipici usati per l’addestramento. Di conseguenza, l’IA tendeva a sottostimare la percentuale di plasmacellule rispetto ai conteggi manuali e a quelli digitali corretti dagli esperti, in particolare quando il carico tumorale era elevato. Un pattern simile è emerso nelle leucemie acute: l’IA individuava abbastanza bene i blasti complessivamente, specialmente sui vetrini a cuneo, ma spesso assegnava blasti atipici a categorie somiglianti come monociti o cellule mieloidi precoci. I conteggi manuali hanno sistematicamente riportato percentuali di blasti più alte rispetto sia ai risultati automatizzati sia a quelli digitali revisionati dagli esperti, con i divari maggiori osservati in alcuni sottotipi genetici come AML con mutazione di NPM1 e ALL B-cellulare con la fusione BCR::ABL1, in cui la morfologia dei blasti è particolarmente insolita.
Perché la preparazione del vetrino e la genetica contano
Lo studio ha mostrato che sia il modo in cui lo striscio è preparato sia la genetica sottostante della malattia modellano le prestazioni dell’IA. Gli strisci a schiacciamento, in cui frammenti di midollo vengono compressi tra vetrini, introducono distorsioni che sfocano dettagli nucleari fini, aumentando la confusione tra stadi di maturazione adiacenti e tra blasti e altre cellule giovani. Gli strisci a cuneo preservano meglio la struttura, offrendo recall e precisione più elevati; perciò gli autori li raccomandano come formato standard per l’analisi assistita da IA. Sul versante biologico, i blasti di specifici sottotipi genetici spesso presentano forme nucleari distintive, talvolta deformate, o altre caratteristiche atipiche. Poiché i sistemi IA attuali sono generalmente addestrati principalmente su cellule normali, queste varianti neoplastiche possono essere costrette nella categoria normale “più vicina”, portando a una sottostima sistematica del carico di malattia proprio nei pazienti per i quali soglie accurate sono più critiche.
Come cambia il laboratorio oggi
Nel complesso, i risultati suggeriscono che BMIA-12A è già sufficientemente affidabile da fungere da potente strumento di screening e triage, soprattutto per campioni di midollo normali e conteggi differenziali di routine. Può esaminare rapidamente decine di migliaia di cellule per vetrino e fornisce risultati stabili e riproducibili che si allineano bene con la revisione degli esperti. Tuttavia, le discrepanze chiare e talvolta ampie con i conteggi manuali nelle leucemie e nei tumori delle plasmacellule indicano che gli specialisti umani restano essenziali per l’interpretazione finale, soprattutto vicino ai cutoff diagnostici e nei sottotipi ad alto rischio definiti geneticamente. Gli autori sostengono che i laboratori che adottano tali strumenti IA devono validarli con cura per i propri metodi di preparazione dei vetrini e costruire flussi di lavoro in cui l’IA fornisce una baseline obiettiva che gli esperti affinano, piuttosto che sostituire il giudizio specialistico.
Citazione: Kim, H.N., Lee, J.H., Jung, Y. et al. Comprehensive performance assessment of the BMIA-12 a system for bone marrow cell quantification in normal and hematological malignancy samples. Sci Rep 16, 8798 (2026). https://doi.org/10.1038/s41598-026-39443-1
Parole chiave: intelligenza artificiale in ematologia, citologia del midollo osseo, diagnosi di leucemia, mieloma multiplo, microscopia digitale