Clear Sky Science · it
Scoperta di potenziali composti antivirali e accelerazione della scoperta terapeutica contro il virus del vaiolo delle scimmie
Perché questa ricerca è importante ora
Il vaiolo delle scimmie, oggi spesso chiamato mpox, è passato dall'essere un'infezione tropicale rara a una preoccupazione globale, con focolai segnalati in diversi continenti negli ultimi anni. Diversamente dalla COVID-19, non esiste ancora un farmaco progettato specificamente per bloccare questo virus. Questo studio utilizza strumenti informatici avanzati per cercare nuove piccole molecole che possano neutralizzare il virus nel suo punto più critico: la capacità di nascondersi dal nostro sistema immunitario. Se confermati in laboratorio, questi composti candidati potrebbero diventare il punto di partenza per una nuova classe di antivirali.
Come il virus si nasconde dalle nostre difese
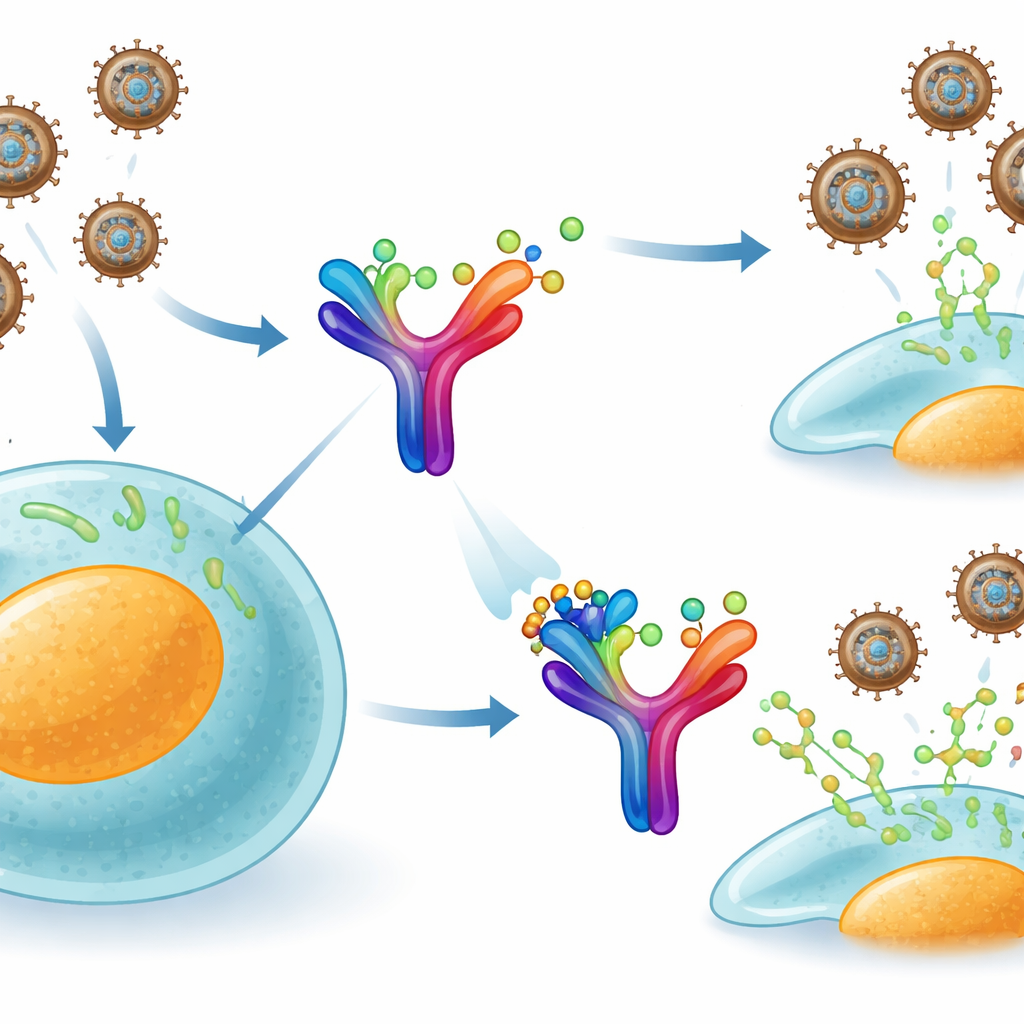
Il vaiolo delle scimmie appartiene alla stessa famiglia più ampia del vaiolo e sfrutta un trucco ingegnoso per eludere il sistema immunitario. Le nostre cellule rilasciano una proteina di segnalazione chiamata interferone-gamma, che normalmente avverte le cellule vicine e attiva difese antivirali. Il virus, però, produce una propria proteina secreta, chiamata B8R, che galleggia al di fuori delle cellule infette. B8R imita da vicino il nostro recettore per l'interferone-gamma e cattura questi segnali immunitari prima che raggiungano il loro vero bersaglio. Di fatto agisce come una spugna, assorbendo i messaggi di allarme dell'organismo e impedendo una risposta antivirale completa.
Usare i computer per progettare terapie più intelligenti
La scoperta tradizionale di farmaci può richiedere molti anni e risorse enormi. Qui, i ricercatori ricorrono alla progettazione di farmaci assistita dal computer per accelerare il processo. Poiché non esiste una struttura 3D sperimentale della proteina B8R, hanno prima utilizzato strumenti basati su AlphaFold per prevederne la forma atomica e hanno verificato attentamente la qualità di quel modello. Con una struttura 3D affidabile a disposizione, hanno effettuato uno screening virtuale di una libreria chimica di 5000 piccole molecole. Regole che descrivono ciò che di solito rende un farmaco simile a una pillola (come dimensione, forma e solubilità) sono state usate per filtrare i candidati scadenti, lasciando 2890 composti promettenti per test dettagliati contro il modello della proteina B8R.
Trovare una promettente “chiave” chimica
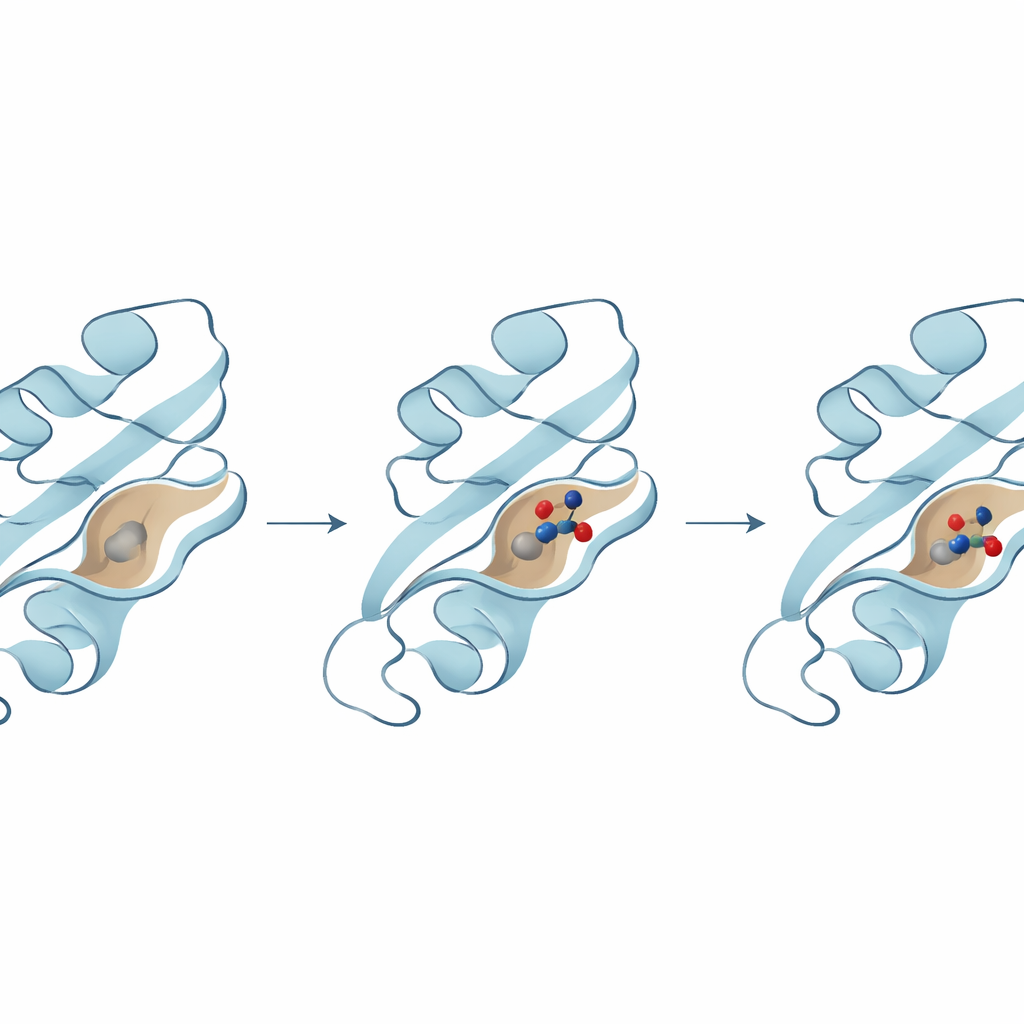
Il passo successivo è stato vedere quali molecole potessero adattarsi perfettamente in una tasca importante sulla superficie di B8R, dove normalmente interagirebbe con l'interferone-gamma. Il team ha utilizzato il docking molecolare, una tecnica che prova miliardi di possibili pose per una molecola nella tasca della proteina e valuta quanto strettamente essa si legherebbe. Sono emersi tre candidati principali, ciascuno previsto formare interazioni forti con amminoacidi chiave nella tasca. Un composto in particolare ha mostrato l'energia di legame più elevata e ha stabilito diversi contatti stabilizzanti con residui critici che ne aiutano l'ancoraggio, suggerendo che potrebbe essere particolarmente efficace nel bloccare l'attività di B8R.
Osservare il movimento delle molecole nel tempo
Proteine e molecole farmacologiche non sono rigide; si muovono, si flettono e "respirano" in un ambiente acquoso. Per cogliere questo comportamento, i ricercatori hanno eseguito lunghe simulazioni di dinamica molecolare — filmati virtuali della durata di centinaia di nanosecondi — per vedere come ogni coppia proteina‑composto si comportasse nel tempo. Queste simulazioni hanno rivelato che il composto con le migliori prestazioni rimaneva profondamente sepolto nella tasca di B8R, con la proteina che si adattava lievemente attorno ad esso pur mantenendo stabilità strutturale. Al contrario, gli altri due composti si muovevano di più, si spostavano in tasche alternative o mostravano fluttuazioni maggiori, suggerendo un legame più debole o meno affidabile. Analisi aggiuntive di flessibilità, energia e movimenti su larga scala hanno tutte indicato lo stesso vincitore: un composto che ha costantemente prodotto il complesso più stabile ed energeticamente favorevole.
Cosa potrebbe significare per le terapie future
Lo studio non sostiene di aver scoperto un farmaco pronto e non sono stati ancora svolti esperimenti su cellule o animali. Invece, propone un solido punto di partenza basato sui dati: una specifica piccola molecola che appare idealmente sagomata per incastrarsi nella proteina B8R del vaiolo delle scimmie e potenzialmente ripristinare il sistema di allarme dell'interferone dell'organismo. Puntando alla strategia di evasione immunitaria del virus anziché alla sua macchina di replicazione, questo approccio offre una nuova prospettiva per la terapia antivirale. Gli autori sostengono che il loro composto guida dovrebbe essere ora testato in laboratorio, dove la sua capacità di bloccare B8R e limitare l'infezione da mpox può essere misurata direttamente. Se quei test avranno successo, ciò potrebbe aprire la strada a una terapia mirata che aiuti il sistema immunitario a vedere e fermare il virus in modo più efficace.
Citazione: Ahmad, F., Navid, A., Irfan, M. et al. Discovery of potential antiviral compounds and accelerating the therapeutic discovery against monkeypox virus. Sci Rep 16, 8306 (2026). https://doi.org/10.1038/s41598-026-39427-1
Parole chiave: antivirale vaiolo delle scimmie, evasione immunitaria, scoperta di farmaci, modellazione computazionale, segnalazione dell'interferone