Clear Sky Science · it
Ottimizzazione dei monociti THP-1-CAR utilizzando la fagocitosi mediata dal segnalamento CD32a per l'attivazione antigenica dei linfociti T
Insegnare nuovi trucchi al sistema immunitario
Le terapie cellulari moderne già riprogrammano le cellule immunitarie per andare alla ricerca del cancro, ma la maggior parte si basa sui linfociti T, che possono incontrare difficoltà nell’ambiente ostile dei tumori solidi. Questo studio si rivolge invece a un altro difensore potente—i macrofagi, i “mangiatori” professionisti del corpo—e indaga come riorientarli in modo che non solo inglobino più efficacemente cellule o virus dannosi, ma richiamino anche i linfociti T per un attacco più duraturo e mirato. Il lavoro rivela regole di progettazione per costruire CAR (recettori chimerici per l’antigene) nei macrofagi che potrebbero essere applicate sia alle infezioni come il COVID-19 sia ai tumori solidi difficili da trattare.
Perché i super-mangiatori contano
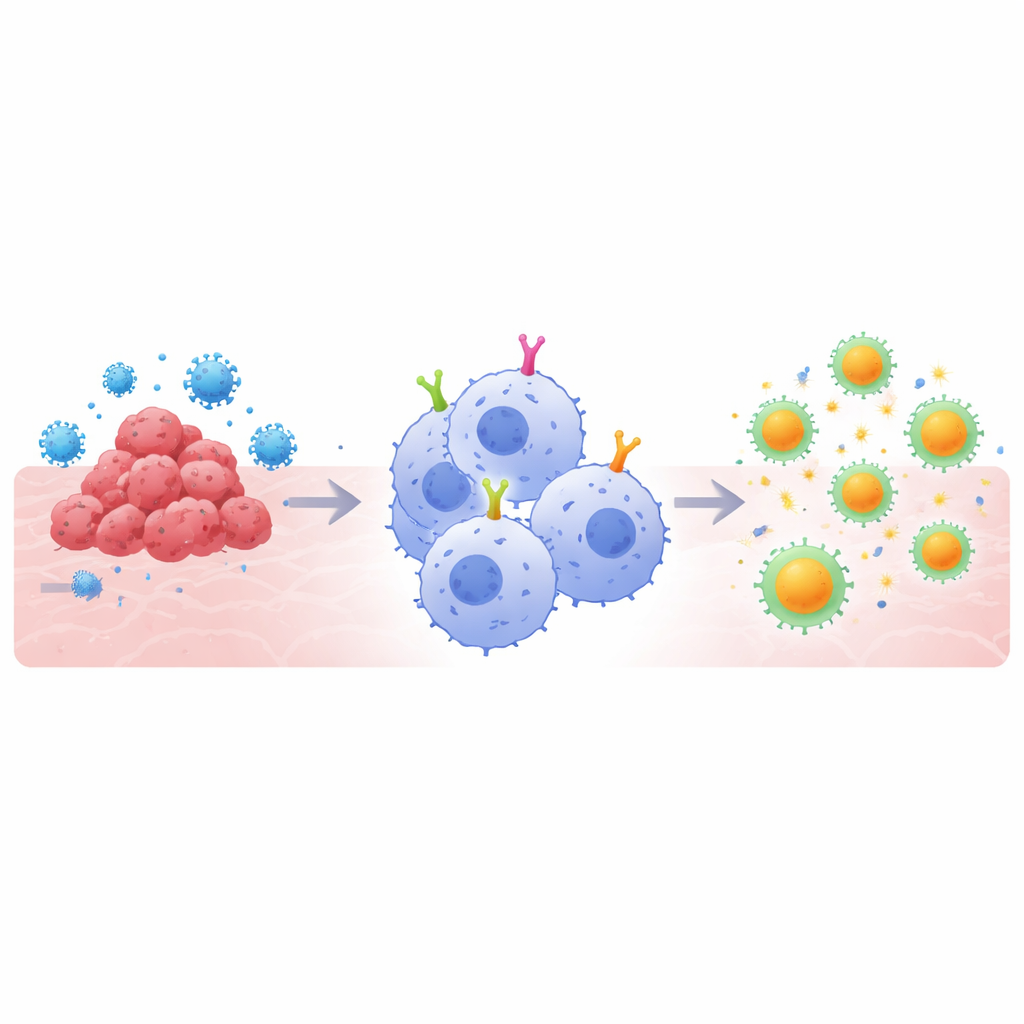
Le terapie basate sui CAR funzionano dotando le cellule immunitarie di recettori di superficie su misura che riconoscono un bersaglio scelto, come una proteina tumorale o una spike virale. Le versioni su linfociti T hanno trasformato il trattamento di alcuni tumori del sangue, ma affrontano ostacoli contro i tumori solidi e in alcune infezioni. I macrofagi offrono un approccio diverso: inglobano naturalmente le minacce e le frammentano in pezzi che possono essere presentati ai linfociti T, fungendo da ponte tra i rami “innato” e “adattativo” dell’immunità. Tuttavia, la maggior parte dei disegni CAR è stata originariamente sviluppata per i linfociti T, non per i macrofagi. Gli autori hanno ipotizzato che per sfruttare pienamente i punti di forza dei macrofagi, le parti intracellulari di segnalazione dei CAR—i segmenti che dicono alla cellula cosa fare una volta che il bersaglio è legato—dovessero essere adattate specificamente a queste cellule “mangianti”.
Trovare il miglior cablaggio interno
Il team ha confrontato sistematicamente diversi domini di segnalazione intracellulari all’interno di CAR introdotti in una linea cellulare monocitaria umana (THP‑1) che può essere indotta a differenziarsi in macrofagi. Si sono concentrati su domini tratti da recettori che normalmente guidano fagocitosi e infiammazione: CD3ζ (il classico modulo dei linfociti T), CD32a (un recettore che lega bersagli rivestiti di anticorpi), componenti di CR3 CD11b e CD18 (recettori chiave del complemento) e TLR4 (un sensore del pericolo microbico). Usando perle e pseudovirus rivestiti con la proteina spike di SARS‑CoV‑2, hanno misurato quanto ogni design di CAR permettesse alle cellule di inglobare i bersagli, produrre molecole infiammatorie e successivamente attivare linfociti CD8 umani che avevano già incontrato il virus. Hanno poi trasferito i design più promettenti in CAR diretti contro la mesotelina, una proteina sovraprodotta in molti tumori solidi, per verificare se le stesse regole valessero in un contesto tumorale.
Costruire migliori mangiatori e amplificatori di segnale
È emerso un quadro chiaro: i CAR basati su CD32a guidavano in modo costante una fagocitosi più forte e più rapida rispetto a quelli che utilizzavano il convenzionale dominio CD3ζ, nonostante CD3ζ contenga più dei consueti motivi di attivazione. In altre parole, l’“adattamento” tra il segnale e la macchina del macrofago contava più della pura intensità del segnale. L’aggiunta di frammenti derivati da CR3 (CD11b o CD18) sopra CD32a non aumentava ulteriormente la capacità di fagocitosi nella maggior parte delle condizioni, ma aumentava i livelli di citochine infiammatorie chiave come TNF‑α e IL‑1β. Le combinazioni contenenti TLR4 spingevano ancora oltre nell’aumentare i segnali infiammatori e il marcatore di superficie CD86, associato alla capacità di stimolare i linfociti T, sebbene ciò comportasse compromessi: livelli più bassi di CAR sulla superficie cellulare e una fagocitosi leggermente ridotta.
Dal mangiare all’insegnare i linfociti T
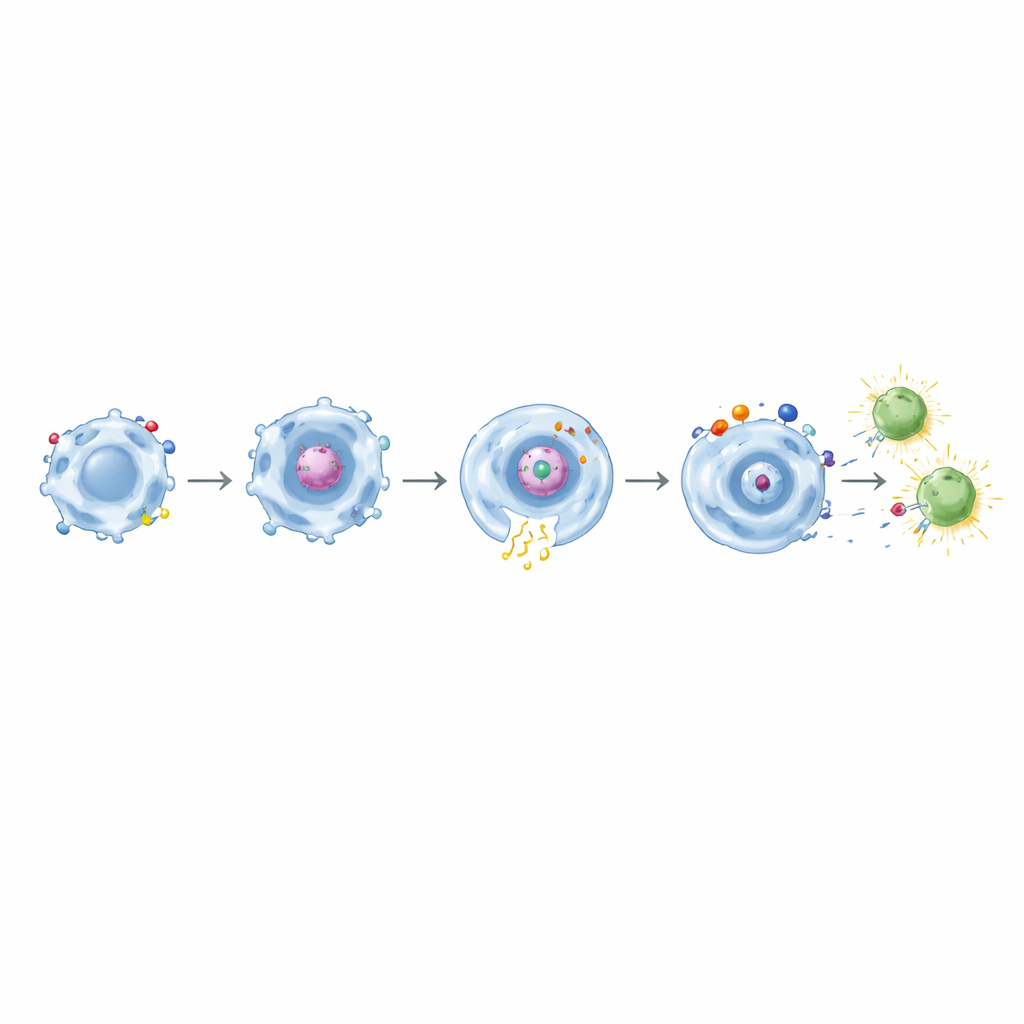
Fondamentalmente, dopo che i macrofagi dotati di CAR basati su CD32a avevano inglobato la proteina spike, sono stati in grado di attivare linfociti CD8 di memoria provenienti da persone precedentemente vaccinate contro il COVID‑19. Questi linfociti hanno espresso marker di attivazione precoce e prodotto molecole effettrici come interferone‑γ e TNF‑α. L’effetto è diventato ancora più forte con CAR a doppio dominio che accoppiavano CD32a con CD11b, CD18 o TLR4. Quando design simili diretti contro la mesotelina sono stati testati su cellule tumorali ingegnerizzate, hanno nuovamente mostrato fagocitosi precisa e dipendente dal bersaglio combinata con un aumento della segnalazione infiammatoria. Tra questi, la combinazione CD32a+TLR4 si è distinta come un potente “allarme tissutale”, potenziando più efficacemente la secrezione di citochine e CD86 pur mantenendo l’ingestione specifica del tumore.
Cosa potrebbe significare per i trattamenti futuri
Per un osservatore non specialista, questo studio mostra che l’ingegnerizzazione dei macrofagi non è un problema di taglia unica. Scambiando e combinando moduli di segnalazione interni, gli scienziati possono modellare cellule che o si concentrano sulla pulizia efficiente delle cellule malate o agiscono più come amplificatori immunitari che rimodellano l’ambiente soppressivo del tumore e richiamano i linfociti T. I CAR basati su CD32a sono emersi come una solida base per tali design, superando i moduli tradizionali dei linfociti T nei macrofagi e funzionando sia contro bersagli virali sia tumorali. Sebbene questi risultati derivino da modelli di laboratorio e debbano essere confermati in cellule umane primarie e in modelli animali, forniscono un progetto per terapie di nuova generazione con CAR-macrofagi che potrebbero affrontare meglio tumori solidi e infezioni persistenti unendo un rapido inglobamento con un’attivazione precisa dei linfociti T.
Citazione: Hong, J., Lee, S., Kim, Y. et al. Optimization of THP-1-CAR monocytes utilizing CD32a signaling phagocytosis for antigen-specific T cell activation. Sci Rep 16, 8175 (2026). https://doi.org/10.1038/s41598-026-39406-6
Parole chiave: CAR macrofagi, segnalazione CD32a, fagocitosi, immunoterapia tumori solidi, attivazione dei linfociti T