Clear Sky Science · it
Dinamicità microbiologica e reologica dei biofilm misti formati da batteri e virus eucariotici
Comunità nascoste sui dispositivi ospedalieri
Molte infezioni ospedaliere non iniziano con un singolo germe, ma con comunità vischiose e invisibili chiamate biofilm che rivestono cateteri e altri dispositivi medici. Questo studio affronta una domanda trascurata ma di grande rilevanza per la sicurezza dei pazienti: cosa succede quando non solo i batteri, ma anche virus capaci di infettare l’uomo penetrano insieme in questi biofilm? Osservando il comportamento di un comune virus dei mammiferi all’interno di biofilm batterici, i ricercatori rivelano come queste città microbiche appiccicose possano silenziosamente ospitare virus e modificarne il comportamento.
Città appiccicose di microbi
I biofilm sono come città microscopiche costruite dai microbi su superfici umide—tubi, rocce, denti o tubi di plastica inseriti nei pazienti. I batteri si insediano, si moltiplicano e secernono una matrice simile a una colla che li protegge dalla disidratazione, dai reagenti chimici e dal sistema immunitario. Negli ospedali, tali biofilm si formano comunemente su cateteri urinari e endovenosi, dove possono dare origine a infezioni del flusso sanguigno e delle vie urinarie difficili da trattare. Questi biofilm contengono di solito molte specie diverse e persino regni di vita differenti, ma la maggior parte delle ricerche si è concentrata unicamente sui batteri, lasciando in gran parte inesplorato il ruolo dei virus.
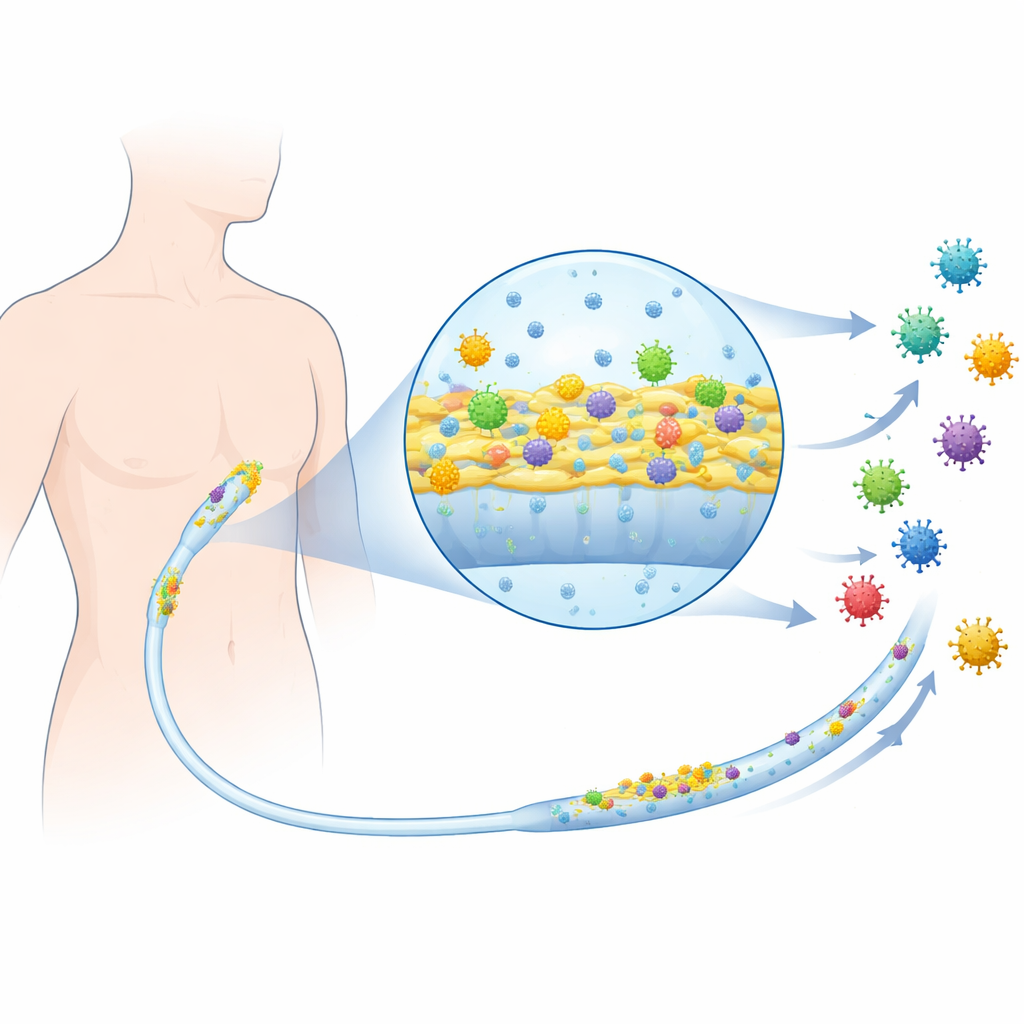
Introdurre un virus di mammifero nella miscela
Il gruppo ha lavorato con ceppi batterici clinici noti per colonizzare i cateteri, inclusi Escherichia coli uropatogeni responsabili di infezioni urinarie e altri batteri frequentemente riscontrati nelle infezioni da catetere centrale. Hanno quindi introdotto il reovirus dei mammiferi, un virus non rivestito ben studiato che infetta cellule animali, come sostituto generale dei virus che infettano l’uomo. Innanzitutto hanno verificato se l’aggiunta di materiale contenente virus influenzasse la crescita batterica normale in sospensione. In molti ceppi i batteri crescevano e sopravvivevano altrettanto bene con o senza il virus, dimostrando che il virus non stava uccidendo direttamente i batteri né agendo come un antibiotico.
I biofilm cambiano consistenza, non dimensione
Quando i batteri si insediano nei biofilm, la storia diventa più sfumata. Per la maggior parte dei ceppi, la quantità totale di biofilm—misurata con una colorazione standard che quantifica quanto materiale riveste una superficie—è cambiata poco in presenza del virus. Alcuni ceppi, però, produssero leggermente più o meno biofilm a seconda della presenza di preparati virali, suggerendo effetti specifici per ceppo. Per andare oltre la semplice quantità, i ricercatori hanno adottato strumenti della scienza dei materiali e misurato quanto ogni biofilm fosse “morbido” o “rigido”, come sondare la consistenza di un gel. Hanno scoperto che ogni ceppo batterico genera una propria firma meccanica. In modo rilevante, l’aggiunta del virus poteva sia irrigidire sia ammorbidire questi biofilm a seconda del ceppo: in un ceppo di E. coli il virus rendeva la matrice più rigida, mentre in un ceppo di Staphylococcus epidermidis il virus portava a una struttura più debole e deformabile.
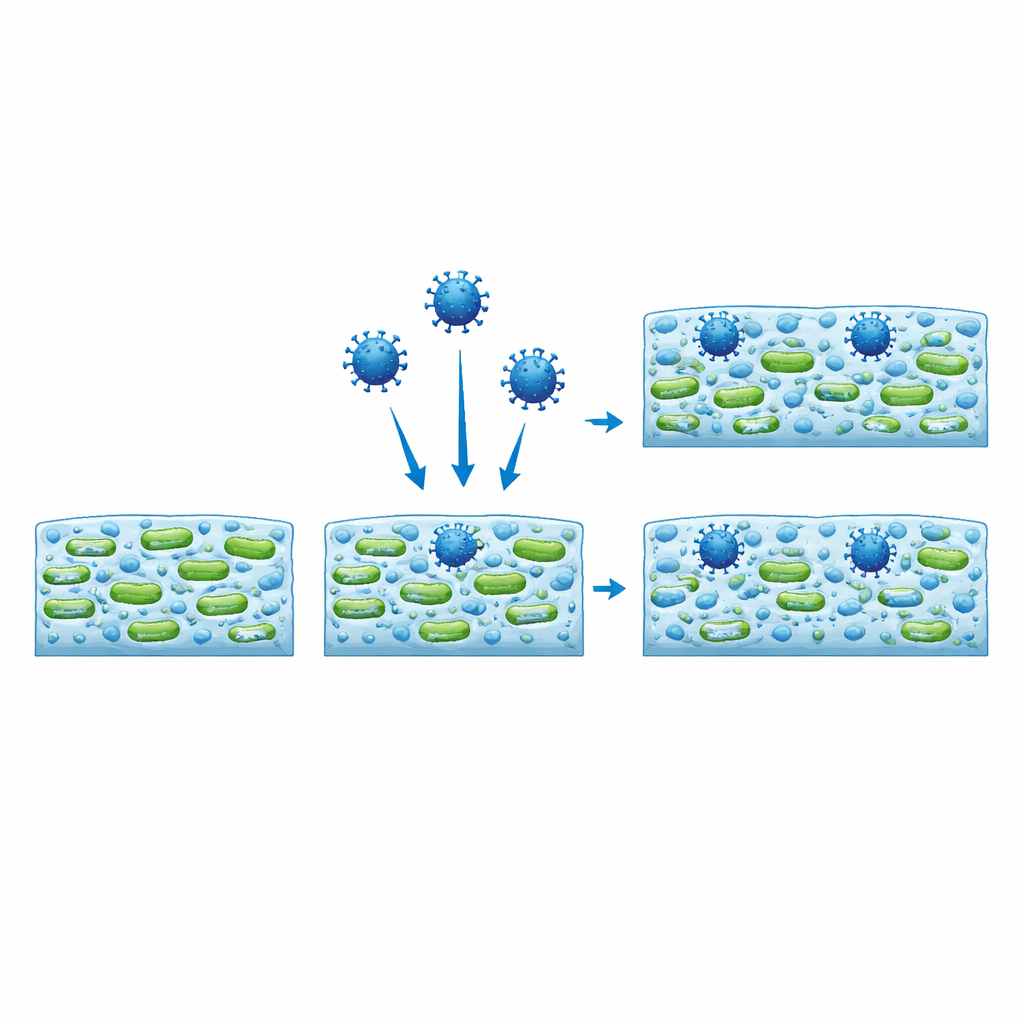
I virus trovano riparo e mantengono la loro capacità infettiva
Con la microscopia a fluorescenza, gli scienziati hanno marcato le particelle virali in modo che brillassero e hanno seguito dove finivano all’interno del biofilm. Diversamente da sfere di plastica inerti di dimensioni simili, che restavano per lo più nelle regioni rade e venivano lavate via, i virus penetrarono in profondità nella matrice e tendevano ad aggregarsi dove le cellule batteriche erano più dense. In alcuni casi la presenza del virus ha persino modificato la forma complessiva del biofilm, trasformando ammassi compatti in reti più filamentose o viceversa, sempre a seconda del ceppo batterico. Per verificare se questi virus intrappolati fossero ancora pericolosi, gli autori li hanno recuperati dai biofilm ed esposti a cellule di mammifero. I virus recuperati sono rimasti infettivi, nonostante fossero stati incorporati nel muco batterico per due giorni.
Perché questo conta per i pazienti e oltre
Per un lettore non specialista, il messaggio chiave è che i biofilm sui dispositivi medici possono non solo proteggere i batteri dai trattamenti—possono anche nascondere e preservare virus che infettano cellule umane o animali. Lo studio mostra che i virus possono alloggiare nella matrice batterica, alterando sottilmente la struttura del biofilm pur restando pienamente capaci di infettare nuove cellule una volta rilasciati. Ciò suggerisce che cateteri e altre superfici ricoperte di biofilm potrebbero fungere da serbatoi silenziosi in cui i virus persistono, protetti dalla disidratazione, dai disinfettanti e dall’attacco immunitario. Comprendere queste comunità microbiche miste può essere cruciale per progettare materiali migliori, strategie di pulizia e terapie che colpiscano sia i partner batterici sia quelli virali, al fine di ridurre le infezioni associate ai dispositivi che risultano difficili da eliminare.
Citazione: Gao, J., Abriat, C., Laekas-Hameder, M. et al. Microbiological and rheological dynamics of mixed biofilms formed by bacteria and eukaryotic virus. Sci Rep 16, 8315 (2026). https://doi.org/10.1038/s41598-026-39314-9
Parole chiave: biofilm, infezioni da catetere, interazioni virus–batteri, reovirus, comunità microbiche