Clear Sky Science · it
Identificazione dei geni condivisi e dei loro microRNA, metaboliti e percorsi correlati nell’ictus ischemico e nell’epilessia
Perché ictus e crisi appartengono allo stesso racconto
L’ictus e l’epilessia vengono spesso trattati come condizioni separate: il primo interrompe l’afflusso di sangue al cervello, la seconda provoca improvvise ondate di attività cerebrale anomala. Eppure molte persone che sopravvivono a un ictus ischemico sviluppano in seguito crisi, una complicanza nota come epilessia post-ictus. Questo studio pone una domanda semplice ma potente: ictus ed epilessia condividono radici biologiche comuni nei nostri geni e nella chimica del sangue, e questi segnali condivisi potrebbero aiutare i medici a prevedere e in ultima analisi prevenire le crisi dopo un ictus?
Alla ricerca di segnali comuni nel sangue
Per esplorare questa connessione, i ricercatori si sono rivolti a grandi banche dati pubbliche di campioni di sangue di persone con ictus ischemico e di persone con epilessia, confrontandoli con controlli sani. Invece di concentrarsi su singoli geni, hanno utilizzato analisi in stile rete che raggruppano geni che tendono ad accendersi o spegnersi in sincronia. Da migliaia di geni che si comportavano in modo diverso nei pazienti rispetto ai controlli, hanno costruito cluster collegati a ciascuna malattia e poi hanno cercato dove le due mappe si sovrapponevano. Questo ha rivelato 38 geni che cambiavano in maniera simile sia nell’ictus sia nell’epilessia, suggerendo meccanismi patologici condivisi piuttosto che coincidenze isolate. 
Rifinire fino a un possibile protagonista chiave
Trovare decine di geni condivisi è solo il primo passo; la sfida è individuare quali contano di più. Il team ha esaminato come questi 38 geni interagivano con altre proteine nella cellula, costruendo una rete proteina–proteina e usando diversi strumenti matematici per segnalare i geni “hub” più influenti. Tre sono emersi in modo chiaro: IL10RA, CD2 e C3AR1. Quando i ricercatori hanno testato quanto l’attività di ciascun gene distinguesse i pazienti dai soggetti sani attraverso più set di dati, tutti e tre hanno mostrato un promettente potere diagnostico. Ma solo uno, C3AR1, risultava costantemente aumentato sia nell’ictus sia nell’epilessia in gruppi di pazienti indipendenti, segnalandolo come il segnale condiviso più robusto.
Dai geni ai piccoli RNA e alle sostanze chimiche cerebrali
I geni raramente agiscono da soli, perciò lo studio si è poi chiesto cosa regoli C3AR1 e come questo possa influenzare la chimica cerebrale. Il team ha analizzato i microRNA — minuscoli frammenti di RNA che modulano finemente l’attività genica — e ha identificato un microRNA in particolare, chiamato let-7b-5p, collegato sia all’ictus sia all’epilessia e predetto come regolatore di C3AR1. Parallelamente, hanno effettuato un’indagine non mirata delle piccole molecole nel sangue (metabolomica) usando campioni di bambini con epilessia. Questo ha rivelato 139 molecole diverse tra i bambini con epilessia e i coetanei sani. Quando questi cambiamenti metabolici sono stati mappati sui percorsi biochimici noti, C3AR1 è riapparso più volte in circuiti connessi alla segnalazione nervosa, in particolare quelli che coinvolgono il neurotrasmettitore acetilcolina, che contribuisce a regolare la comunicazione tra i neuroni.
Come una segnalazione cerebrale alterata potrebbe favorire le crisi
Combinando i dati su geni e metaboliti, i ricercatori hanno costruito una rete più ampia che collega C3AR1 a diverse vie di segnalazione cerebrale, inclusi il ciclo delle vescicole sinaptiche (come i neuroni imballano e rilasciano i messaggeri chimici), la segnalazione colinergica (percorsi guidati dall’acetilcolina), la segnalazione correlata al gusto e percorsi associati alla nicotina. Nel sangue dei bambini con epilessia, i livelli di acetilcolina erano ridotti, e C3AR1 occupava punti strategici nei percorsi dove questa molecola esercita i suoi effetti. Gli autori propongono che variazioni nell’attività di C3AR1, eventualmente guidate da let-7b-5p, potrebbero disturbare la segnalazione legata all’acetilcolina e il rilascio di neurotrasmettitori nelle sinapsi. Col tempo, tali squilibri potrebbero rendere i circuiti cerebrali più eccitabili dopo un ictus, spingendoli verso le crisi. 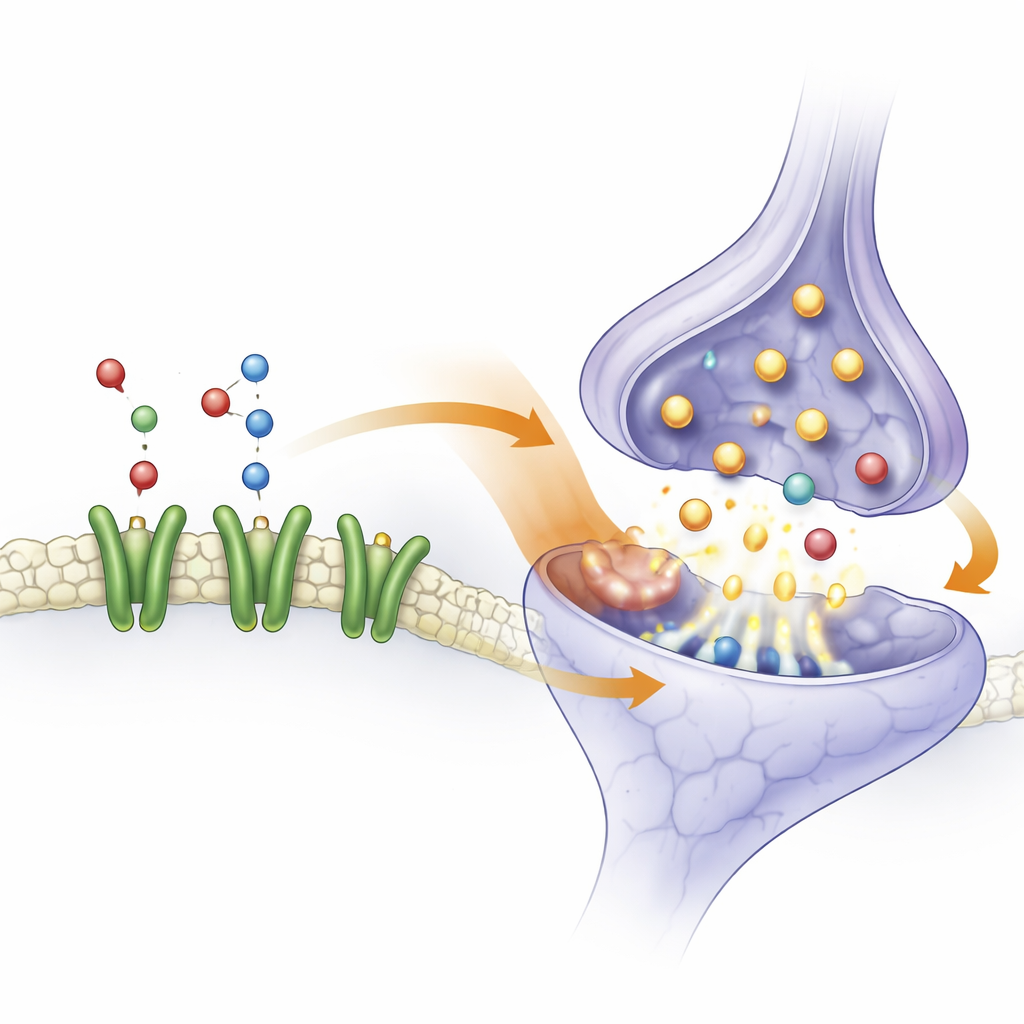
Cosa potrebbe significare per i pazienti
Nel complesso, i risultati suggeriscono che ictus ed epilessia condividono non solo legami clinici ma anche una spina dorsale biologica che comprende il gene C3AR1, il suo microRNA regolatore let-7b-5p e il neurotrasmettitore acetilcolina. Sebbene questi risultati derivino principalmente da analisi di dati e da un gruppo relativamente piccolo di bambini con epilessia, sollevano la possibilità che marcatori ematici possano un giorno aiutare a identificare i sopravvissuti all’ictus ad alto rischio di sviluppare crisi. Gli autori avvertono che C3AR1 da solo difficilmente sarà un predittore perfetto; piuttosto, pannelli di geni, microRNA e metaboliti potrebbero offrire gli strumenti diagnostici più affidabili. Tuttavia, questo lavoro indica una direzione in cui un semplice esame del sangue potrebbe guidare strategie di monitoraggio e trattamento personalizzate per le persone che vivono all’ombra sia dell’ictus sia dell’epilessia.
Citazione: Chen, Y., Man, S., Li, Q. et al. Identifying the shared genes and their related microRNAs, metabolites, and pathways in ischemic stroke and epilepsy. Sci Rep 16, 8166 (2026). https://doi.org/10.1038/s41598-026-39299-5
Parole chiave: ictus ischemico, epilessia post-ictus, biomarcatori, C3AR1, metabolomica