Clear Sky Science · it
Un modello di fisica dei polimeri del nucleo cellulare interfase per simulazioni radiobiologiche
Perché conta la forma della nostra «casa» del DNA
La radiazione è una lama a doppio taglio in medicina: può uccidere le cellule tumorali, ma può anche danneggiare i tessuti sani. Al centro sia dei rischi sia dei benefici c’è il nostro DNA, compattato all’interno del nucleo cellulare. Questo articolo mostra come un modello tridimensionale dettagliato, ispirato alla fisica, di quella «città del DNA» nucleare possa aiutare gli scienziati a prevedere come le radiazioni provocano rotture e riparazioni errate dei cromosomi, con potenziali ricadute sul miglioramento delle terapie oncologiche e delle stime dei rischi da radiazione nello spazio.
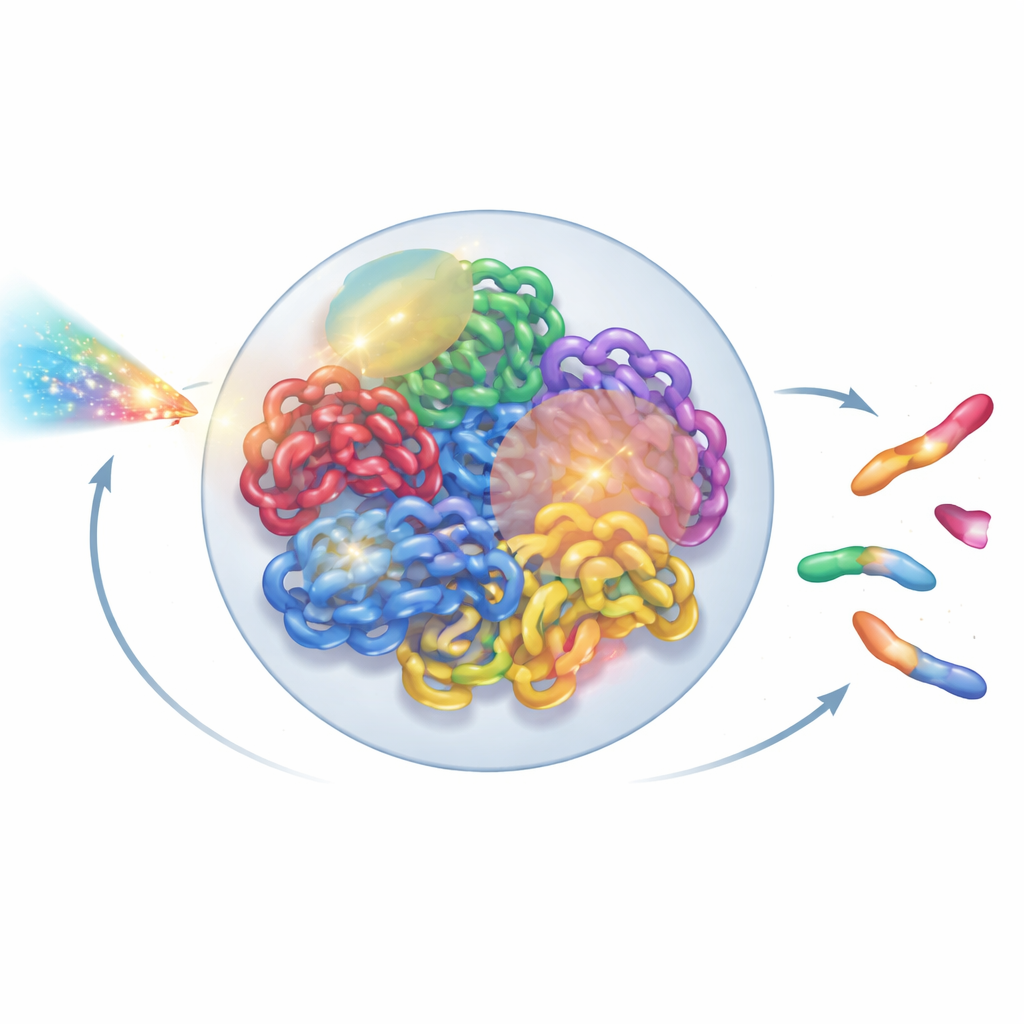
Vedere il genoma come una struttura vivente
All’interno di ogni cellula umana, due metri di DNA sono ripiegati in un nucleo minuscolo di pochi micrometri di diametro. Questo ripiegamento non è casuale: ogni cromosoma tende a occupare il proprio territorio, ulteriormente suddiviso in quartieri e domini ad anello. Nuovi strumenti sperimentali, come la microscopia a super-risoluzione e le mappe di contatto Hi-C, hanno rivelato questo intricato layout 3D in dettaglio sorprendente. Eppure la maggior parte dei modelli di radiazione continua a trattare il DNA come un groviglio semplificato di linee o anelli idealizzati, trascurando questa organizzazione su ordine superiore. Gli autori si sono posti l’obiettivo di costruire un modello dell’intero nucleo che rispetti le conoscenze dei biologi sull’architettura reale della cromatina, pur restando sufficientemente veloce da eseguire su normali computer di laboratorio.
Costruire un nucleo virtuale con la fisica dei polimeri
Il gruppo ha modellizzato i cromosomi come catene flessibili, prendendo spunto dalla fisica dei polimeri, lo stesso campo usato per capire materie plastiche e materiali morbidi. Hanno suddiviso il problema in tre fasi di rilassamento per contenere l’enorme costo computazionale. Prima hanno posizionato ampi blocchi costitutivi chiamati domini di cromatina all’interno del nucleo, permettendo loro di respingersi, allungarsi lungo la lunghezza e raggrupparsi in subcompartimenti più estesi. Secondo, hanno ingrandito ciascun dominio per disporre le fibre di cromatina più fini, incluse le regioni ad anello tenute insieme da proteine leganti. Terzo, hanno lasciato interagire liberamente tutte le fibre di nuovo all’interno del confine nucleare per avvicinarsi a una configurazione finale realistica. Dividendo il processo in questo modo e aggiungendo ricerche gerarchiche e trucchi di calcolo parallelo, hanno ridotto il tempo di esecuzione da quattro mesi impraticabili a circa tre ore per nucleo virtuale su una workstation a 64 core.
Dalle tracce di radiazione alle rotture e riparazioni del DNA
Una volta costruito il nucleo virtuale, gli autori hanno sovrapposto le tracce di radiazione dettagliate generate dalle simulazioni Geant4-DNA. Hanno usato una ricerca gerarchica per trovare, per ogni evento di ionizzazione, quale dominio di cromatina, quale segmento di fibra e infine quale nucleotide fosse il più vicino, senza mai memorizzare in memoria tutte e dieci miliardi di posizioni nucleotidiche. Al contrario, hanno mantenuto un modello riutilizzabile di cromatina e applicato trasformazioni di coordinate intelligenti al volo. Le ionizzazioni nello scheletro del DNA sono state trattate come rotture di filamento, e rotture vicine su filamenti opposti sono diventate rotture a doppio filamento. Per imitare la macchina di riparazione cellulare, gli autori hanno introdotto una regola di riunione basata sulla distanza: estremità di DNA libere che si trovano vicine sono più propense a ricongiungersi. Le decisioni di riunione sono state prese passo dopo passo fino a quando tutte le estremità sono risultate o abbinate o lasciate non riparate, ricreando sia riparazioni corrette sia frammenti mal ricongiunti.
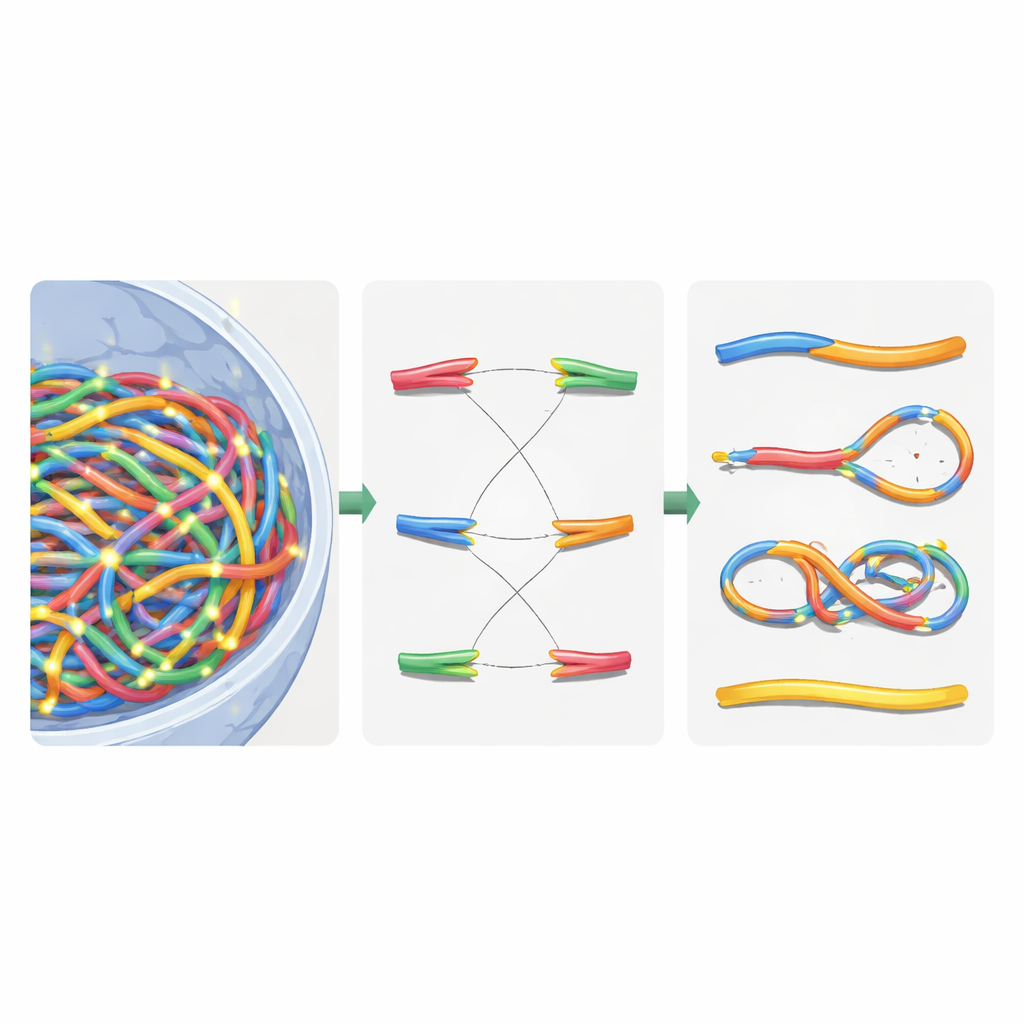
Smistare i cromosomi rotti con la logica delle reti
Dopo questa riparazione virtuale, il nucleo conteneva un mix di cromosomi riassemblati e pezzi residui. Per classificare quanto accaduto, gli autori hanno tradotto il genoma riparato in un grafo non orientato: i segmenti di cromosoma sono diventati archi, e le loro estremità e i punti di rottura sono diventati nodi. Usando un algoritmo standard per componenti connesse, hanno potuto recuperare automaticamente ogni nuovo oggetto di tipo cromosomico e contare caratteristiche chiave come il numero di centromeri (punti di attacco per la divisione cellulare) e telomeri (estremità naturali). Da ciò hanno identificato dicentrici (cromosomi con due centromeri), anelli e delezioni. Hanno quindi confrontato le loro simulazioni con esperimenti classici su cellule della pelle umana esposte a raggi gamma e particelle alfa, rilevando che le aberrazioni cromosomiche totali sono state riprodotte entro circa il 20% dei valori misurati, un miglioramento sostanziale rispetto ai modelli precedenti.
Cosa significa questo per pazienti e astronauti
In termini semplici, questo lavoro mostra che “dove” il DNA si trova nel nucleo e “come” si ripiega influenzano fortemente come il danno da radiazione si somma in cambiamenti cromosomici pericolosi. Combinando un’architettura genomica 3D realistica, simulazioni efficienti basate sulla fisica e una lettura delle rotture cromosomiche basata su grafi, gli autori forniscono un ponte potente tra biologia strutturale e radiobiologia. Sostengono che ulteriori perfezionamenti — come aggiungere la tempistica dettagliata delle riparazioni e utilizzare dati di sequenziamento dell’intero genoma — potrebbero rendere questo approccio ancora più accurato nel prevedere l’impatto biologico delle particelle ad alta energia usate in terapia oncologica o incontrate nello spazio profondo. In ultima analisi, modelli migliori della «casa» del DNA all’interno delle nostre cellule potrebbero aiutare a personalizzare trattamenti a radiazioni più sicuri ed efficaci e affinare la nostra comprensione dei rischi radiativi a lungo termine.
Citazione: Zhao, M., Huang, G., Xu, Z. et al. A polymer physics model of the interphase cell nucleus for radiobiological simulations. Sci Rep 16, 7913 (2026). https://doi.org/10.1038/s41598-026-39234-8
Parole chiave: danno al DNA indotto da radiazioni, architettura 3D della cromatina, aberrazioni cromosomiche, modellizzazione tramite fisica dei polimeri, terapia con particelle