Clear Sky Science · it
Progressione della funzione mitocondriale nelle cellule mononucleate del sangue periferico durante la fase iniziale della sepsi nei pazienti delle unità di terapia intensiva
Perché i “centri energetici” delle nostre cellule contano nelle infezioni letali
La sepsi, una reazione pericolosa per la vita a un’infezione, porta centinaia di migliaia di persone nelle unità di terapia intensiva (UTI) ogni anno e uccide milioni di persone nel mondo. I medici sanno che molti organi possono indebolirsi durante la sepsi, ma il ruolo nascosto di piccoli “centrali” all’interno delle nostre cellule immunitarie — i mitocondri — è stato più difficile da chiarire. Questo studio ha seguito pazienti delle UTI con sepsi durante la prima settimana di cura intensiva per osservare come sia cambiata nel tempo la produzione di energia delle principali cellule immunitarie del sangue e se tali cambiamenti fossero collegati alla sopravvivenza.
Uno sguardo al sangue durante la sepsi
I ricercatori si sono concentrati sulle cellule mononucleate del sangue periferico, un gruppo principale di globuli bianchi che contribuiscono all’infiammazione e alla difesa contro i germi. Poiché circolano in tutto il corpo e sono facili da prelevare, queste cellule offrono una finestra utile su come il sistema immunitario stia affrontando la situazione. Il team ha confrontato 40 adulti con sepsi o shock settico in una UTI olandese con 30 controlli ospedalieri accuratamente abbinati per età e sesso, che non avevano sepsi e risultavano altrimenti metabolicamente sani. Il sangue dei pazienti con sepsi è stato prelevato tre volte — entro due giorni dall’ammissione in UTI e di nuovo intorno ai giorni tre‑quattro e cinque‑sei — mentre il sangue dei controlli è stato campionato una sola volta. Da ogni campione gli investigatori hanno isolato le cellule immunitarie, le hanno poste in una soluzione nutritiva standardizzata e hanno misurato quanto rapidamente i loro mitocondri consumavano ossigeno in diverse condizioni, una lettura diretta di quanto stessero lavorando le “centrali” delle cellule. 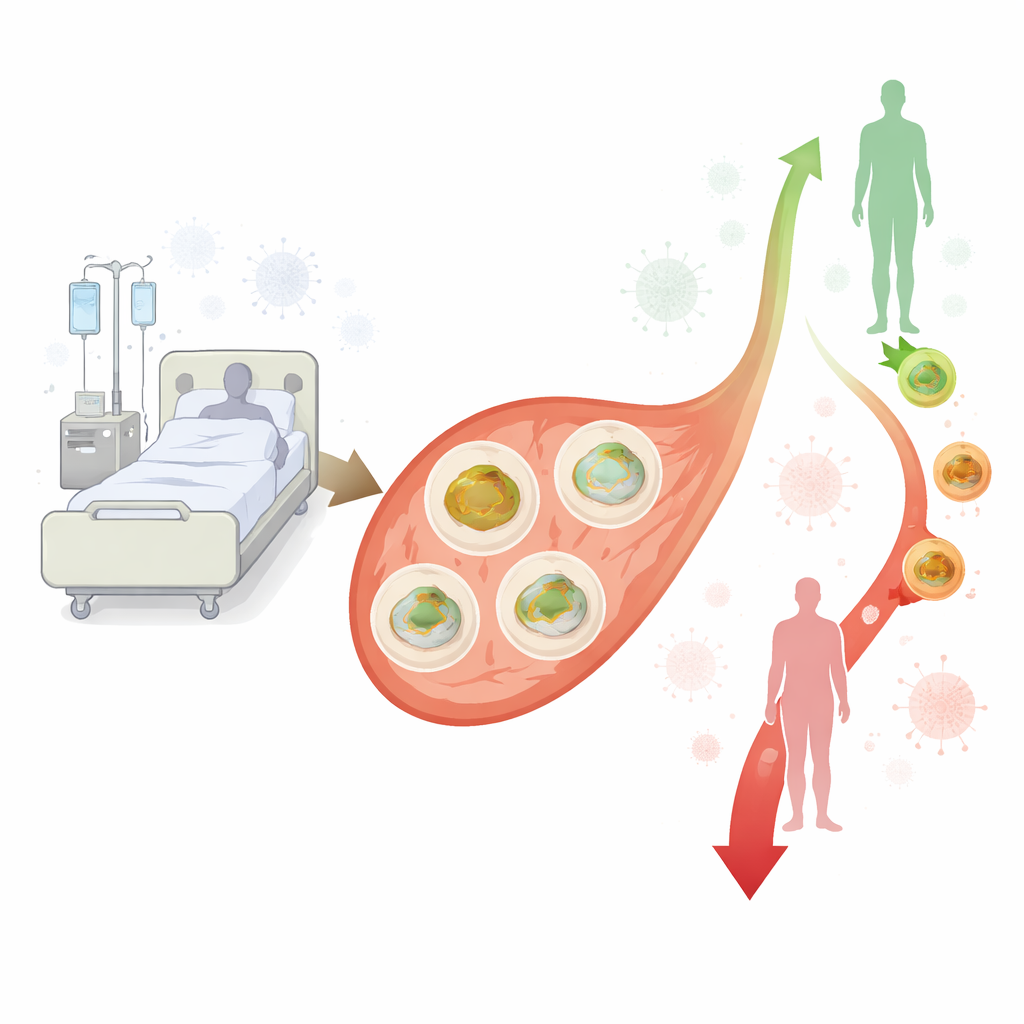
Motori delle cellule immunitarie a pieno regime
Contrariamente all’idea che la sepsi semplicemente «spenga» la produzione energetica cellulare, il team ha riscontrato che l’attività mitocondriale nelle cellule immunitarie era costantemente più elevata nei pazienti con sepsi rispetto ai controlli. In tutti i punti temporali la respirazione basale (l’uso di ossigeno a riposo) risultava aumentata. Anche componenti legati alla produzione utile di energia — la respirazione legata all’ATP — così come la capacità respiratoria massima dei mitocondri tendevano a essere più alte, in particolare verso la fine della prima settimana. Persino la perdita di protoni, una forma di «dispersione» in cui il combustibile viene consumato senza produrre energia, risultava aumentata. Nel loro insieme, questi risultati suggeriscono che, almeno nelle cellule immunitarie circolanti, la macchina energetica è più accelerata che non arrestata durante la fase iniziale della sepsi, forse riflettendo le intense richieste di una risposta immunitaria attivata.
Segnali genici coerenti con l’attività aumentata
Per verificare se questo aumento della «respirazione» fosse supportato a livello molecolare, i ricercatori hanno esaminato l’attività di diversi geni che codificano componenti critici della macchina mitocondriale. In un sottoinsieme di 10 pazienti con sepsi e 10 controlli abbinati hanno misurato l’espressione genica di parti dei complessi della fosforilazione ossidativa — gli assemblaggi proteici che convertono il combustibile in ATP. Due geni in particolare, SDHB (parte del complesso II) e ATP5F1A (parte del complesso V, l’ATP sintasi), risultavano significativamente più attivi nei pazienti con sepsi in più punti temporali, con aumenti di circa il 40–50% rispetto ai controlli. Questo «innalzamento» molecolare dei componenti di base si accorda bene con i dati funzionali, rafforzando l’idea che i mitocondri delle cellule immunitarie siano spinti a lavorare di più durante la sepsi piuttosto che andare incontro a un cedimento totale. 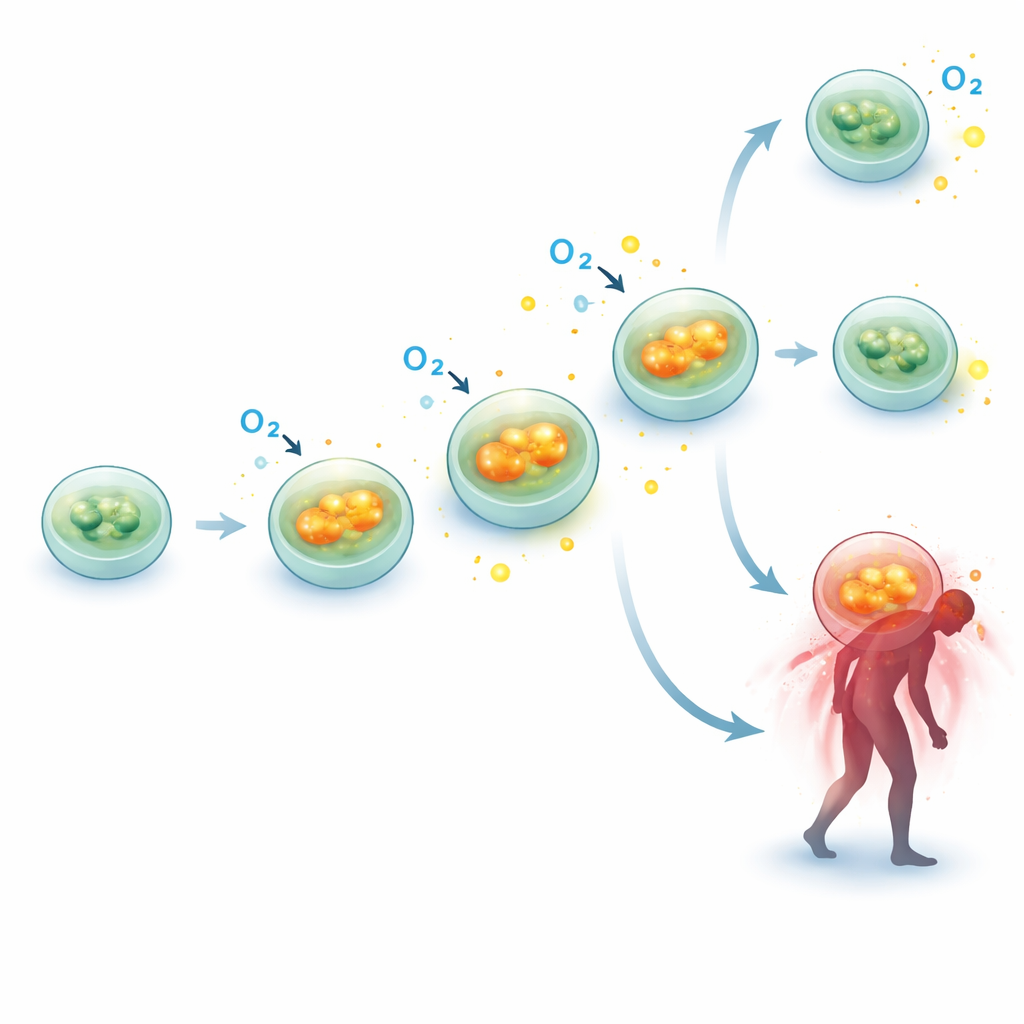
Cambiamenti energetici legati a chi sopravvive e chi no
La scoperta più inquietante riguarda come questi cambiamenti mitocondriali si collegano all’esito clinico. Confrontando i sopravvissuti con i non sopravvissuti a tre mesi, non si osservavano grandi differenze nella funzione mitocondriale alla prima misurazione. Tuttavia, la direzione del cambiamento nella prima settimana raccontava una storia diversa. Nei sopravvissuti la respirazione mitocondriale nelle cellule immunitarie tendeva a diminuire leggermente o a restare stabile. Nei pazienti che poi sono deceduti, le stesse misure — respirazione basale, legata all’ATP, respirazione massima e capacità di riserva — aumentavano ulteriormente nel corso della settimana. L’analisi statistica suggeriva che un incremento più marcato della respirazione basale tra la prima e l’ultima misurazione fosse associato a un rischio maggiore di morte entro tre mesi, anche tenendo conto dei punteggi di gravità della malattia. Poiché il numero di decessi è stato modesto, gli autori sottolineano che questo collegamento è esplorativo e richiede conferma, ma suggerisce che una spinta metabolica persistente e in aumento nelle cellule immunitarie potrebbe essere un segnale d’allarme.
Che cosa significa per i pazienti con sepsi
Per un non specialista, il messaggio centrale è che nella sepsi precoce i “centri energetici” all’interno delle cellule immunitarie circolanti non si limitano a guastarsi; sembrano invece entrare in sovraaccensione. Questo sforzo aggiuntivo può contribuire a sostenere la risposta iniziale dell’organismo contro l’infezione, ma in alcuni pazienti continua a crescere anziché normalizzarsi, e quell’iperattività persistente nelle cellule immunitarie del sangue è stata associata a una sopravvivenza peggiore. Lo studio non dimostra ancora se questo aumento mitocondriale sia utile, dannoso o entrambe le cose in fasi diverse, ma sottolinea che la sepsi è tanto una malattia dell’economia energetica del corpo quanto un problema di infezione e infiammazione. In futuro, monitorare con cura e forse modulare con delicatezza l’uso energetico cellulare potrebbe diventare parte degli strumenti con cui i medici valutano il rischio e personalizzano i trattamenti per le persone che affrontano la sepsi in terapia intensiva.
Citazione: Moonen, H.P.F.X., Slingerland-Boot, R., de Jong, J.C.B.C. et al. Progression of peripheral blood mononuclear cell mitochondrial function during the early phase of sepsis in intensive care unit patients. Sci Rep 16, 8828 (2026). https://doi.org/10.1038/s41598-026-39202-2
Parole chiave: sepsi, mitocondri, cellule immunitarie, malattia critica, metabolismo cellulare