Clear Sky Science · it
Attivazione trascrizionale di PPP1R14C da parte di KLF7 libera l’attività di CDK1 per favorire il carcinoma polmonare a cellule squamose
Perché questa scoperta sul cancro polmonare è importante
Il cancro ai polmoni resta la principale causa di decessi per cancro nel mondo, e una sua forma importante — il carcinoma polmonare a cellule squamose — è rimasta indietro nell’era dei farmaci mirati. A differenza di alcuni altri tumori polmonari trattabili con medicinali diretti contro specifiche mutazioni, questo sottotipo spesso costringe i medici a ricorrere a chemioterapia e immunoterapia, che non funzionano per tutti. Questo studio rivela un circuito di controllo finora nascosto nelle cellule del carcinoma polmonare squamoso che agisce come se tagliasse i freni della divisione cellulare, e indica un punto debole concreto che futuri farmaci potrebbero sfruttare.
Un anello mancante in un cancro difficile da trattare
I ricercatori hanno iniziato esaminando grandi banche dati pubbliche sul cancro per vedere se qualche gene emergesse nel carcinoma polmonare a cellule squamose. Uno, chiamato PPP1R14C, è risultato costantemente presente a livelli elevati nei campioni tumorali rispetto al tessuto polmonare normale. La sua abbondanza aumentava con l’avanzare dello stadio tumorale, e i pazienti i cui tumori esprimevano maggiormente questa molecola tendevano ad avere una sopravvivenza più breve. Questi schemi erano evidenti sia a livello di RNA — i messaggi che le cellule usano per costruire le proteine — sia a livello proteico, suggerendo che PPP1R14C non fosse solo presente ma attivamente coinvolto nella progressione della malattia. 
Come i tumori polmonari tolgono i freni
Per capire perché PPP1R14C fosse così abbondante in questi tumori, il team si è concentrato sull’interruttore on–off del gene, il suo promotore. Combinando più database che tracciano dove vari fattori di controllo si legano al DNA, hanno individuato un fattore chiamato KLF7 come sospetto principale. In cellule di carcinoma squamoso polmonare coltivate in laboratorio, aumentare i livelli di KLF7 faceva salire PPP1R14C, mentre ridurre KLF7 lo abbassava nettamente. Esperimenti che hanno collegato il promotore di PPP1R14C a un riportatore luminescente hanno confermato che KLF7 può attivare direttamente questo interruttore; modificare una breve sequenza di DNA dove KLF7 si lega annullava l’effetto. Una tecnica che isola il DNA legato a KLF7 da cellule intatte ha mostrato che questo fattore si trova fisicamente sul promotore di PPP1R14C, chiudendo il cerchio sul fatto che KLF7 attiva direttamente questo gene.
Dal interruttore genetico al comportamento aggressivo
Una volta capito cosa aumenta PPP1R14C, gli scienziati hanno chiesto cosa faccia effettivamente la molecola. Usando linee cellulari di carcinoma squamoso polmonare, hanno abbassato PPP1R14C con strumenti genetici e osservato il comportamento delle cellule. Le cellule prive di PPP1R14C crescevano più lentamente, formavano meno colonie, invadevano meno attraverso una barriera di gel e avevano una maggiore propensione alla morte cellulare programmata. L’immagine speculare era vera: cellule ingegnerizzate per produrre PPP1R14C in eccesso si dividevano più rapidamente, formavano più colonie e invadevano con maggiore aggressività. Quando queste cellule modificate sono state impiantate in topi, i tumori con PPP1R14C ridotto crescevano meno e pesavano di meno. Messo insieme, ciò dimostra che PPP1R14C non è un semplice spettatore ma un driver attivo delle proprietà cancerose.
Uno sguardo passo dopo passo al motore del ciclo cellulare
Approfondendo, il team ha esaminato quali programmi cellulari dipendessero da PPP1R14C. Indagini ampie sull’attività genica hanno rivelato che la rimozione di PPP1R14C disturbava in particolare i geni che controllano il checkpoint critico G2/M — il punto in cui una cellula si impegna a dividersi in due. Al centro di questo checkpoint c’è CDK1, un interruttore maestro per l’ingresso in mitosi. Nelle cellule cancerose con alto PPP1R14C, CDK1 portava un gruppo fosfato attivante e i suoi target a valle risultavano attivati, segnalando via libera alla divisione. Quando PPP1R14C veniva ridotto, questa attivazione diminuiva. Esperimenti biochimici hanno spiegato il motivo: PPP1R14C si lega a un enzima «gomma da cancellare» cellulare chiamato PP1, che normalmente rimuove il gruppo fosfato attivante da CDK1. Bloccando PP1, PPP1R14C ne impedisce l’accesso a CDK1, così il segnale di attivazione persiste e le cellule continuano a ciclare. 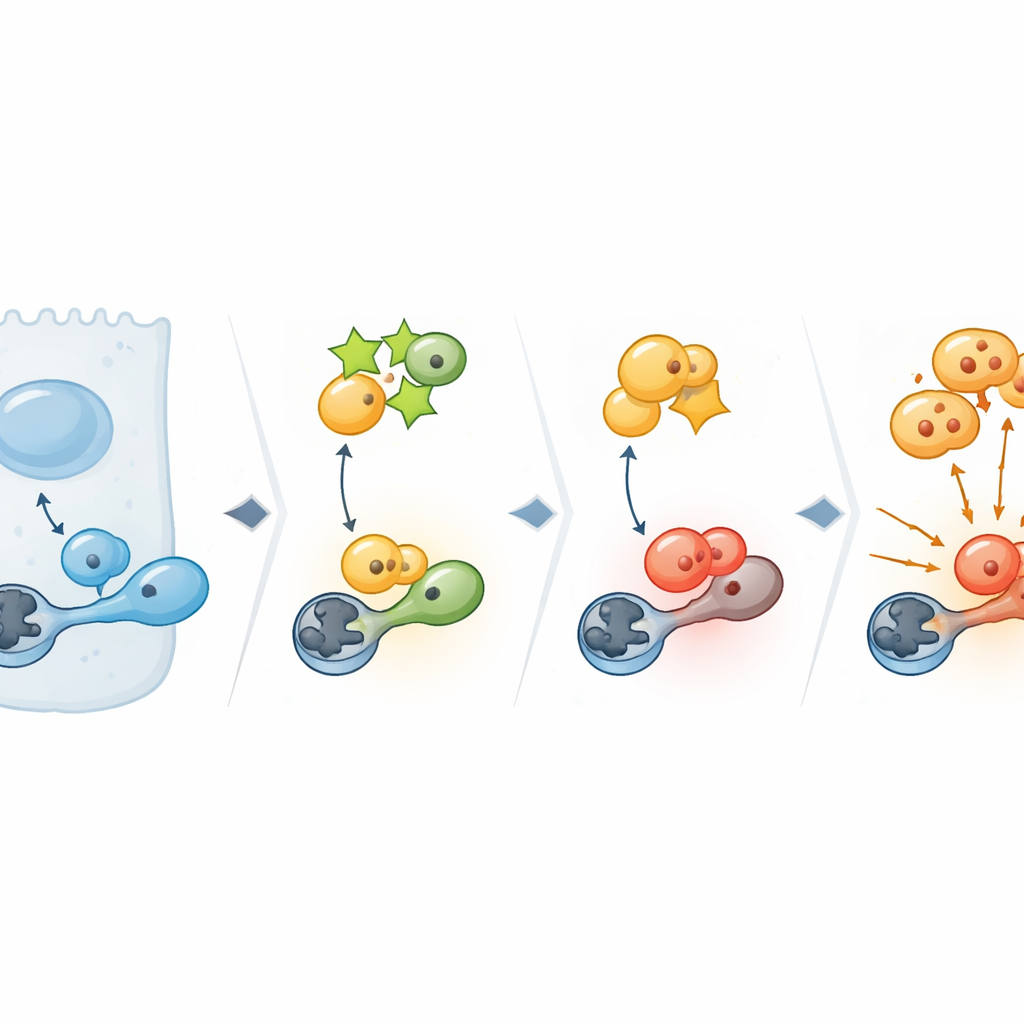
Trasformare un’intuizione molecolare in un’idea terapeutica
La parte più incoraggiante del lavoro è arrivata quando i ricercatori hanno testato un farmaco che blocca direttamente CDK1. In cellule sovraccariche di PPP1R14C, questo inibitore di CDK1 ha annullato il vantaggio di crescita, ridotto la formazione di colonie e limitato l’invasione, riapplicando efficacemente i freni che PPP1R14C aveva rilasciato. Mettendo insieme i pezzi, lo studio delinea una catena di eventi chiara: KLF7 attiva PPP1R14C; PPP1R14C neutralizza PP1; CDK1 rimane iperattivo; e le cellule del carcinoma squamoso polmonare si dividono senza controllo. Per i non specialisti, questo significa che gli scienziati hanno identificato sia un segnale d’allarme — livelli elevati di PPP1R14C che contraddistinguono tumori più pericolosi — sia una leva terapeutica promettente: farmaci che spengono CDK1, in particolare nei pazienti i cui tumori dipendono da questo circuito fuori controllo.
Citazione: Xing, L., Yuan, C., Shen, X. et al. Transcriptional activation of PPP1R14C by KLF7 unleashes CDK1 activity to promote lung squamous cell carcinoma. Sci Rep 16, 9244 (2026). https://doi.org/10.1038/s41598-026-39174-3
Parole chiave: carcinoma polmonare a cellule squamose, ciclo cellulare, CDK1, PPP1R14C, terapia mirata