Clear Sky Science · it
La carenza di Dlgap2 interrompe l’omeostasi sinaptica promuovendo la degradazione ubiquitina-mediata di Itsn1 in un modello simile all’autismo indotto dall’acido valproico
Perché un farmaco comune e l’organizzazione del cervello contano
L’acido valproico è un farmaco usato da tempo per l’epilessia e i disturbi dell’umore, ma se assunto durante la gravidanza è stato associato a un maggiore rischio di autismo nei figli. Questo studio affronta una domanda importante per famiglie e clinici: cosa fa esattamente questo medicinale al cablaggio del cervello in sviluppo? Tracciando i cambiamenti fino a molecole specifiche nelle sinapsi — i punti di comunicazione tra i neuroni — i ricercatori svelano una nuova catena di eventi che potrebbe aiutare a spiegare comportamenti simili all’autismo e indicare possibili strategie terapeutiche future. 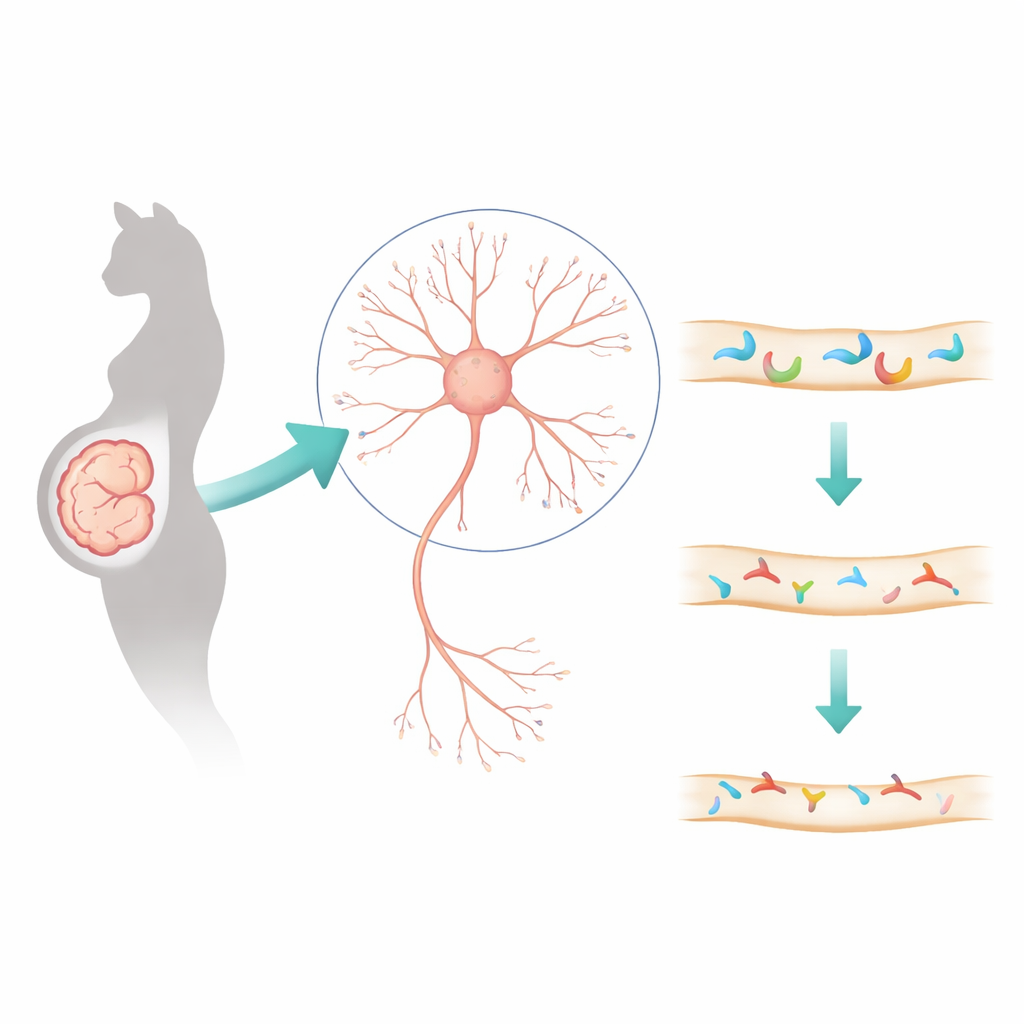
Cercare punti critici condivisi attraverso le specie
Per trovare indizi affidabili, il team non si è basato su un unico modello animale. Ha confrontato cervelli o tessuti corticali simili al cervello provenienti da organoidi corticali umani, scimmie, ratti e topi esposti all’acido valproico prima della nascita. Utilizzando indagini su larga scala di geni e proteine, hanno identificato un piccolo insieme di geni che cambiavano in tutti questi sistemi e che erano legati alle sinapsi e all’isolamento delle fibre nervose. Tra questi, uno è emerso in modo particolare: Dlgap2, una proteina impalcatura che aiuta a organizzare il lato postsinaptico delle sinapsi eccitatorie. Nei topi esposti prenatally all’acido valproico, i livelli di Dlgap2 sono diminuiti nella corteccia e, più specificamente, all’interno di minuscoli compartimenti sinaptici, suggerendo che questa molecola strutturale sia una vittima chiave dell’esposizione al farmaco.
Dai cambiamenti molecolari ai comportamenti
Gli autori si sono poi chiesti se la perdita di Dlgap2 sia di per sé sufficiente a disturbare la funzione cerebrale. Hanno usato virus contenenti RNA a forcina corta per ridurre Dlgap2 in neuroni murini coltivati e in topi neonati. In coltura, i neuroni con Dlgap2 ridotto sviluppavano rami più corti e presentavano meno puncta postsinaptici, segni di connessioni indebolite. Negli animali viventi, l’abbassamento mirato di Dlgap2 nel cervello ha prodotto comportamenti simili all’autismo: giovani maschi mostravano difficoltà a imparare la posizione di una piattaforma nascosta in un labirinto d’acqua e ridotto interesse per i partner sociali e per la novità sociale in un test a tre camere. Questi cambiamenti imitano i deficit di apprendimento e sociali osservati negli animali esposti all’acido valproico, rafforzando l’ipotesi che la perdita di Dlgap2 non sia solo un effetto collaterale ma un fattore causale delle alterazioni comportamentali.
Individuare un partner vulnerabile nella sinapsi
Per capire come la perdita di Dlgap2 riverberi nella sinapsi, i ricercatori hanno esaminato più da vicino le proteine ancorate nella densità postsinaptica, il denso tappetino molecolare che riceve i segnali chimici. Attraverso la proteomica, hanno riscontrato che la riduzione di Dlgap2 alterava l’abbondanza di centinaia di proteine sinaptiche, in particolare quelle coinvolte nell’organizzazione delle sinapsi e nel riciclo delle vescicole tramite endocitosi. Una proteina, Intersectin‑1 (Itsn1), è diminuita in modo particolarmente marcato. Ulteriori analisi biochimiche hanno mostrato che Dlgap2 e Itsn1 convivono fisicamente negli stessi complessi proteici nelle frazioni arricchite per sinapsi e che entrambe sono presenti nell’elenco di geni associati all’autismo. Ciò ha indicato una partnership regolatoria mirata tra le due molecole all’interno del paesaggio sinaptico affollato. 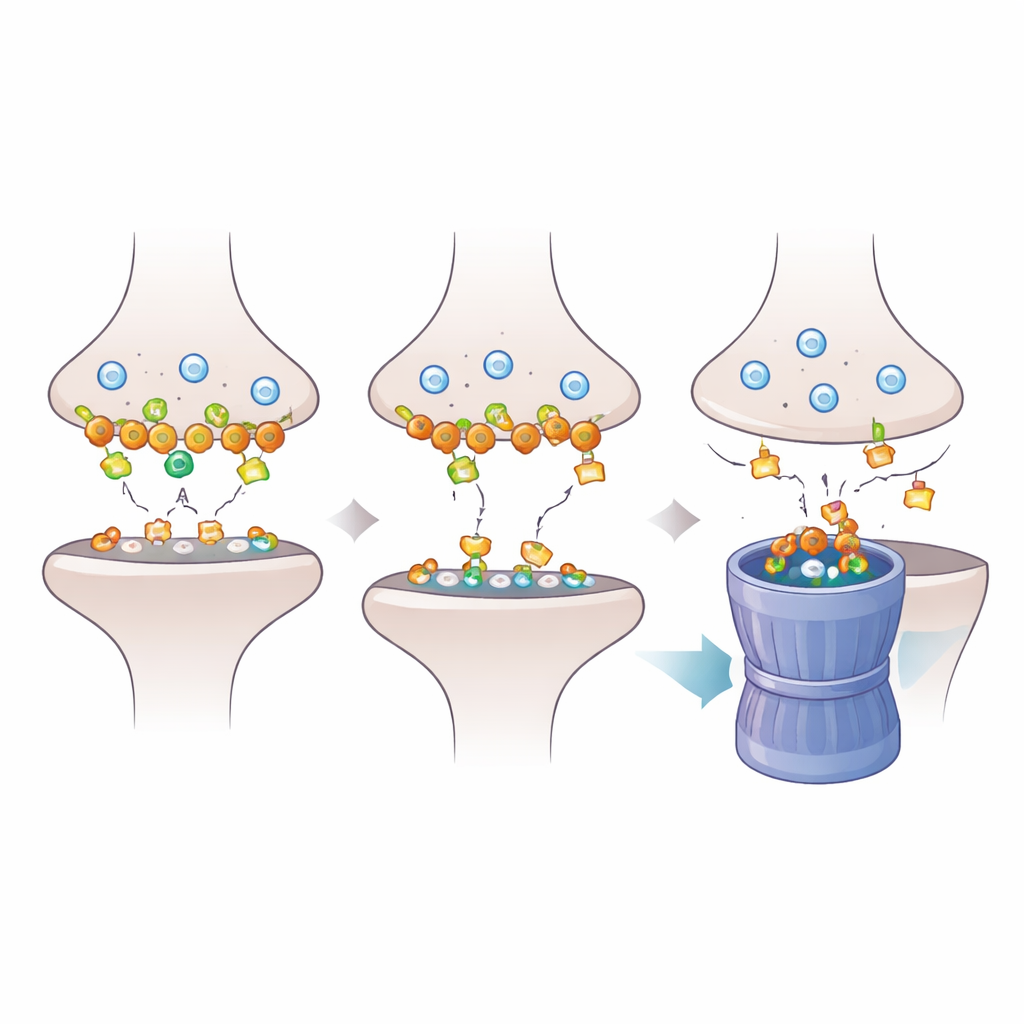
Viene alla luce una via di smaltimento nascosta
Il team si è poi chiesto perché i livelli di Itsn1 diminuiscano quando manca Dlgap2. Hanno osservato che nei compartimenti sinaptici l’abbassamento di Dlgap2 scatenava una forma di marcatura proteica nota come ubiquitinazione legata a K48, che segnala le proteine per la degradazione da parte del proteasoma cellulare, il “tritaglio” della cellula. Bloccare questo sistema di smaltimento con il farmaco MG132 ha impedito la perdita di Itsn1, indicando che Dlgap2 normalmente protegge Itsn1 dall’essere marcata e distrutta. In assenza di Dlgap2, Itsn1 viene sempre più etichettata, avviata al proteasoma e depletata dalle sinapsi, compromettendo il riciclo endocitico e l’equilibrio dell’attività sinaptica. Il lavoro suggerisce che spostamenti sottili nella velocità di turnover delle proteine chiave possono destabilizzare le sinapsi durante lo sviluppo cerebrale.
Cosa significa per l’autismo e i trattamenti futuri
Nel complesso, lo studio propone un’idea semplice ma potente per il pubblico non specialistico: l’esposizione prenatale all’acido valproico può indebolire una proteina strutturale “di supporto” (Dlgap2) nelle sinapsi. Quando quel supporto viene meno, la sua proteina partner (Itsn1) diventa eccessivamente bersagliata dal sistema di smaltimento cellulare, portando a un riciclo difettoso dei componenti sinaptici e, in ultima analisi, a circuiti cablati in modo errato e a comportamenti simili all’autismo nei topi. Sebbene molti geni e fattori ambientali contribuiscano all’autismo, questo asse Dlgap2–Itsn1 offre una catena molecolare concreta che collega l’esposizione prenatale al farmaco alla funzione cerebrale alterata. A lungo termine, strategie che preservino questa partnership o modulino finemente la macchina di smaltimento delle proteine nelle sinapsi potrebbero aiutare a proteggere i cervelli in via di sviluppo da forme simili di perturbazione.
Citazione: Guo, X., Zhang, L. & Zhuang, K. Dlgap2 deficiency disrupts synaptic homeostasis by promoting ubiquitin-mediated Itsn1 degradation in a valproic acid-induced autism-like model. Sci Rep 16, 8305 (2026). https://doi.org/10.1038/s41598-026-39099-x
Parole chiave: acido valproico e gravidanza, proteine impalcatura sinaptica, meccanismi dello spettro autistico, via ubiquitina-proteasoma, modelli murini di autismo