Clear Sky Science · it
Il recettore CaSR nei pesci zebra modula struttura e funzione cardiaca
Perché il cuore dei pesci importa per la salute umana
I nostri cuori si affidano al calcio, un minerale semplice, per battere correttamente. Quando i segnali calciici si alterano, il risultato può essere insufficienza cardiaca o altre malattie gravi. Questo studio usa piccoli pesci zebra—pesci d’acqua dolce trasparenti spesso impiegati nei laboratori—per esplorare come un interruttore che rileva il calcio nelle cellule modelli la forza e la sopravvivenza del cuore. Disattivando un singolo gene che aiuta le cellule a percepire il calcio, i ricercatori hanno scoperto una catena di problemi nella capacità di pompa del cuore, nella forma del corpo e persino nella vescica natatoria piena d’aria del pesce. Il loro lavoro mostra anche che il background genetico di un animale può attenuare o aggravare in modo drammatico l’impatto di una mutazione dannosa, una lezione con chiare risonanze nella medicina umana.
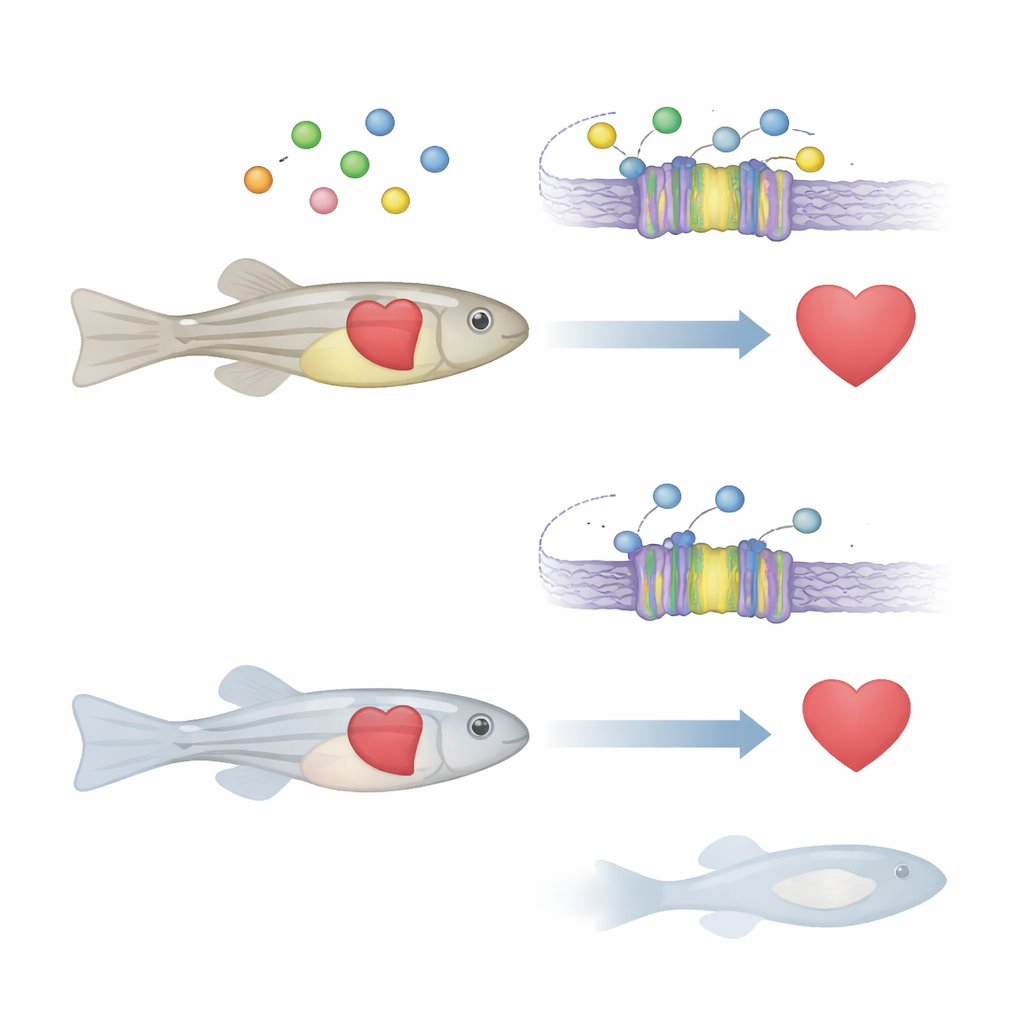
Un “termostato” cellulare per il calcio
Il calcio dentro e fuori le cellule agisce come un segnale universale che controlla il movimento muscolare, il rilascio ormonale e persino quali geni si attivano. Molti organi dipendono da una proteina chiamata recettore sensibile al calcio, che funziona come un termostato per i livelli di calcio. Quando il calcio extracellulare cambia, questo recettore regola il rilascio di ormoni e altri processi per ripristinare l’equilibrio. Nell’uomo, i difetti di questo recettore sono già associati a disturbi di ossa e minerali e sono sospettati attori in malattie cardiache e alcuni tumori. Tuttavia, rimaneva poco chiaro come questo sensore del calcio influisca sullo sviluppo e sulla funzione cardiaca in un organismo completo.
Cosa succede quando il sensore del calcio viene spento
Il team si è concentrato sulla versione del gene nel pesce zebra, chiamata casr, che è fortemente conservata rispetto al corrispondente umano. Usando strumenti moderni di editing genetico, hanno creato pesci zebra in cui entrambe le copie di casr erano disattivate. All’inizio, i giovani pesci apparivano quasi normali. Ma entro cinque giorni dalla fecondazione, molti mutanti non riuscivano a gonfiare la vescica natatoria, un piccolo organo pieno di gas che controlla la galleggiabilità. Questi pesci affondavano sul fondo, nuotavano male, sviluppavano presto una curvatura della colonna vertebrale e tutti morivano entro due settimane di età. Questi segni esteriori indicavano seri problemi interni che coinvolgevano più di un sistema d’organo.
Un cuore più debole, più piccolo e più lento
Video ad alta velocità e analisi delle immagini dei cuori in attività hanno rivelato quanto profondamente il mancato sensore del calcio avesse compromesso le prestazioni cardiache. Nei normali larve di pesce zebra, il ventricolo si riempie e si svuota in un pattern ritmico e robusto. Nei mutanti, il ventricolo era visibilmente più piccolo durante la fase di riempimento, il battito cardiaco era più lento e ogni contrazione pompava meno sangue. Le misure di quanto il muscolo cardiaco si accorcia e di quanto cambia l’area della camera di pompaggio a ogni battito erano entrambe ridotte, indicando una contrazione indebolita. La gittata cardiaca complessiva—il volume di sangue spostato al minuto—è diminuita drasticamente. A livello genico, centinaia di trascritti erano alterati e le reti chiave che regolano la gestione del calcio e la macchina della contrazione muscolare risultavano depotenziate, collegando la modifica genetica sia al fallimento molecolare che a quello meccanico del cuore.
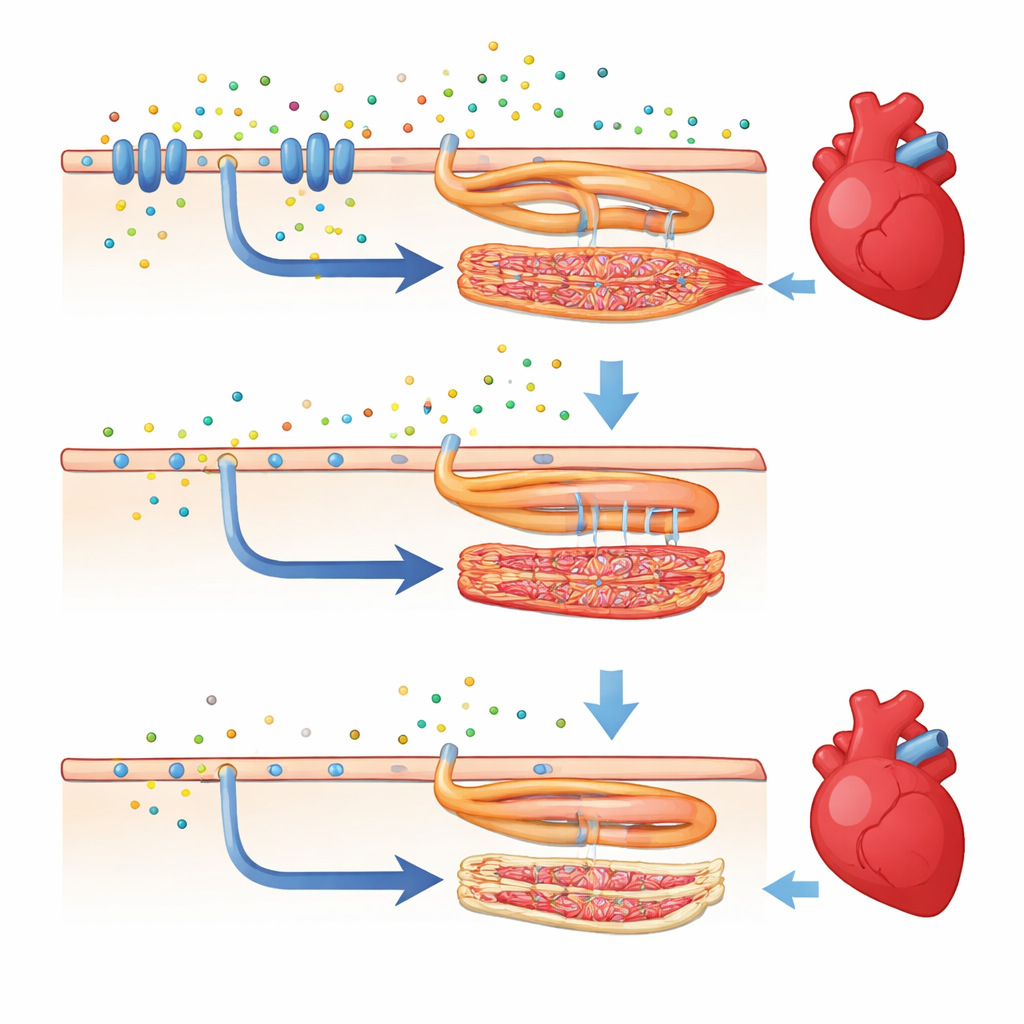
Come i geni di background possono salvare un cuore malato
Sorprendentemente, la stessa mutazione di casr si comportava in modo molto diverso in un’altra comune linea di pesce zebra, nota come TL (Tupfel long-fin). Quando il knockout del gene è stato trasferito in questo nuovo background genetico, i pesci sono riusciti a gonfiare la vescica natatoria, a sopravvivere fino all’età adulta e hanno mostrato una capacità di pompaggio molto migliore. I loro cuori erano ancora in parte compromessi—la frequenza cardiaca restava più bassa del normale—ma le misure di quanto vigorosamente il ventricolo si contraeva e la quantità di sangue pompata al minuto si avvicinavano a quelle dei pesci sani. In questi animali “salvati”, molti dei geni legati alla segnalazione del calcio e alla contrazione del muscolo cardiaco sono tornati a livelli intermedi, più alti rispetto alla linea originariamente malata. Questo rivela che altri geni sparsi nel genoma possono attenuare o intensificare l’impatto di una variazione dannosa.
Segnali che modellano cuore e galleggiamento
Oltre al cuore, la perdita del sensore del calcio ha disturbato anche importanti sistemi di controllo della crescita nell’embrione. I geni delle vie di segnalazione Wnt e Hedgehog—architetti ben noti della formazione degli organi—erano soppressi nei mutanti. Questi cambiamenti probabilmente contribuiscono al fallimento del gonfiamento della vescica natatoria, che a sua volta può peggiorare la sopravvivenza rendendo più difficile per i pesci nutrirsi e muoversi efficacemente. Anche i marcatori della differenziazione delle cellule del muscolo cardiaco risultavano ridotti e i ventricoli erano più piccoli, suggerendo che il sensore del calcio aiuta a guidare come le cellule muscolari cardiache crescono e maturano.
Cosa significa per la comprensione del rischio di malattia
Considerato nel suo insieme, questo lavoro mostra che il recettore sensibile al calcio è un guardiano cruciale sia della funzione cardiaca sia del corretto sviluppo degli organi nel pesce zebra. Quando questo sensore viene a mancare, i segnali calciici vacillano, il muscolo cardiaco si contrae debolmente, la vescica natatoria non si forma correttamente e gli animali muoiono giovani. Eppure il drammatico recupero osservato in una diversa linea genetica evidenzia un messaggio chiave: il resto del genoma può modificare in modo consistente quanto sia pericolosa una certa mutazione. Per la salute umana, questo sottolinea perché persone portatrici di varianti geniche rischiose analoghe possono manifestare esiti molto diversi e perché comprendere sia i geni centrali della malattia sia il loro contesto genetico è essenziale per prevedere e trattare le patologie cardiache.
Citazione: Liu, L., Hu, Y., Xie, B. et al. Zebrafish casr modulates cardiac structure and function. Sci Rep 16, 8543 (2026). https://doi.org/10.1038/s41598-026-39063-9
Parole chiave: segnalazione del calcio, sviluppo cardiaco, modello di pesce zebra, background genetico, funzione cardiaca