Clear Sky Science · it
Identificazione in silico di piccoli antagonisti inalabili IL-33/ST2 per endotipi di asma grave tipo-2-alta
Perché è importante per la respirazione
Per milioni di persone con asma grave, anche gli inalatori moderni e le iniezioni avanzate possono lasciare fiato corto e a rischio di attacchi pericolosi. Questo studio esplora se farmaci familiari, simili a compresse, possano essere riprogettati per funzionare come trattamenti inalati che bloccano uno dei segnali di “allarme” a monte dell’asma nei polmoni. Usando solo simulazioni al computer, i ricercatori hanno cercato piccole molecole che possano adattarsi a un recettore chiave coinvolto nell’asma grave guidata da allergie, gettando le basi per futuri test di laboratorio piuttosto che offrire un medicinale pronto all’uso.
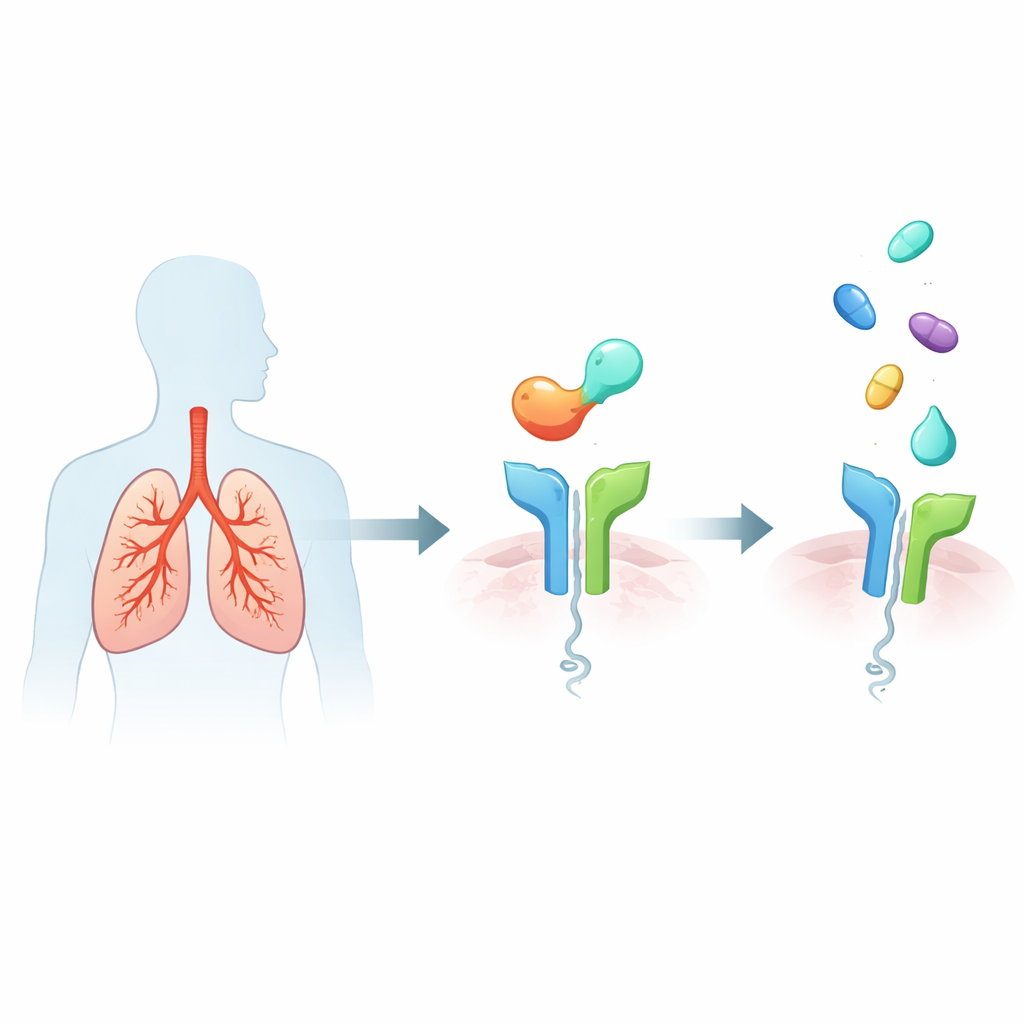
Il sistema di allarme all’interno dei polmoni asmatici
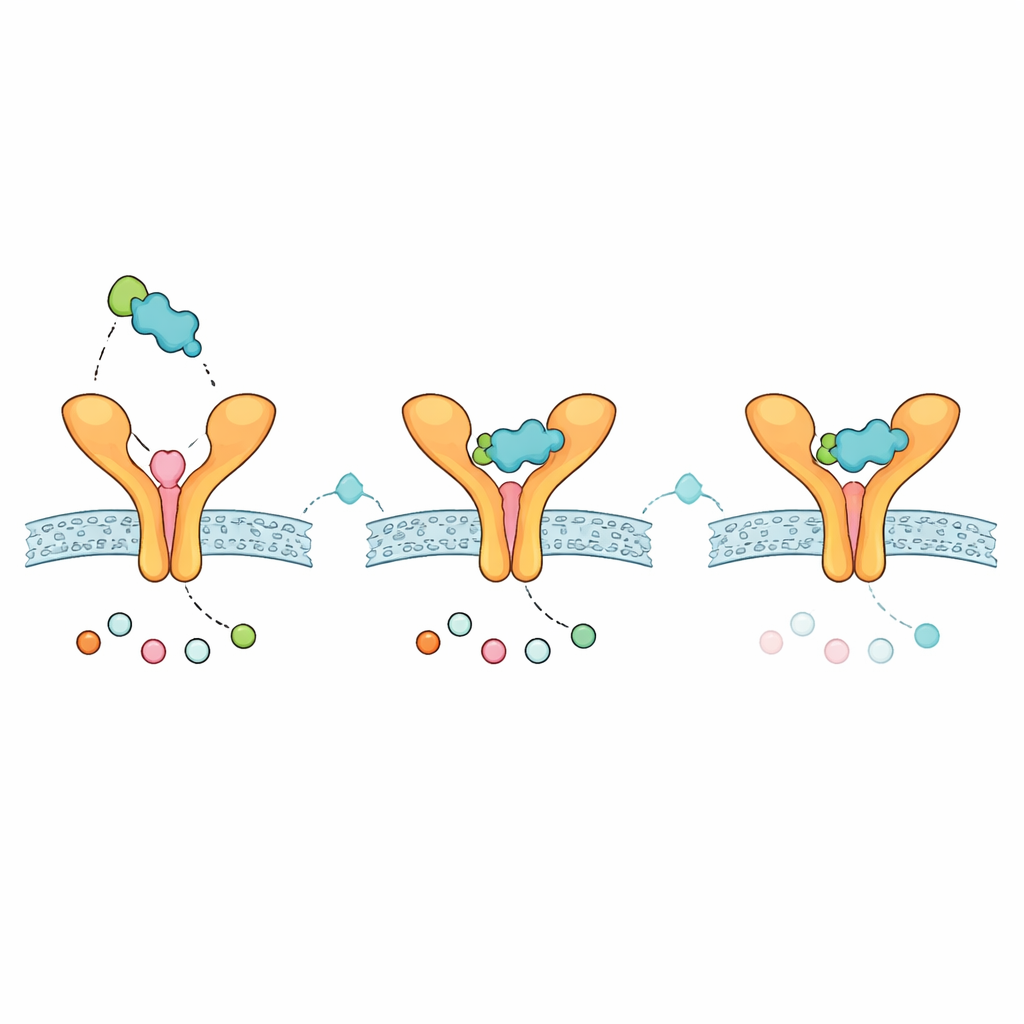
L’asma grave tipo‑2‑alta è caratterizzata da una risposta immunitaria iperattiva che riempie le vie aeree di muco e cellule infiammatorie, restringe i condotti respiratori e danneggia la struttura polmonare nel tempo. Un innesco principale è una proteina chiamata IL‑33, rilasciata dalle cellule della mucosa delle vie aeree sotto stress. IL‑33 si lega a un recettore chiamato ST2 su varie cellule immunitarie, che quindi rilasciano potenti molecole messaggere che guidano le caratteristiche tipiche dell’asma come sibili, riacutizzazioni e rimodellamento a lungo termine delle vie aeree. Poiché una maggiore attività IL‑33/ST2 è collegata a sintomi più gravi e a episodi più frequenti, ST2 è emerso come un interessante bersaglio a monte: bloccare ST2 potrebbe attenuare contemporaneamente molti segnali infiammatori a valle.
Dagli anticorpi ai farmaci di uso quotidiano
Diverse terapie correnti per l’asma grave utilizzano anticorpi iniettati che assorbono proteine infiammatorie nel sangue o bloccano i loro recettori. Pur efficaci per alcuni, questi farmaci biologici sono costosi, devono essere somministrati con iniezione e si concentrano principalmente su segnali più a valle della via. Al contrario, i piccoli farmaci molecolari — più simili a compresse o inalatori tradizionali — potrebbero essere prodotti su larga scala, conservati facilmente e potenzialmente somministrati direttamente nei polmoni. La sfida è che ST2 si lega a IL‑33 tramite un’ampia interfaccia proteina‑proteina, che è più difficile da interrompere per piccole molecole rispetto a una nicchia profonda e ben definita su un enzima. Gli autori si sono quindi rivolti a dati strutturali ad alta risoluzione del complesso ST2–IL‑33 e a strumenti in silico moderni per verificare se alcuni farmaci antiinfiammatori noti potessero inaspettatamente agganciarsi a parte di questa interfaccia.
Esplorare la superficie del recettore con il computer
Utilizzando la struttura cristallina dell’omino ST2 legata a IL‑33, il team ha prima rimosso IL‑33 per esporre la superficie di legame del recettore e ha usato un programma per individuare le tasche più promettenti in cui una piccola molecola potesse annidarsi. Hanno quindi selezionato dieci piccole molecole clinicamente rilevanti già usate per l’asma o malattie immunitarie correlate — come gli antagonisti dei leucotrieni Montelukast e Zafirlukast, relazioni della talidomide con effetti immunomodulanti e inibitori JAK — più una molecola già riportata focalizzata su ST2 come riferimento. Con software di docking virtuale, ogni composto è stato posizionato migliaia di volte sulla superficie di ST2 e le pose meglio adattate sono state valutate in base alla forza di legame predetta. Zafirlukast è emerso come lo scaffold meglio classificato, superando leggermente Montelukast e il comparatore noto diretto contro ST2.
Ottimizzare una molecola guida sullo schermo
Poiché Zafirlukast ha mostrato il bilancio più promettente tra legame predetto e comportamento farmacologico generale, gli autori hanno usato uno strumento di design guidato dall’IA per creare una versione modificata di questa molecola. L’obiettivo era mantenere la sua aderenza a ST2 migliorando al contempo il profilo di sicurezza predetto. L’analogo riprogettato ha avuto un punteggio di docking molto simile ed è stato previsto meno tossico in silico. Mappe di contatto dettagliate hanno suggerito che sia il composto parentale sia quello modificato toccano diversi degli stessi amminoacidi di ST2 che normalmente contattano IL‑33, insinuando che occupano parti funzionalmente importanti dell’interfaccia. Simulazioni di dinamica molecolare estese — mezzo microsecondo di moto virtuale in acqua e sale — hanno mostrato che sia il recettore sia il ligando rimanevano flessibili, con la piccola molecola che campionava diverse posizioni lungo la superficie piuttosto che bloccarsi rigidamente in un punto. I calcoli delle energie di interazione nel tempo hanno indicato un’associazione significativa ma dinamica, coerente con una molecola che esplora una superficie proteina‑proteina relativamente piatta.
Indizi su come potrebbe comportarsi un futuro inalatore
Per esplorare se lo Zafirlukast modificato potesse plausibilmente funzionare come farmaco, il team ha eseguito controlli computazionali standard di assorbimento, distribuzione, metabolismo, escrezione e tossicità. L’analogo ha soddisfatto le regole comuni di drug‑likeness per i farmaci orali, ha mostrato dimensioni e lipofilicità moderate ed è stato previsto che non entri nel cervello — caratteristiche che possono essere favorevoli per un trattamento focalizzato sui polmoni con effetti sistemici limitati. Le stime di solubilità variavano a seconda del modello, implicando che sarebbe necessaria una formulazione accurata, specialmente per vie non orali come l’inalazione. Il composto è stato anche previsto interagire con certi enzimi epatici, suggerendo che eventuali interazioni farmacologiche dovrebbero essere considerate se venisse usato insieme ad altri medicinali.
Cosa dimostra realmente questo lavoro
Piuttosto che fornire un nuovo farmaco per l’asma, questo studio dimostra una strategia computazionale passo‑passo per trovare e perfezionare piccole molecole che potrebbero interferire con il sistema di allarme IL‑33/ST2 sulla superficie delle cellule delle vie aeree. Mettere in evidenza Zafirlukast e un suo parente ottimizzato dall’IA come potenziali punti di partenza per esperimenti di laboratorio mostra che possono occupare parti chiave dell’interfaccia di ST2 e possiedono proprietà predette di sicurezza e di drug‑likeness generalmente accettabili. Tuttavia, tutte le prove sono virtuali: il lavoro non dimostra che queste molecole impediscano a IL‑33 di legarsi a ST2, attenuino la segnalazione infiammatoria o aiutino i pazienti a respirare meglio. Quelle risposte richiederanno test biochimici, studi su cellule, modelli animali e infine trial clinici. Per ora, lo studio offre una mappa computazionale e una breve lista di scaffold candidati per gli scienziati che mirano a trasformare l’interruttore di allarme dell’asma del corpo in un bersaglio terapeutico inalabile pratico.
Citazione: Sun, G., Liu, Q., Yu, M. et al. In Silico identification of inhalable small-molecule IL-33/ST2 antagonists for severe type-2-high asthma endotypes. Sci Rep 16, 7996 (2026). https://doi.org/10.1038/s41598-026-39027-z
Parole chiave: asma grave, via IL-33 ST2, piccoli antagonisti molecolari, progettazione di farmaci in silico, terapeutici per inalazione