Clear Sky Science · it
Peptide derivato dal polline d’api con duplice inibizione della DPP-IV e modulazione del trasporto del glucosio
Perché il polline d’api potrebbe essere importante per la glicemia
Il diabete di tipo 2 viene spesso descritto come un problema di troppo zucchero e troppo poca insulina, ma dietro le quinte una rete di enzimi e trasportatori dirige in modo discreto come il nostro corpo gestisce il glucosio. Questo studio esplora un’idea interessante: che il polline d’api, un “superfood” naturale, possa essere una fonte di piccolissimi frammenti proteici (peptidi) che sia proteggono i segnali ormonali che controllano la glicemia sia modulano in modo lieve l’assorbimento degli zuccheri dall’intestino. Il lavoro si concentra su uno di questi peptidi, chiamato AA-7, e si chiede se potrebbe un giorno ispirare strategie alimentari più sicure per aiutare a gestire il diabete.
Dall’alveare al banco di laboratorio
Il polline d’api è una miscela di pollini vegetali e materiali derivati dalle api, ricca di proteine, vitamine e altri nutrienti. Per simulare la digestione umana, i ricercatori hanno trattato le proteine del polline con due enzimi digestivi, pepsina e pancreatina, simili a quelli del nostro stomaco e del piccolo intestino. Questo processo ha spezzato le grandi proteine in molti frammenti più piccoli, alcuni lunghi solo pochi amminoacidi. Hanno quindi separato questi frammenti per dimensione e proprietà chimiche, testando ogni frazione per la capacità di bloccare un enzima chiamato DPP-IV, che normalmente taglia e inattiva gli ormoni che stimolano il rilascio di insulina. Una frazione di peptidi molto piccoli e relativamente oleosi (idrofobici) è emersa per la sua forte attività inibitoria della DPP-IV. 
Individuare un peptide di spicco
Mediante spettrometria di massa ad alta risoluzione, il team ha identificato un peptide di sette amminoacidi con la sequenza Ala-Thr-His-Ala-Leu-Leu-Ala, che hanno chiamato AA-7. Hanno sintetizzato questo peptide per testarlo isolatamente. Negli saggi enzimatici, AA-7 ha inibito la DPP-IV a concentrazioni micromolari, un po’ meno potente di un farmaco di riferimento da laboratorio ma paragonabile o migliore di molti peptidi di origine alimentare riportati in letteratura. Analizzando come la velocità della reazione cambiava con diverse quantità di peptide e substrato, hanno dimostrato che AA-7 agisce come inibitore competitivo: si posiziona nello stesso sito attivo della DPP-IV usato dai substrati naturali, ostacolandone l’accesso senza distruggere l’enzima.
Interazioni peptide–enzima a livello atomico
Per capire perché AA-7 funziona, i ricercatori hanno usato simulazioni al computer per far incastrare il peptide in un modello tridimensionale della DPP-IV e poi hanno eseguito simulazioni dinamiche molecolari nel tempo. I modelli hanno suggerito che AA-7 si annida nella tasca catalitica dell’enzima, entrando in contatto con amminoacidi chiave già noti come cruciali per l’attività della DPP-IV. Il legame è stato previsto almeno stabile quanto quello di un inibitore di riferimento. Ulteriori analisi computazionali di assorbimento, distribuzione, metabolismo e tossicità (ADMET) hanno fornito un avvertimento realistico: AA-7 è probabilmente sicuro ma non viene assorbito efficacemente attraverso la parete intestinale così com’è, una limitazione comune per i peptidi piccoli. Ciò indica la necessità di strategie di somministrazione o modifiche strutturali se AA-7, o molecole modellate su di esso, dovessero essere impiegate nell’uomo.
Modulare il modo in cui l’intestino gestisce lo zucchero
Lo studio non si è fermato agli enzimi in provetta. Il team ha esposto cellule intestinali umane coltivate (cellule Caco-2) ad AA-7 e ha misurato sia l’assorbimento di glucosio sia l’attività dei geni che codificano per due principali trasportatori intestinali del glucosio, SGLT1 e GLUT2. A dosi non tossiche, AA-7 ha modificato la velocità con cui una forma fluorescente di glucosio entrava nelle cellule, con effetti dipendenti da dose e tempo. Ha inoltre alterato i livelli di espressione genica di SGLT1 e GLUT2 in modi diversi su brevi (30 minuti) e più lunghi (24 ore) periodi. Il docking computazionale ha suggerito che AA-7 può interagire con regioni strutturali di questi trasportatori, sebbene questi modelli vadano considerati ipotesi piuttosto che prove definitive. Nel complesso, i dati cellulari e di modellazione suggeriscono che AA-7 fa più che bloccare la DPP-IV: influisce anche sul meccanismo che trasferisce lo zucchero dall’intestino al sangue. 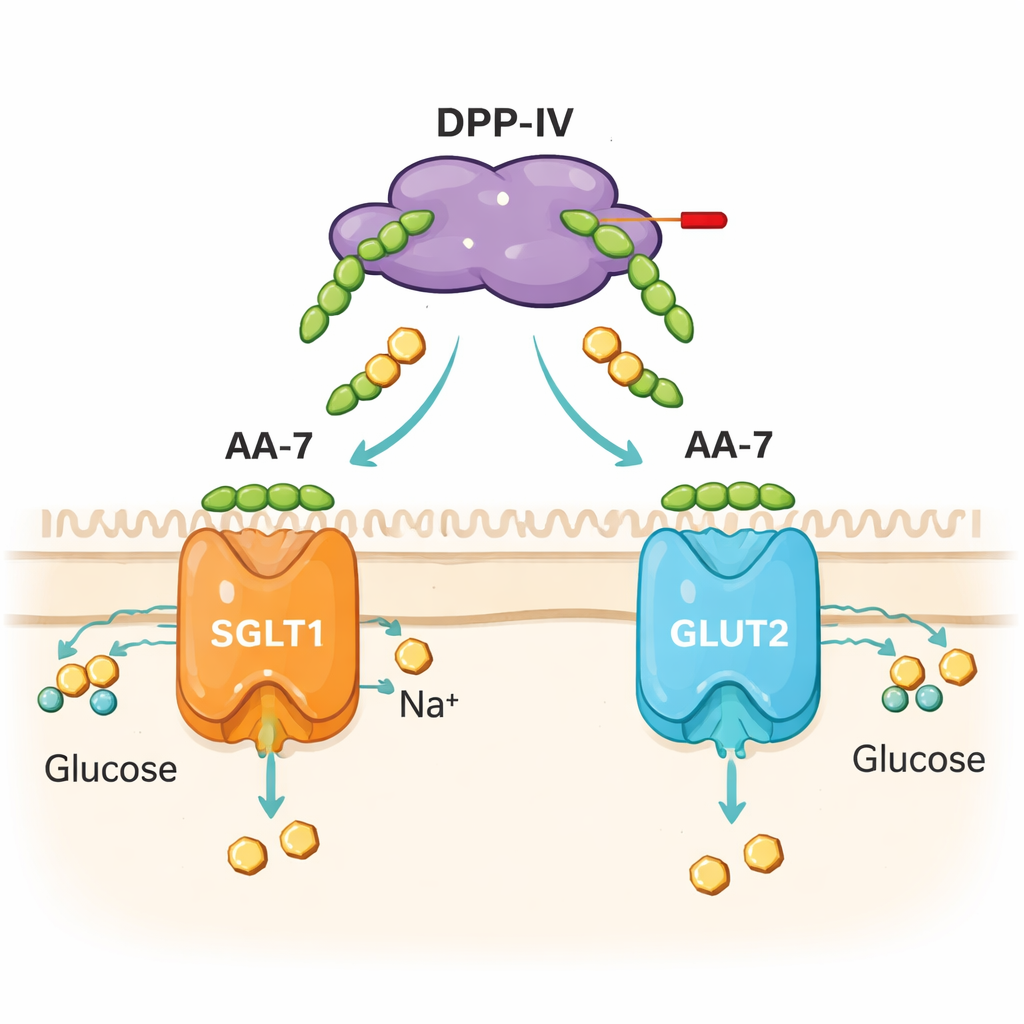
Cosa potrebbe significare per gli alimenti del futuro
Per un lettore non specialista, il messaggio principale è che il peptide del polline d’api AA-7 sembra agire su due fronti rilevanti per il diabete di tipo 2: rallenta un enzima chiave che degrada gli ormoni che stimolano l’insulina e influenza l’assorbimento del glucosio da parte delle cellule intestinali. Di per sé, AA-7 non è pronto per diventare un farmaco o un integratore, in parte perché potrebbe non essere assorbito in modo efficiente. Tuttavia indica che il polline d’api—e forse altri alimenti ricchi di proteine—potrebbero essere serbatoi di piccoli peptidi multitasking in grado di ispirare nuovi alimenti funzionali o terapie a base di peptidi. Con ulteriori studi su animali e esseri umani, e con modi migliori per somministrare tali peptidi, questo tipo di molecola ad azione duplice potrebbe entrare a far parte di un approccio più sfumato e informato dall’alimentazione per mantenere sotto controllo la glicemia.
Citazione: Mongkolnkrajang, U., Kuptawach, K., Sangtanoo, P. et al. Bee pollen-derived peptide with dual DPP-IV Inhibition and glucose transport modulation. Sci Rep 16, 7616 (2026). https://doi.org/10.1038/s41598-026-39009-1
Parole chiave: peptidi del polline d’api, inibizione DPP-IV, trasporto del glucosio, diabete di tipo 2, alimenti funzionali