Clear Sky Science · it
La modellazione basata sulla struttura rivela le basi molecolari della nuova attività di CYP153A6 verso i derivati del toluene
Affidare a natura i lavori chimici difficili
Chimici e industria si affidano a reazioni che introducono ossigeno in legami carbonio–idrogeno tenaci, per esempio per bonificare inquinanti o per costruire ingredienti per farmaci e fragranze. Eseguire queste trasformazioni in modo pulito, senza agenti chimici aggressivi o rifiuti di metalli pesanti, è difficile. Questo studio esamina un catalizzatore naturale, un enzima chiamato CYP153A6 proveniente da un batterio del suolo, e pone una domanda semplice ma dalle grandi implicazioni: è possibile indirizzare questo enzima a «migliorare» selettivamente i composti simili al toluene—componenti comuni di carburanti e solventi—trasformandoli in prodotti più utili e rispettosi dell’ambiente?
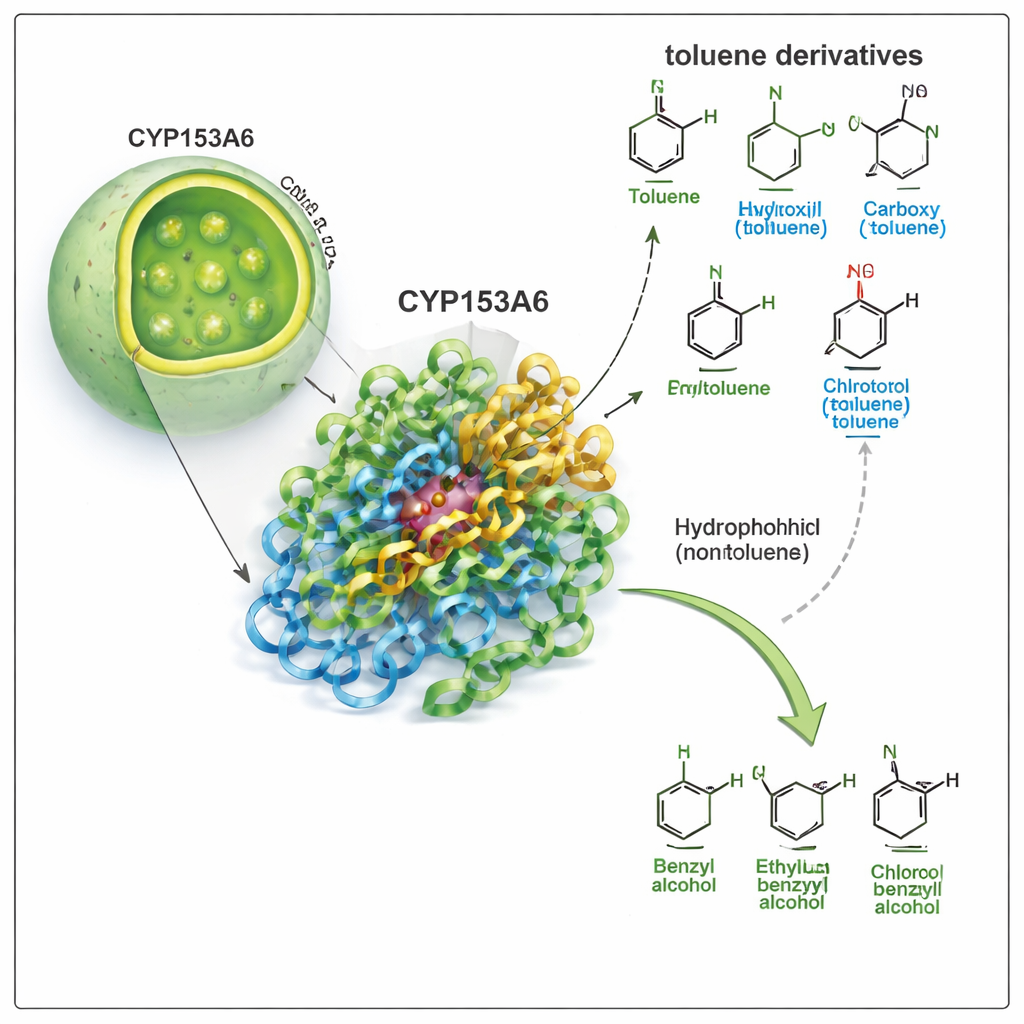
Un enzima che sceglie un singolo punto
CYP153A6 appartiene alla vasta famiglia dei citocromi P450, gli specialisti naturali delle ossidazioni. A differenza di molti catalizzatori industriali, questo enzima lavora in acqua, a temperature moderate, e seleziona posizioni molto specifiche su una molecola. Lavori precedenti avevano mostrato che CYP153A6 introduce ossigeno alle estremità di catene idrocarburiche semplici e su certi composti aromatici di origine vegetale. Qui gli autori indagano se può anche attaccare la posizione «benzylica»—la piccola catena laterale attaccata a un anello benzenico—nel toluene e nei composti correlati. Questa trasformazione converte i derivati del toluene in alcoli benzilici, preziosi mattoni per prodotti farmaceutici, aromi e chimica fine.
Mettere alla prova quali molecole piacciono all’enzima
Il gruppo ha prima condotto esperimenti di biotrasformazione usando cellule di E. coli ingegnerizzate che esprimono CYP153A6, sia come cellule intere sia come estratti cellulari. Hanno esposto l’enzima a un pannello di derivati del toluene, modificando il gruppo attaccato all’anello aromatico (come metile, cloro, metossile, idrossile o nitro) e la sua posizione (para, meta o orto). L’enzima ha dato ottime prestazioni su composti apolari o solo leggermente polari, come p-cimene, p-xilene, p-metilanisolo e p-clorotoluene, convertendo in modo consistente il gruppo metilico benzylico in un alcol benzilico. In modo sorprendente, ha completamente ignorato molecole più fortemente polari come p-cresolo, p-metilbenzilalcol e p-nitrotoluene, nonostante la somiglianza strutturale. Questo schema suggeriva che la tasca dell’enzima è fortemente idrofobica e sfavorevole verso gruppi polari.
Costruire una mappa 3D della macchina molecolare
Poiché la struttura tridimensionale di CYP153A6 non era stata risolta sperimentalmente, i ricercatori hanno costruito un modello computerizzato di alta qualità usando un P450 strettamente correlato di cui è nota la struttura. Hanno validato il modello controllandone la geometria e eseguendo lunghe simulazioni di dinamica molecolare per verificare la stabilità della proteina nel tempo, risultata soddisfacente. Le simulazioni hanno rivelato un sito attivo sepolto collegato all’esterno tramite tunnel stretti attraverso i quali i substrati entrano e i prodotti escono. Questi tunnel sono sagomati e regolati da loop flessibili sulla superficie proteica, aiutando a spiegare come l’enzima possa guidare molecole idrofobiche verso il centro reattivo a base di eme permettendo al contempo a acqua e prodotti ossidati di allontanarsi.
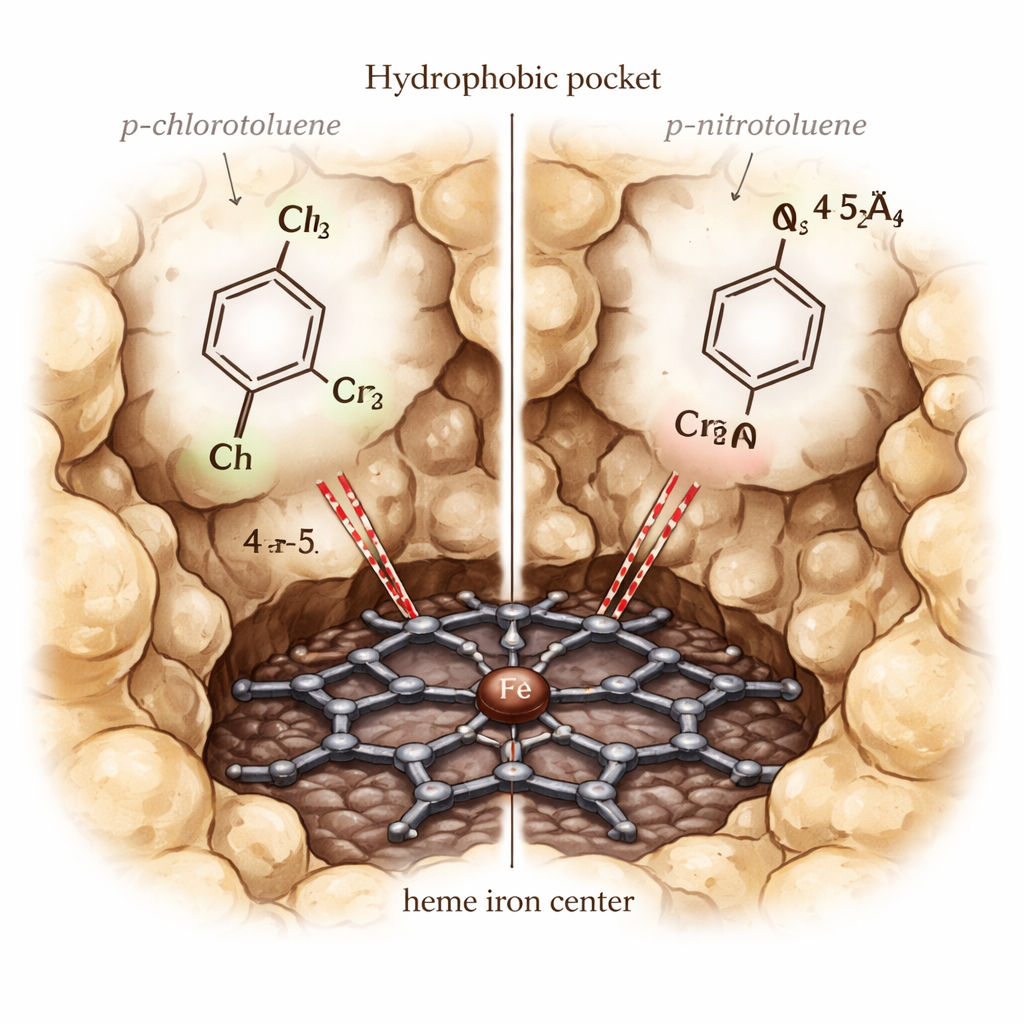
Osservare molecole che si legano, si muovono e reagiscono
Con il modello a disposizione, gli autori hanno simulato come diversi derivati del toluene si legano all’interno di CYP153A6. Hanno usato un approccio chiamato ensemble docking, provando molteplici forme proteiche leggermente diverse e diversi stati elettronici del ferro dell’eme, per identificare quali configurazioni distinguevano meglio i veri substrati dai non-substrati. Lo scenario vincente utilizzava il ferro nel suo stato ferrico di riposo e senza molecole d’acqua aggiuntive nella tasca, e favoriva correttamente i substrati noti. Simulazioni successive hanno seguito, fotogramma per fotogramma, come ogni molecola si posizionava rispetto all’eme. Buoni substrati come p-cimene e p-xilene rimanevano vicini al ferro con il loro gruppo metilico benzylico puntato verso di esso, e le loro energie di legame predette erano fortemente favorevoli. I substrati scadenti tendevano a allontanarsi, assumere orientamenti scomodi o interagire in modo sfavorevole con le catene laterali per lo più oleose che rivestono la tasca.
Perché un sosia reagisce e un altro no
Un enigma emerso è stato il comportamento diverso di due analoghi: p-clorotoluene viene ossidato efficacemente da CYP153A6, mentre p-nitrotoluene non lo è, pur potendo entrambi adattarsi alla tasca e legarsi con forza simile nelle simulazioni. Per risolvere la questione, gli autori hanno eseguito calcoli più dettagliati di tipo meccanica quantistica/meccanica molecolare (QM/MM) sullo stato altamente reattivo «Compound I» dell’enzima. Questi calcoli hanno mostrato che il gruppo nitro sottrae così tanta densità elettronica dal carbonio benzylico che quest’ultimo diventa molto difficile da ossidare, nonostante la vicinanza geometrica. Al contrario, il gruppo cloro consente una migliore comunicazione elettronica tra l’eme e il substrato, riflessa in una maggiore densità di spin sull’anello aromatico e sul gruppo metilico e in un allineamento più reattivo per il cruciale passaggio di astrazione dell’idrogeno.
Cosa significa per una chimica più pulita
In termini pratici, CYP153A6 si comporta come un piccolo guanto oleoso che tiene certi composti simili a carburanti nella posizione giusta affinché si possa aggiungere ossigeno in un punto specifico—trasformandoli in prodotti più solubili in acqua, utili e infine più degradabili. Lo studio mostra che l’enzima preferisce sostituenti non polari e che sia la forma sia il flusso elettronico determinano se un dato derivato del toluene verrà trasformato. Chiarendo come CYP153A6 riconosce e attiva queste molecole, il lavoro fornisce un progetto per ingegnerizzare versioni migliorate che potrebbero aiutare a bonificare inquinanti aromatici o a produrre composti complessi in modo più sostenibile.
Citazione: Wei, Y., Donzella, S., Foiadelli, S. et al. Structure-based modeling reveals molecular basis for CYP153A6’s novel activity toward toluene derivatives. Sci Rep 16, 7570 (2026). https://doi.org/10.1038/s41598-026-38986-7
Parole chiave: biocatalisi, citocromo P450, idrossilazione del toluene, ingegneria degli enzimi, chimica verde