Clear Sky Science · it
Sintesi di immagini pseudo-sane tramite modelli di diffusione guidati dalla localizzazione per la localizzazione di lesioni da displasia corticale focale
Perché individuare piccole cicatrici cerebrali è importante
Per molte persone con epilessia, le crisi continuano nonostante farmaci potenti. Un colpevole nascosto comune è una piccola area di tessuto cerebrale malformato chiamata displasia corticale focale. Queste aree possono spesso essere curate chirurgicamente—se i medici riescono a individuarle. Ma sulle scansioni cerebrali standard le lesioni possono essere così sottili che anche radiologi esperti le trascurano. Questo studio presenta una nuova tecnica di intelligenza artificiale (IA) che “immagina” come sarebbe la risonanza di una persona se fosse completamente sana, poi usa le differenze per rivelare lesioni difficili da vedere, aprendo potenzialmente la strada alla chirurgia per più pazienti.
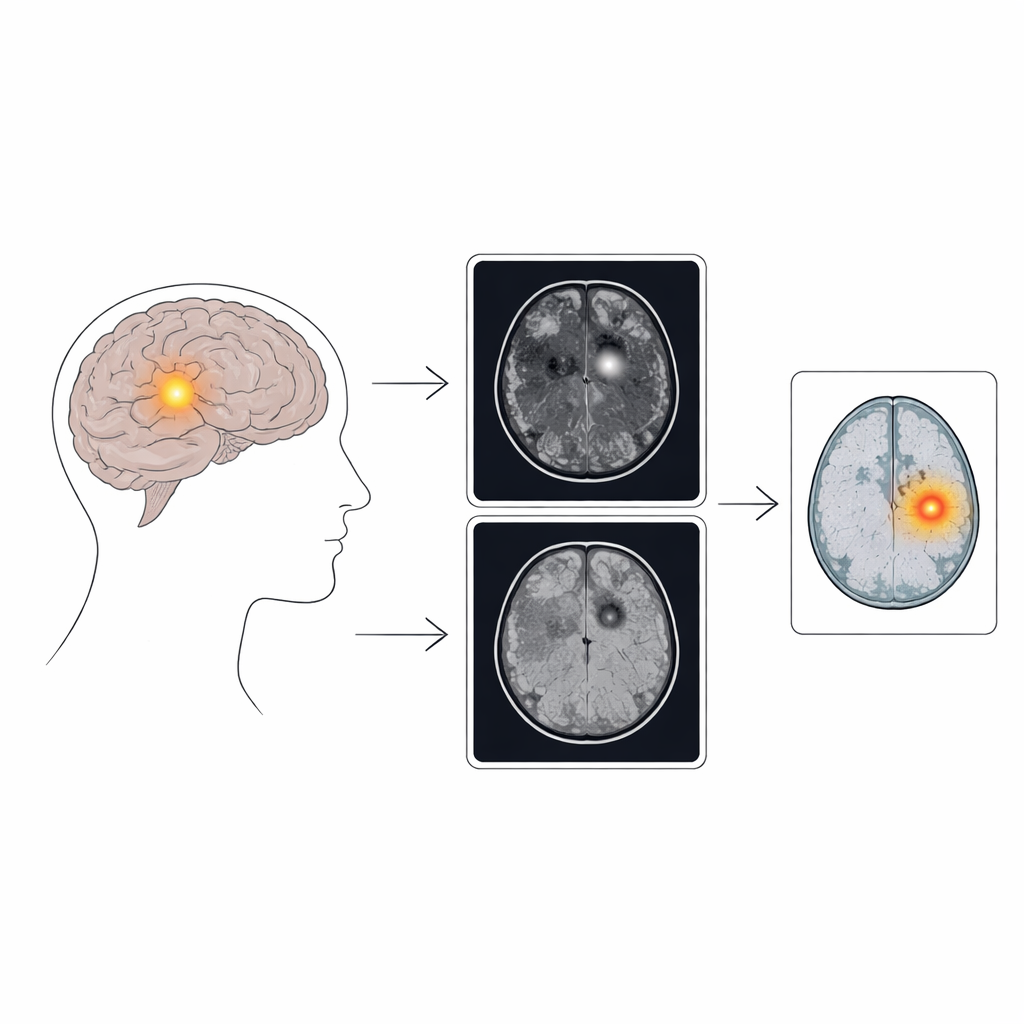
Piccoli punti problematici in un grande problema
L’epilessia colpisce più di 70 milioni di persone nel mondo, e circa un terzo continua ad avere crisi anche dopo aver provato diversi farmaci. Nei bambini, una delle cause principali è la displasia corticale focale, in cui una piccola porzione di cervello si sviluppa in modo anomalo. Nelle scansioni MRI queste aree possono mostrare una corteccia leggermente ispessita o un bordo sfumato tra materia grigia e bianca—modifiche che possono essere estremamente facili da sottovalutare. Poiché etichettare queste delicate anomalie slice dopo slice è dispendioso in termini di tempo e incoerente tra gli ospedali, esistono pochi dataset ampi e ben annotati per addestrare gli strumenti IA supervisionati tradizionali. Gli autori si sono quindi concentrati sul rilevamento di anomalie debolmente supervisionato, un approccio che apprende i modelli del tessuto normale e segnala tutto ciò che appare fuori posto, senza richiedere contorni manuali dettagliati di ogni lesione.
Un’IA che chiede: come apparirebbe un cervello sano?
L’idea centrale del metodo è generare una versione “pseudo-sana” della risonanza di un paziente e poi misurare come differisce dall’immagine reale. Per farlo, il gruppo si è basato sui modelli di diffusione, una classe potente di generatori di immagini che aggiungono rumore a un’immagine e poi imparano a invertire quel processo. In questo lavoro, il modello è addestrato a convertire un tipo di MRI (un’immagine T1-pesata, che evidenzia l’anatomia) in un altro tipo (una immagine FLAIR, particolarmente sensibile ad alcune caratteristiche delle lesioni). Durante il processo inverso, il modello viene spinto delicatamente a trasformare le regioni sospette in modo che somiglino a tessuto sano, lasciando sostanzialmente inalterate le aree normali. La differenza tra la scansione FLAIR originale e la FLAIR generata e “ripulita” diventa una mappa delle anomalie che evidenzia le probabili posizioni delle lesioni.
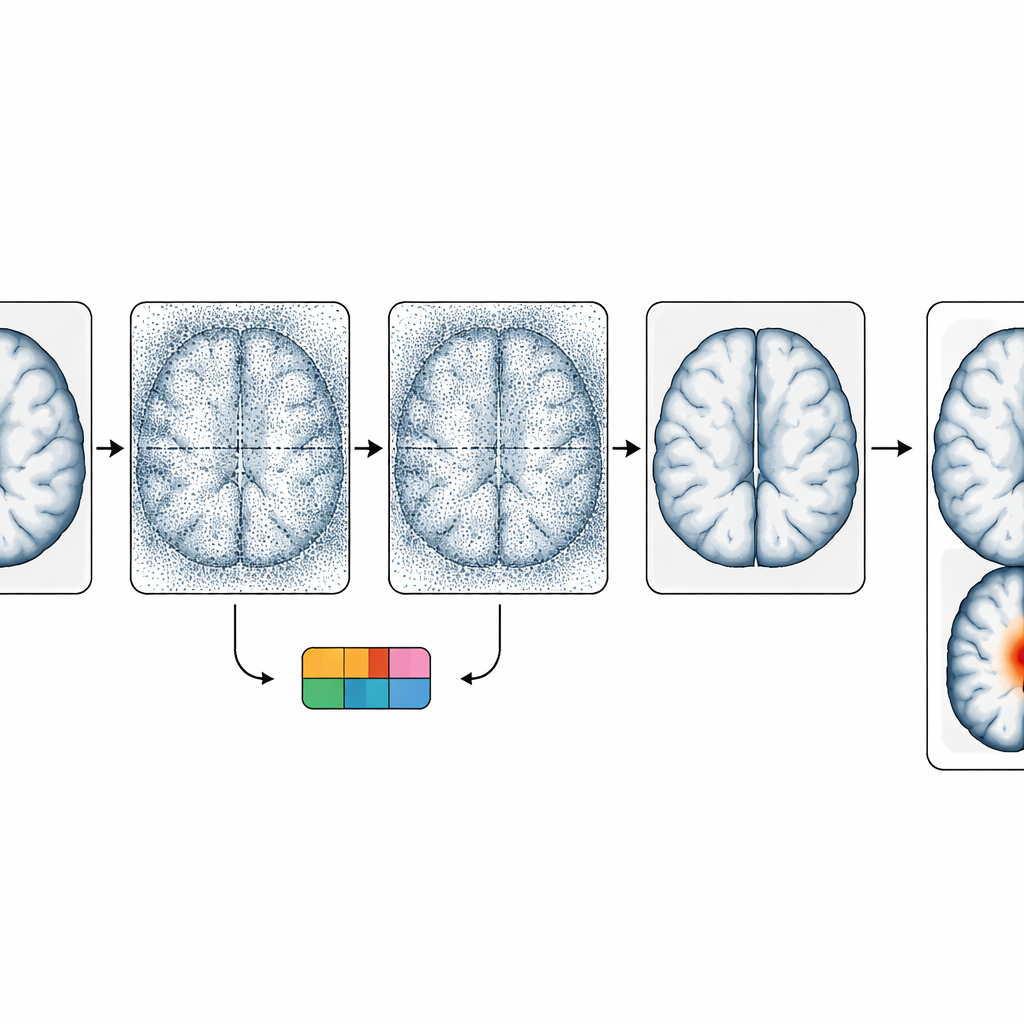
Usare due tipi di scansioni e suggerimenti di localizzazione approssimativi
Diverse sequenze MRI mostrano la displasia corticale focale in modi differenti. Le immagini T1 rivelano meglio i cambiamenti di forma nella corteccia, mentre le FLAIR tendono a rendere il tessuto anomalo, ricco d’acqua, più evidente con segnale più luminoso e confini sfumati. Gli autori sfruttano questa complementarità fornendo l’immagine T1 come guida durante la generazione della FLAIR, incoraggiando il modello a usare la struttura di una modalità e i cambiamenti di segnale dell’altra. Aggiungono anche una seconda fonte di guida: un classificatore addestrato a riconoscere quale ampia regione cerebrale (come il lobo frontale o temporale) contiene l’anomalia, o se la scansione è normale. Questa informazione regionale indirizza il processo di diffusione a concentrare i suoi sforzi di “guarigione” nelle aree dove le lesioni sono più probabili, migliorando le possibilità di rivelare piccoli focolai epilettici senza alterare fortemente l’intero cervello.
Correggere gli spostamenti di intensità e test su pazienti reali
I modelli generativi possono modificare sottigliezze come luminosità o contrasto dell’immagine, il che rischia di confondere i medici o nascondere vere anomalie. Per contrastare ciò, i ricercatori applicano l’histogram matching, una tecnica standard di elaborazione delle immagini che forza l’immagine FLAIR generata ad avere la stessa distribuzione di intensità complessiva della scansione originale. Questo mantiene l’aspetto familiare dell’immagine preservando le differenze locali introdotte dal modello relative alle lesioni. Il metodo è stato testato su un dataset pubblico dell’University Hospital Bonn, contenente risonanze di 85 pazienti con displasia corticale focale di tipo II e 85 controlli sani. Dopo un attento preprocessing e addestramento, il nuovo approccio ha superato quattro metodi concorrenti di rilevamento di anomalie, raggiungendo un’elevata recall a livello di immagine (trovando lesioni nella maggior parte delle scansioni affette) e una migliore corrispondenza con le mappe delle lesioni annotate dagli esperti a livello di pixel.
Cosa potrebbe significare per le persone con epilessia
Lo studio mostra che l’IA può essere utilizzata non solo per classificare le scansioni cerebrali, ma per generare immagini realistiche del tipo “e se fosse sana?” che fanno emergere lesioni nascoste. Senza richiedere etichette dispendiose voxel per voxel, il metodo combina MRI multimodale, suggerimenti di posizione approssimativi e una corretta correzione delle intensità per rilevare cicatrici epilettiche sottili in modo più affidabile rispetto ad alcuni strumenti esistenti. Pur non essendo perfetto—le differenze tra i tipi di scansione possono ancora introdurre falsi allarmi e alcune lesioni possono restare troppo simili al tessuto normale—l’approccio avvicina il campo a un supporto automatizzato e affidabile per i radiologi. Sul lungo periodo, tali tecniche potrebbero aiutare a identificare bersagli chirurgici prima e in modo più coerente, migliorando gli esiti per le persone con epilessia farmacoresistente.
Citazione: Li, Y., Pan, Y., Zhang, X. et al. Pseudo-healthy image synthesis via location-guided diffusion models for focal cortical dysplasia lesion localization. Sci Rep 16, 8101 (2026). https://doi.org/10.1038/s41598-026-38981-y
Parole chiave: epilessia, risonanza magnetica cerebrale, displasia corticale focale, IA per imaging medico, rilevamento di anomalie