Clear Sky Science · it
Un nuovo asse regolatorio C/EBPα–miR-335-5p–PRKAA2 guida l’accumulo lipidico epatico nella MASLD
Perché la steatosi epatica è importante
Molte persone che consumano pochissimo alcool sviluppano comunque un «fegato grasso», una condizione oggi denominata steatosi epatica associata a disfunzione metabolica (MASLD). È strettamente collegata all’obesità e al diabete di tipo 2 e può progredire silenziosamente verso la fibrosi epatica, la cirrosi e persino il cancro del fegato. Questo studio pone una domanda semplice ma cruciale: cosa succede dentro le cellule del fegato che le porta a immagazzinare così tanto grasso, e possiamo individuare un interruttore molecolare che, se spento, protegga l’organo?
Una reazione a catena nascosta nelle cellule epatiche
I ricercatori si sono concentrati su una reazione a catena molecolare che collega dieta e metabolismo all’accumulo di lipidi nel fegato. Hanno studiato topi alimentati con una dieta ad alto contenuto di grassi e cellule epatiche coltivate immerse in acidi grassi per simulare la MASLD. In questi modelli, gli animali aumentavano di peso, i lipidi ematici salivano e i loro fegati si riempivano di goccioline oleose, riproducendo caratteristiche chiave del fegato grasso umano. All’interno di questi fegati steatosici, il gruppo ha osservato che un particolare regolatore genetico, un fattore di trascrizione chiamato C/EBPα, e una piccola molecola di RNA, miR‑335‑5p, erano entrambi aumentati, mentre una subunità enzimatica protettiva denominata PRKAA2, parte del noto sensore energetico AMPK, risultava diminuita.
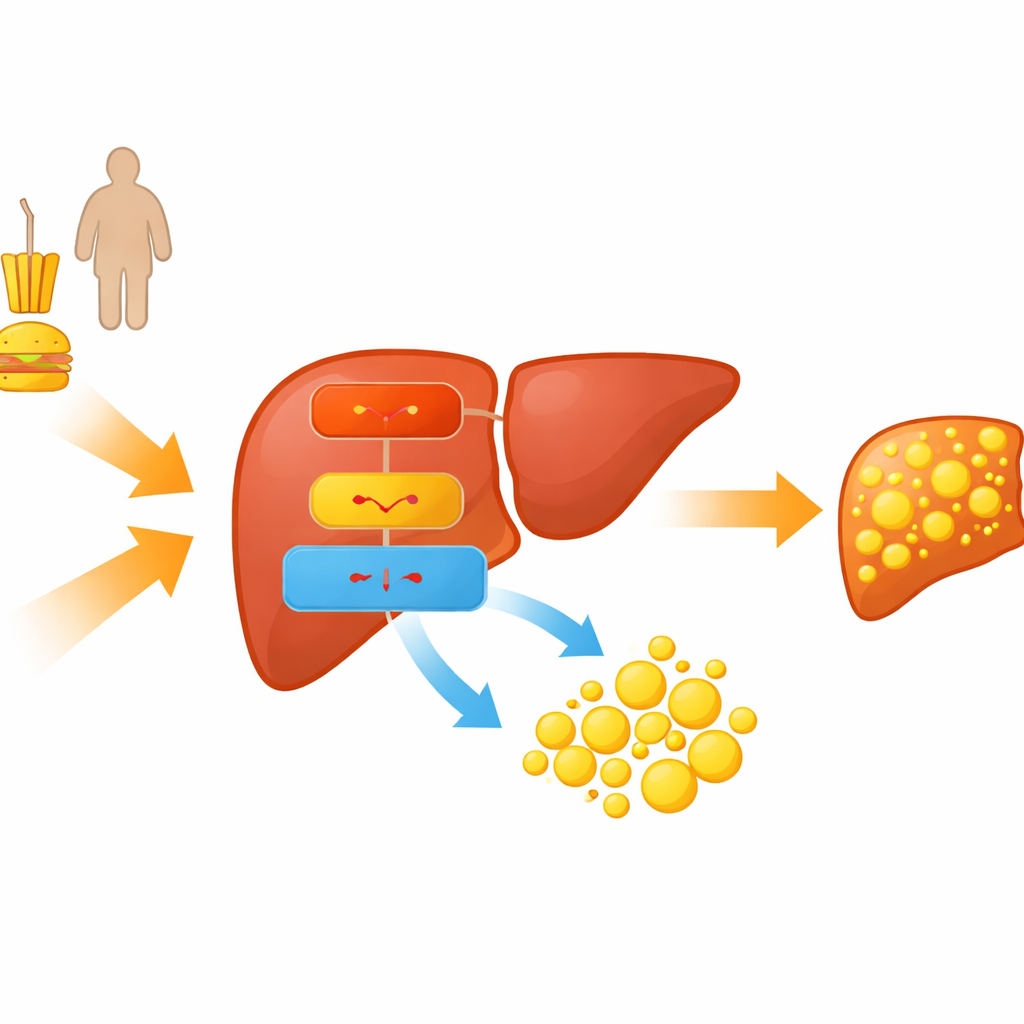
Come un piccolo RNA sposta l’equilibrio verso il grasso
Le piccole molecole di RNA chiamate microRNA agiscono come dimmer molecolari, attenuando l’espressione di geni specifici. Il gruppo ha dimostrato che miR‑335‑5p si lega direttamente al messaggio che codifica PRKAA2 e impedisce alla cellula di sintetizzare questa proteina. PRKAA2 contribuisce all’assemblaggio del complesso AMPK, che normalmente rileva il basso livello energetico e risponde frenando la sintesi lipidica e promuovendo la combustione dei grassi. Quando i livelli di miR‑335‑5p venivano aumentati artificialmente nelle cellule epatiche, i livelli di PRKAA2 calavano, l’attività di AMPK diminuiva e le proteine che favoriscono la lipogenesi aumentavano, portando a visibili accumuli di goccioline lipidiche. Quando miR‑335‑5p veniva bloccato, si osservava l’effetto opposto: PRKAA2 e l’attività di AMPK aumentavano e l’accumulo di lipidi diminuiva.
Il commutatore maestro che avvia la cascata
Cosa attiva inizialmente miR‑335‑5p? Analizzando la sequenza di DNA che controlla questo microRNA, gli scienziati hanno previsto diversi possibili interruttori principali e si sono concentrati su C/EBPα, già noto per influenzare la gestione dei grassi e degli zuccheri. Hanno confermato che C/EBPα si lega direttamente alla regione di controllo di miR‑335‑5p e ne aumenta l’attività. L’aumento di C/EBPα nelle cellule epatiche elevava i livelli di miR‑335‑5p, riduceva PRKAA2, indeboliva la segnalazione AMPK e favoriva l’accumulo lipidico. Il silenziamento di C/EBPα produceva l’effetto opposto, rafforzando il «freno» del rilevatore energetico della cellula e riducendo i lipidi. Esperimenti di rescue, in cui miR‑335‑5p veniva bloccato o PRKAA2 ripristinato, hanno mostrato che gran parte dell’effetto promuovi‑grasso di C/EBPα passa attraverso questa singola catena.
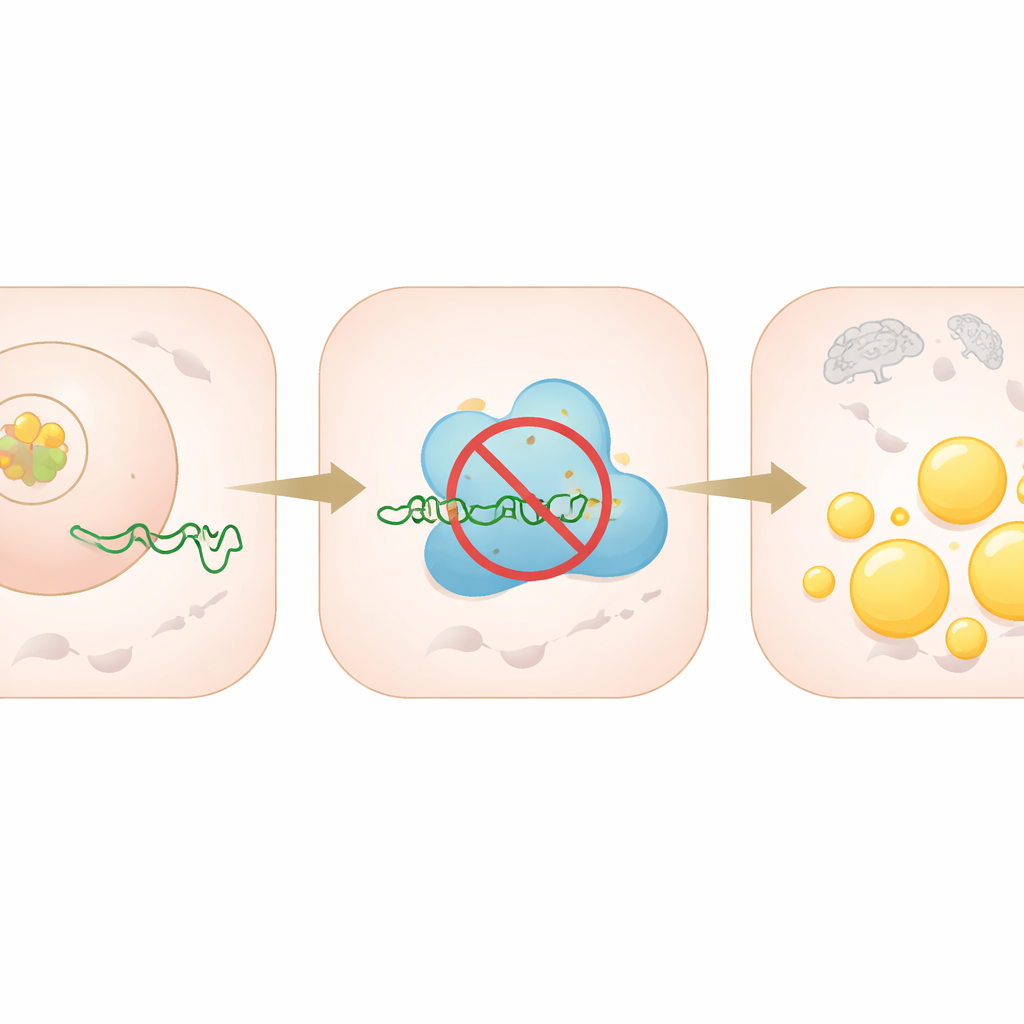
Dalle colture cellulari ai topi vivi
Per verificare se questa via avesse rilevanza negli organismi viventi, i ricercatori hanno usato virus ingegnerizzati per consegnare strumenti genetici direttamente ai fegati di topi nutriti con dieta ricca di grassi. Uno strumento riduceva i livelli di C/EBPα; un altro assorbiva l’eccesso di miR‑335‑5p. In entrambi i casi, i fegati degli animali contenevano meno grasso, l’aspetto microscopico migliorava e PRKAA2 e l’attività di AMPK rimbalzavano, mentre le proteine che guidano la sintesi lipidica diminuivano. Questi risultati in vivo concordavano con quelli delle colture cellulari e sottolineavano che la catena C/EBPα–miR‑335‑5p–PRKAA2 non è una curiosità da laboratorio, ma un potente motore della steatosi epatica in un organismo vivente.
Cosa significa per i trattamenti futuri
In termini semplici, lo studio rivela una staffetta molecolare in tre passaggi che induce le cellule del fegato ad accumulare grasso: C/EBPα attiva miR‑335‑5p, che a sua volta spegne PRKAA2 e indebolisce AMPK, il freno energetico della cellula. Con quel freno disattivato, la macchina della sintesi lipidica funziona senza controllo e il fegato si riempie di lipidi. Interrompere qualsiasi anello di questa catena — attenuare C/EBPα, bloccare miR‑335‑5p o potenziare PRKAA2/AMPK — ha ridotto il grasso nei fegati dei topi. Pur rimanendo molto lavoro da fare prima che tali strategie possano essere impiegate in sicurezza negli esseri umani, questa via offre un bersaglio chiaro e verificabile per farmaci futuri volti a rallentare o invertire la MASLD.
Citazione: Zeng, X., Xu, Y., You, S. et al. A novel C/EBPα–miR-335-5p–PRKAA2 regulatory axis drives hepatic lipid accumulation in MASLD. Sci Rep 16, 9255 (2026). https://doi.org/10.1038/s41598-026-38918-5
Parole chiave: steatosi epatica, microRNA, AMPK, metabolismo dei lipidi, malattia metabolica