Clear Sky Science · it
Microbiota intestinale e profili dei percorsi metabolici in pazienti con trapianto di cuore infetti e non infetti prima e dopo l’intervento
Perché il tuo intestino conta dopo un nuovo cuore
Il trapianto di cuore può offrire una seconda possibilità di vita alle persone con insufficienza cardiaca grave, ma le infezioni nelle settimane successive all’intervento restano una minaccia importante. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni: come cambia la comunità di microrganismi che vive nel nostro intestino — il microbiota — intorno al momento del trapianto di cuore, e tali cambiamenti possono aiutare a spiegare chi sviluppa infezioni e chi no?
Il minuscolo ecosistema nei pazienti trapiantati
I nostri intestini ospitano trilioni di batteri che aiutano a digerire il cibo, addestrano il sistema immunitario e respingono i germi invasori. L’intervento chirurgico, potenti farmaci immunosoppressori e antibiotici ad ampio spettro possono tutti sconvolgere questo fragile ecosistema. Per tracciare cosa accade nei pazienti sottoposti a trapianto cardiaco, i ricercatori in Cina hanno seguito 20 adulti riceventi un cuore donato. Hanno raccolto campioni di feci circa una settimana prima dell’intervento e di nuovo 30 giorni dopo, quindi hanno usato il sequenziamento del DNA per catalogare i batteri presenti e strumenti informatici per prevedere cosa quei microbi potrebbero fare a livello metabolico.
Quattro gruppi di pazienti, quattro modelli microbici
Il team ha diviso i pazienti in quattro gruppi: con e senza infezioni prima dell’intervento e con e senza infezioni nel primo mese dopo l’intervento. Prima del trapianto, la diversità complessiva e la struttura del microbiota intestinale apparivano sorprendentemente simili sia nei pazienti con che in quelli senza infezione. Le persone senza infezioni pre-operatorie erano per lo più colonizzate da un genere familiare chiamato Bacteroides, spesso associato a uno stato di salute intestinale stabile. Al contrario, i pazienti infetti mostravano una composizione mista che includeva il potenzialmente dannoso Enterococcus casseliflavus insieme a batteri spesso considerati favorevoli, come Limosilactobacillus e Weissella cibaria, suggerendo una comunità intestinale in un equilibrio delicato e instabile.
Dopo l’intervento: una biforcazione nel mondo microbico
A 30 giorni dall’operazione, il microbiota dei pazienti che avevano evitato l’infezione mostrava un modello riconoscibile, mentre quelli che avevano sviluppato infezioni apparivano molto diversi. I pazienti non infetti avevano comunità microbiche più ricche e uniformi, con molti membri di un genere chiamato Blautia e batteri correlati che producono butirrato, un acido grasso a corta catena noto per nutrire le cellule intestinali e sostenere la stabilità immunitaria. I loro ecosistemi intestinali apparivano diversi ed equilibrati. Nei pazienti che hanno sofferto di infezioni, invece, la diversità è diminuita e la comunità era dominata da Enterococcus faecium, un batterio resistente spesso riscontrato nelle infezioni nosocomiali e noto per la resistenza agli antibiotici. Le analisi statistiche hanno mostrato che i microbi di questo gruppo infetto si raggruppavano separatamente da tutti gli altri, indicando un chiaro caso di alterazione microbica post-operatoria, o disbiosi.
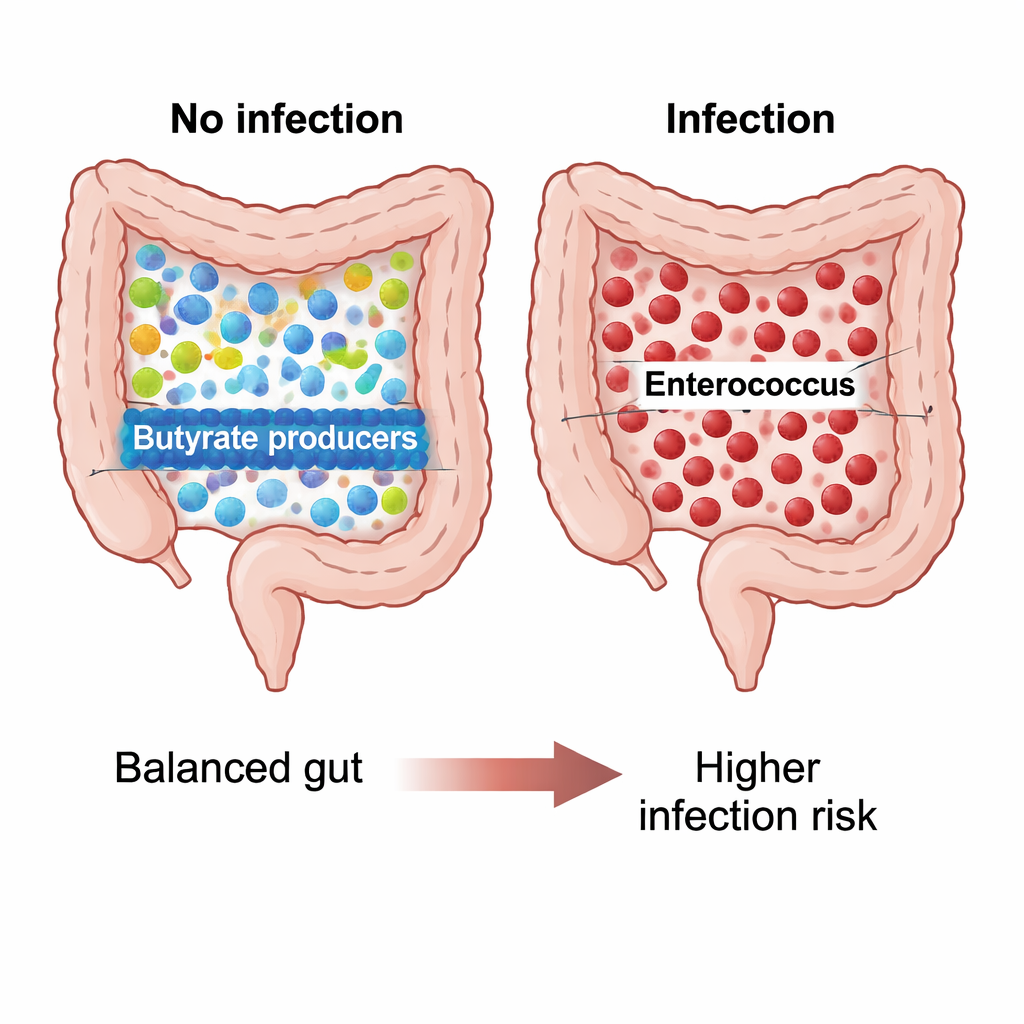
Chimica microbica collegata a protezione o rischio
I ricercatori hanno anche indagato quali tipi di attività chimiche questi microbi potrebbero svolgere. Usando software predittivi, hanno trovato che nel gruppo post-operatorio non infetto Blautia era correlata a vie che degradano un composto chiamato L-1,2-propandiolo, un intermedio nella fermentazione delle fibre che alimenta la produzione di acidi grassi benefici come il propionato. Nei pazienti infetti questo potenziale metabolico previsto era marcatamente inferiore, coerente con una comunità intestinale meno capace di produrre molecole protettive. Prima dell’intervento, Enterococcus casseliflavus nei pazienti infetti era associato a vie fermentative insolite che potrebbero riflettere un ambiente microbico stressato e affamato di energia, sebbene ciò richieda conferma diretta in laboratorio.
Cosa significa per i pazienti e i team di cura
Per le persone in attesa di un trapianto cardiaco, questi risultati suggeriscono che l’intestino non è un semplice spettatore; può contribuire a modellare il rischio di infezioni pericolose. Lo studio indica uno spostamento dinamico dalla dominanza di Bacteroides prima dell’intervento verso un arricchimento protettivo di Blautia o una sovracrescita dannosa di Enterococcus dopo l’intervento, a seconda di come procede il primo periodo di recupero. Lo stress legato alle infezioni e l’uso intensivo di antibiotici sembrano spingere la comunità intestinale verso lo stato a bassa diversità dominato da Enterococcus osservato nei pazienti infetti. Gli autori propongono una strategia “a doppio bersaglio”: favorire il ritorno dei batteri produttori di butirrato — forse tramite dieta o probiotici selezionati con cura — monitorando al contempo attentamente i livelli di Enterococcus. Pur richiedendo studi più ampi e di durata maggiore, questo lavoro apre la strada a una futura assistenza ai trapiantati in cui modulare il microbiota intestinale diventi parte integrante della protezione dei pazienti dalle infezioni potenzialmente letali.
Citazione: Han, J., Hua, L., Yang, B. et al. Gut microbiota and metabolic pathway profiles in infected and non-infected heart transplant patients before and after surgery. Sci Rep 16, 7697 (2026). https://doi.org/10.1038/s41598-026-38911-y
Parole chiave: trapianto di cuore, microbiota intestinale, infezione postoperatoria, antibiotici, batteri produttori di butirrato