Clear Sky Science · it
Determinanti a livello di residuo della stabilità termica dell’endolisina estremofila Ts2631
Perché i virus termofili sono importanti per i futuri antibiotici
Con l’aumento della resistenza agli antibiotici, gli scienziati sono in corsa per trovare nuovi modi per eliminare batteri pericolosi. Un approccio promettente prende in prestito armi da virus che infettano i batteri, chiamati batteriofagi. Questi virus producono enzimi, noti come endolisine, che perforano la parete cellulare batterica. Lo studio qui discusso si concentra su un’endolisina straordinariamente resistente al calore, Ts2631, proveniente da un virus che vive nelle sorgenti termali islandesi. Scoprendo quali singoli mattoni di questa proteina la rendono così stabile a temperature prossime all’ebollizione, i ricercatori sperano di progettare enzimi antibatterici più robusti e durevoli per la medicina e la biotecnologia. 
Uno strumento virale forgiato nelle sorgenti bollenti
Ts2631 proviene da un batteriofago che infetta il batterio termofilo Thermus scotoductus, che prospera in acque che raggiungono ben oltre i 60 °C. L’enzima Ts2631 taglia un legame specifico nel peptidoglicano, la maglia resistente che circonda le cellule batteriche. Ciò che distingue Ts2631 è la sua estrema termostabilità: rimane ripiegata fino a circa 100–105 °C, a seconda della soluzione. Questo è molto al di sopra delle temperature alle quali la maggior parte delle proteine si denatura. Gli autori hanno confrontato Ts2631 con il suo parente più studiato, la lisozima T7 di un virus di temperatura moderata, per capire quali stratagemmi strutturali la natura ha usato per mantenere Ts2631 integra in condizioni così estreme.
Loop più corti e una diversa miscela di mattoni
Le proteine sono catene di 20 tipi di aminoacidi, ripiegate in forme complesse. Quando i ricercatori hanno sovrapposto le strutture 3D di Ts2631 e della lisozima T7, hanno scoperto che l’architettura generale è molto simile: entrambe possiedono un nucleo compatto di eliche e foglietti. La differenza chiave risiede nelle regioni a loop flessibili che collegano questi elementi. In Ts2631 questi loop sono più corti e mostrano minore flessibilità, mentre la lisozima T7 ha loop più lunghi e più molli. Ts2631 presenta inoltre una maggiore presenza di alcuni aminoacidi spesso legati alla resistenza al calore: la rigida prolina; residui aromatici come tirosina e triptofano; e l’arginina carica positivamente. Allo stesso tempo contiene meno residui di serina, acido aspartico e acido glutammico, che possono rendere le proteine più vulnerabili ad alte temperature. Questo schema non vale solo rispetto alla lisozima T7, ma anche quando Ts2631 viene confrontata con centinaia di migliaia di proteine virali e con milioni di proteine batteriche.
Sostituire singoli aminoacidi per testarene l’importanza
Per passare dalle correlazioni alla causalità, il team ha sostituito sistematicamente 55 singoli aminoacidi in Ts2631 e ha misurato come ciascuna mutazione ha influenzato la temperatura di fusione (Tm) e la capacità dell’enzima di degradare la parete cellulare batterica. Alcune modifiche intorno al sito attivo contenente zinco sono risultate particolarmente dannose. Quando sono stati alterati tre residui che coordinano lo zinco (H30, H131 e C139), la Tm della proteina è diminuita fino a circa 20 °C e l’attività è andata persa. Due tirosine conservate (Y60 e Y69) hanno contribuito anch’esse alla stabilità. Sorprendentemente, rimuovere un ponte disolfuro — un tipo di legame covalente tra le cisteine C80 e C90 — ha effettivamente aumentato la temperatura di fusione, sebbene abbia distrutto l’attività. Questo mostra che essere molto stabile in provetta non significa sempre che una proteina funzionerà meglio in condizioni reali. 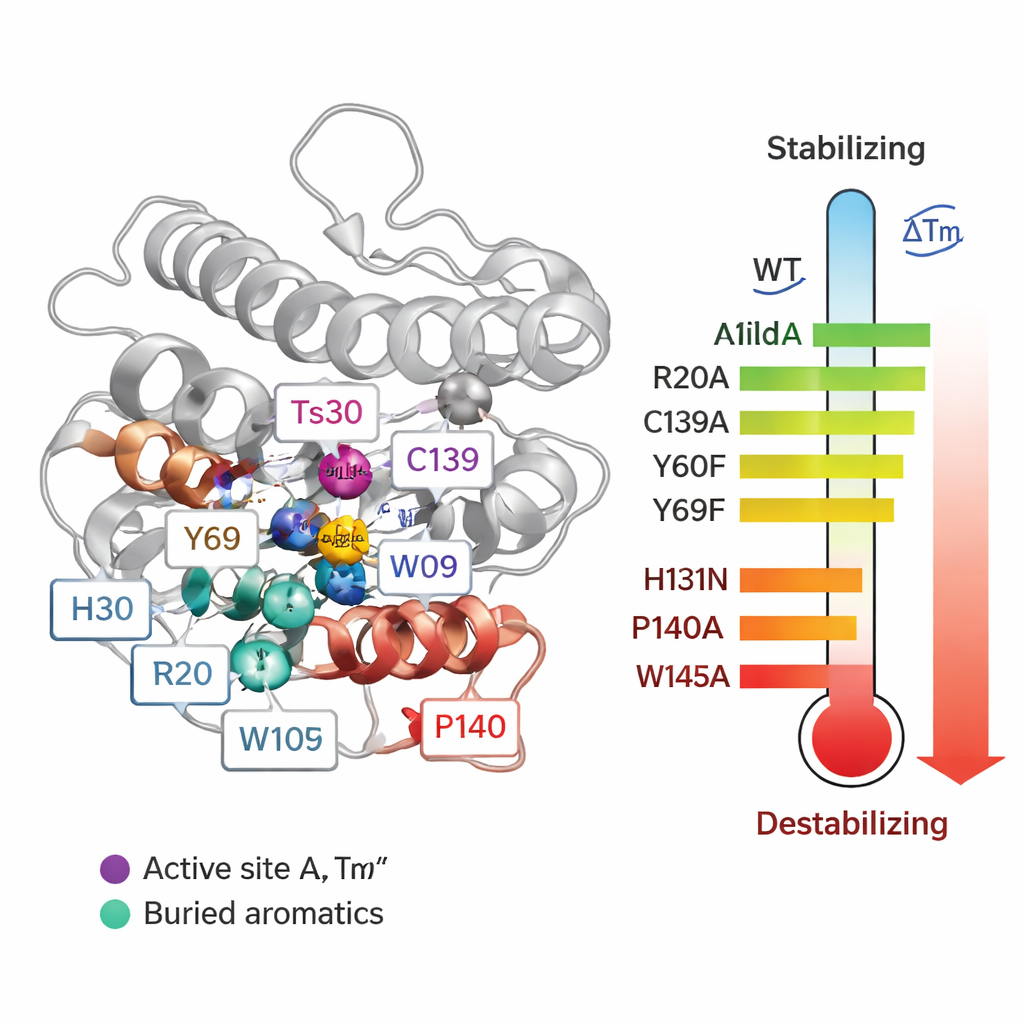
“Ancora” aromatiche nascoste e una presa chiave sulla parete batterica
I risultati più sorprendenti sono emersi dalle mutazioni di residui di prolina e triptofano. La sostituzione di una singola prolina (P140), situata immediatamente accanto alla cisteina legante lo zinco C139, ha ridotto la Tm di oltre 21 °C e ha indebolito l’attività dopo il riscaldamento, perché la mutazione ha perturbato una geometria di legame speciale necessaria per il corretto coordinamento del metallo. Diversi triptofani profondamente sepolti (W102, W109 e soprattutto W145) si sono rivelati anch’essi critici: sostituirli con alanina ha causato cali di Tm di 14–24 °C e ha reso l’enzima molto più sensibile al calore nei test di attività. Questi residui aromatici agiscono come ancore interne che bloccano il nucleo della proteina in posizione. Tra le arginine, la maggior parte ha avuto scarso effetto sulla stabilità, ma R20 è risultata essenziale per afferrare il peptidoglicano. Quando R20 è stata sostituita, l’enzima si è legato male alla parete cellulare batterica e ha perso attività al riscaldamento, rivelando che alcuni residui contribuiscono più alla funzione che alla sola robustezza termica.
Dalle enzimi delle sorgenti calde ad antibatterici più resistenti
Nel complesso, lo studio mostra che l’eccezionale resistenza al calore di Ts2631 si basa su una manciata di aminoacidi ben posizionati piuttosto che su un indurimento uniforme dell’intera proteina. I residui che legano lo zinco, una prolina conservata vicino al sito attivo e catene laterali aromatiche sepolte formano un nucleo stabilizzante, mentre alcune caratteristiche classiche di stabilizzazione, come i ponti disolfuro o i ponti salini, qui contano meno di quanto ci si potrebbe aspettare. Per il campo più ampio, questo lavoro suggerisce che le endolisine mesofile (di temperatura moderata) potrebbero essere rese più durevoli sostituendo con cura posizioni selezionate con triptofano o prolina senza sacrificare l’attività antibatterica. In altre parole, imparando come la natura costruisce enzimi che resistono a temperature prossime all’ebollizione, gli scienziati ottengono un progetto pratico per ingegnerizzare antibiotici a base proteica più affidabili e di lunga durata.
Citazione: Cieminska, K., Kaczorowska, AK., Kozlowski, L.P. et al. Residue-level determinants of the thermal stability of the extremophilic Ts2631 endolysin. Sci Rep 16, 7630 (2026). https://doi.org/10.1038/s41598-026-38786-z
Parole chiave: endolisina termostabile, enzimi di batteriofagi, termostabilità delle proteine, resistenza agli antibiotici, ingegneria delle proteine