Clear Sky Science · it
Studio sui biomarcatori della trasformazione indotta dall'omocisteina delle cellule muscolari lisce vascolari in cellule schiumose
Perché le arterie si otturano a partire da piccoli cambiamenti cellulari
L’aterosclerosi — l’ostruzione e l’indurimento lento delle arterie — è una delle principali cause di infarto e ictus. Si parla spesso di colesterolo e dieta, ma meno di come singole cellule della parete vascolare cambino durante lo sviluppo della malattia. Questo studio esamina da vicino uno di questi fattori scatenanti, una molecola ematica chiamata omocisteina, e mostra come possa spingere le cellule muscolari normalmente ben comportate nelle arterie a immagazzinare grasso e trasformarsi nelle cosiddette cellule schiumose, i mattoni delle placche pericolose.
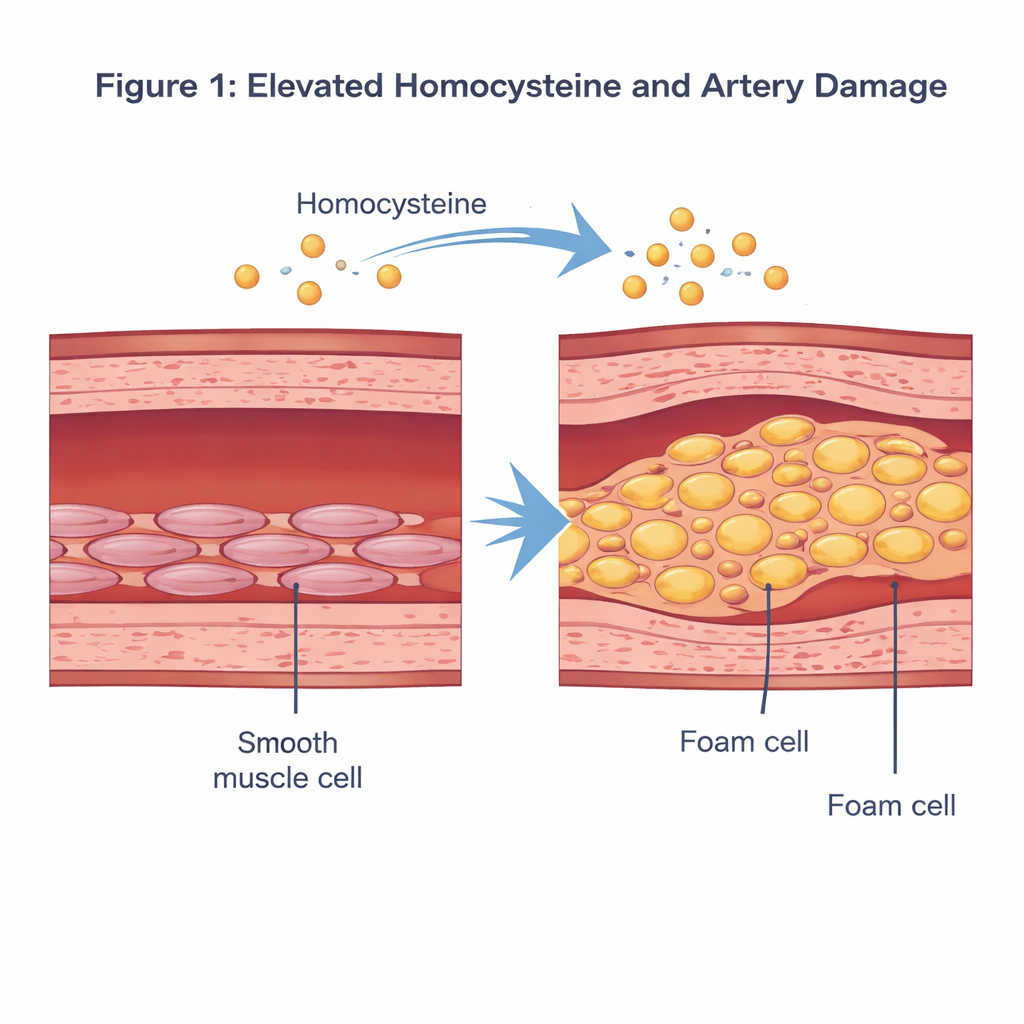
Un amminoacido guastafeste nel flusso sanguigno
L’omocisteina è un amminoacido contenente zolfo prodotto quando il nostro organismo metabolizza la metionina alimentare. In condizioni normali, la sua concentrazione nel sangue è bassa. Quando supera circa 15 micromoli per litro — una condizione chiamata iperomocisteinemia — studi epidemiologici l’hanno collegata a un rischio più elevato di malattie cardiovascolari. Ricerche precedenti suggerivano che l’eccesso di omocisteina può danneggiare il rivestimento interno delle arterie, scatenare infiammazione e alterare il comportamento delle cellule muscolari lisce vascolari, che si trovano nello strato medio della parete vascolare e contribuiscono a regolare la pressione sanguigna contraendosi e rilassandosi.
Come le cellule muscolari arteriose diventano cellule schiumose ricche di grasso
I ricercatori si sono concentrati su come l’omocisteina rimodelli queste cellule muscolari lisce. In coltura, hanno esposto cellule muscolari lisce vascolari umane a una dose di omocisteina pensata per imitare uno stato patologico e le hanno confrontate con cellule non trattate. Usando colorazioni standard e test biochimici, hanno osservato che le cellule trattate con omocisteina si riempivano di goccioline di grasso colorate di rosso e che i loro livelli di colesterolo e trigliceridi aumentavano notevolmente. Allo stesso tempo, i marker proteici della loro identità “contrattile” abituale diminuivano, mentre aumentavano i marker di uno stato più sintetico e promotore di placca. Messo insieme, questo quadro mostra che l’omocisteina può allontanare le cellule muscolari lisce dal loro ruolo normale verso un fenotipo simile a quello delle cellule schiumose, carico di lipidi, che contribuisce direttamente alla formazione della placca.
Alla ricerca delle impronte molecolari all’interno delle cellule
Per capire quali proteine cambiano durante questa trasformazione, il gruppo ha utilizzato la proteomica moderna, una tecnologia che può misurare migliaia di proteine contemporaneamente. Hanno confrontato i livelli proteici nelle cellule trattate con omocisteina rispetto ai controlli e hanno quantificato in modo affidabile quasi 4.800 proteine. Tra queste, 54 sono emerse come significativamente alterate: 13 aumentate e 41 diminuite. Molte delle proteine in cambiamento sono coinvolte nella gestione dei lipidi, nella sopravvivenza cellulare, nello stress ossidativo e nel rimodellamento strutturale delle cellule. Gli autori hanno poi usato strumenti bioinformatici per raggruppare queste proteine in percorsi funzionali e mappare le loro interazioni reciproche, evidenziando reti connesse al metabolismo del colesterolo e alle risposte allo stress nella parete vascolare.
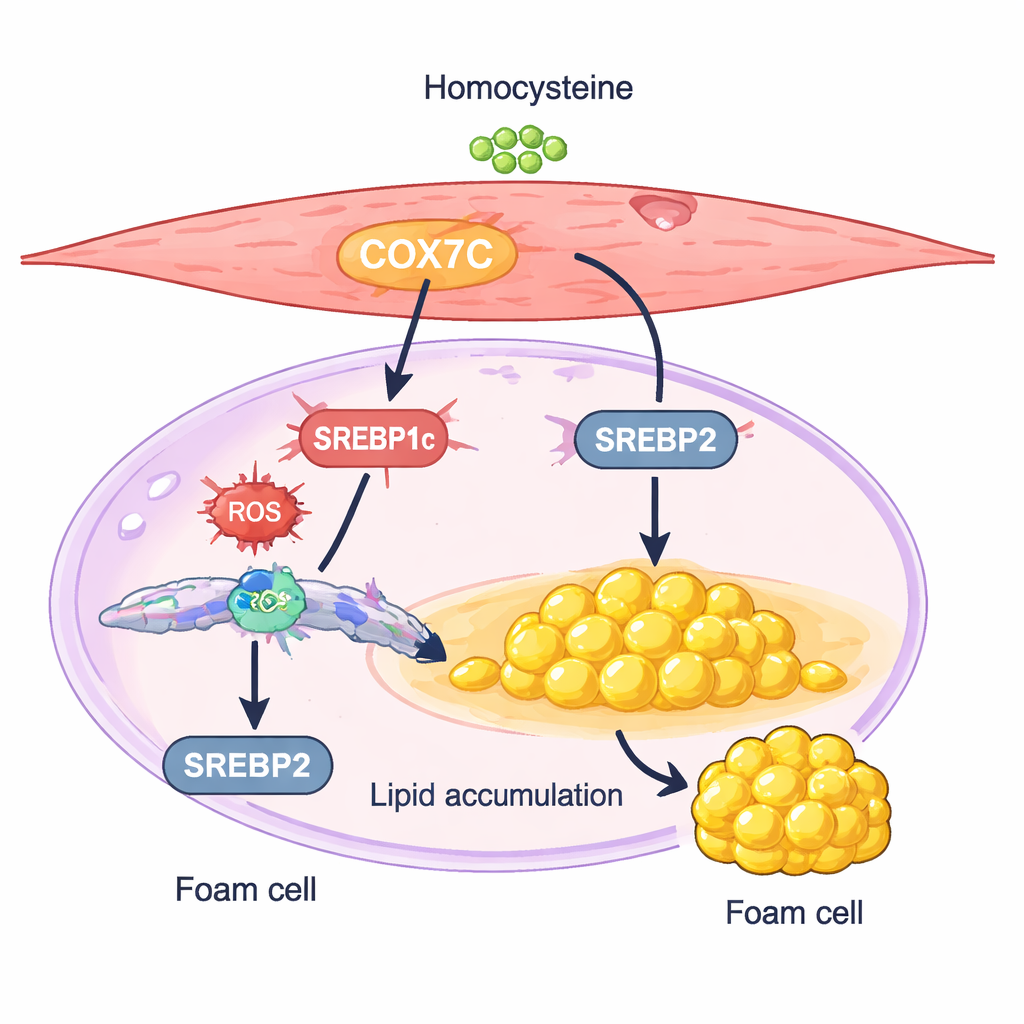
Un interruttore mitocondriale che spinge le cellule a immagazzinare grasso
Una proteina, chiamata COX7C, è emersa come un sospetto particolarmente interessante. COX7C è una componente delle centrali energetiche della cellula, i mitocondri, dove contribuisce a gestire la produzione di energia. Nelle cellule muscolari lisce trattate con omocisteina, i livelli di COX7C erano più alti rispetto ai controlli. I ricercatori hanno mostrato che aumentare ulteriormente COX7C induceva le cellule ad accumulare ancora più grasso ed esprimere livelli più elevati di due regolatori principali della produzione lipidica, SREBP1c e SREBP2. Silenziare COX7C aveva l’effetto opposto: attenuava l’attività delle SREBP, riduceva l’accumulo di colesterolo e trigliceridi e mitigava i cambiamenti simili a quelli delle cellule schiumose. Questi risultati sostengono un modello in cui l’omocisteina aumenta COX7C nei mitocondri, intensifica i segnali di stress cellulare e, a sua volta, attiva la sintesi lipidica guidata dalle SREBP, spingendo le cellule muscolari lisce verso uno stato di accumulo di lipidi.
Cosa significa per la salute del cuore e per terapie future
Questo lavoro non dimostra ancora quello che accade nelle arterie umane ed è stato condotto in cellule coltivate anziché in pazienti. Tuttavia fornisce uno sguardo dettagliato su come l’aumento dell’omocisteina possa contribuire a convertire cellule muscolari arteriose utili in cellule schiumose dannose, e individua COX7C e proteine correlate come potenziali biomarcatori o bersagli farmacologici. Per il lettore non specialista, il messaggio chiave è che oltre al “colesterolo buono” e “cattivo”, piccole variazioni nella chimica del sangue — come l’eccesso di omocisteina — possono riprogrammare la parete vascolare dall’interno. Identificando attori molecolari come COX7C e la via SREBP, questo studio pone le basi per strategie future volte a fermare la formazione delle placche, impedendo alle cellule arteriose di trasformarsi in piccoli depositi di grasso.»
Citazione: Wang, X., Ma, X., Zhang, X. et al. Study on biomarkers of homocysteine-induced transformation of vascular smooth muscle cells into foam cells. Sci Rep 16, 7411 (2026). https://doi.org/10.1038/s41598-026-38763-6
Parole chiave: aterosclerosi, omocisteina, cellule schiumose, cellule muscolari lisce vascolari, COX7C