Clear Sky Science · it
ConvAHKG: grafo di conoscenza ibrido basato sulle azioni con approccio convoluzionale a doppio canale per il riposizionamento dei farmaci
Trovare nuovi usi per farmaci esistenti
Portare un nuovo farmaco sul mercato può richiedere più di un decennio e costare miliardi di dollari, e molti candidati falliscono lungo il percorso. Questo studio esplora una scorciatoia più intelligente: usare dati e intelligenza artificiale per scoprire nuove malattie che farmaci già approvati potrebbero trattare in sicurezza. Gli autori presentano un framework, chiamato ConvAHKG, che intreccia diversi tipi di informazioni biomediche in una singola mappa connessa e poi utilizza una rete neurale moderna per individuare abbinamenti promettenti tra farmaco e malattia—offrendo una via più rapida ed economica verso nuove terapie.
Una mappa ricca delle interazioni tra farmaci e malattie
Il nucleo di questo lavoro è un “grafo di conoscenza ibrido”, una mappa gigantesca che collega farmaci, malattie, proteine, effetti collaterali, strutture chimiche e vie biologiche. Invece di memorizzare solo semplici collegamenti sì/no (ad esempio, “il farmaco A cura la malattia B”), la mappa registra come un farmaco agisca su una proteina—se la attiva, la inibisce o si lega ad essa—and come le proteine siano coinvolte nelle malattie, per esempio come biomarcatori o mediante variazioni di attività. Il grafo contiene oltre 11.000 entità e 59 tipi di relazioni, incluse informazioni dettagliate su classificazioni dei farmaci, effetti collaterali, contatti proteina–proteina e sotto-strutture chimiche. Catturando questi molteplici strati di contesto, il grafo può riflettere una maggiore complessità biologica reale dietro gli effetti terapeutici e le reazioni avverse. 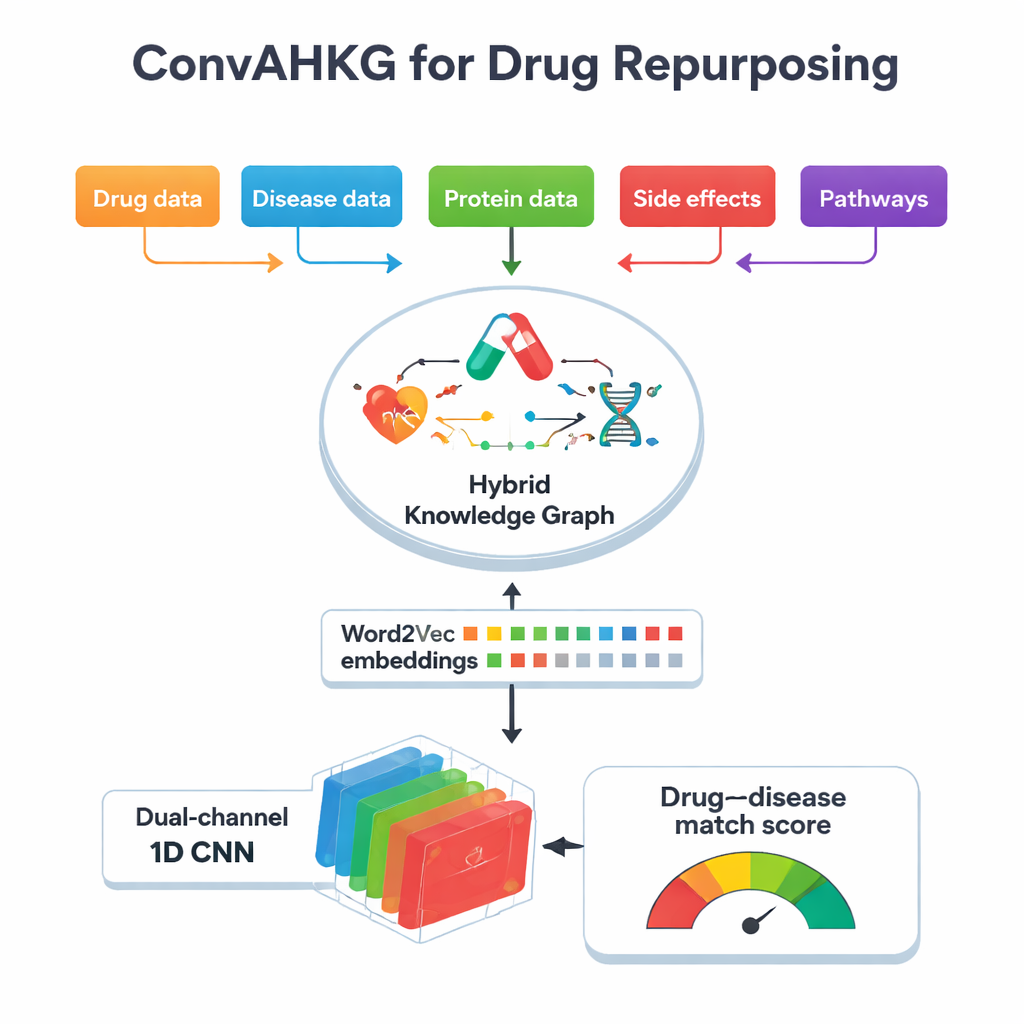
Insegnare al computer il linguaggio della biologia
Per rendere questa mappa complessa utilizzabile per l’apprendimento automatico, il team converte ogni connessione del grafo in una semplice “frase” in tre parti: una testa (per esempio una malattia), una relazione (per esempio biomarcatore) e una coda (per esempio una proteina). Applicano quindi Word2Vec, un metodo sviluppato originariamente per l’elaborazione del linguaggio naturale, per apprendere “embedding” numerici per ogni farmaco, malattia e proteina. Gli elementi che compaiono spesso insieme in queste frasi finiscono vicini nello spazio matematico, proprio come le parole con significati simili nel testo. Questo approccio è molto più semplice e veloce rispetto a molte tecniche di embedding specifiche per grafi, pur catturando pattern sottili. Nei test confrontati con diversi popolari metodi di embedding per grafi, Word2Vec ha eguagliato o superato il loro potere predittivo usando molto meno tempo di calcolo.
Un percorso neurale doppio per decisioni di trattamento sì/no
Una volta che ogni farmaco e ogni malattia sono tradotti in vettori numerici, ConvAHKG li alimenta in una rete neurale convoluzionale monodimensionale a doppio canale. Un canale elabora il vettore del farmaco e l’altro elabora il vettore della malattia usando una sequenza di filtri convoluzionali che rilevano pattern locali e motivi più ampi, ispirati a design provenienti dal riconoscimento delle immagini come InceptionNet e AlexNet. Dopo questo processo separato, i due flussi vengono uniti e passano attraverso diversi strati completamente connessi che producono una singola probabilità: questa coppia farmaco–malattia rappresenta un trattamento probabilmente efficace o piuttosto un effetto collaterale dannoso? Per gestire il fatto che le coppie positive note sono molto più rare di quelle negative, gli autori introducono una funzione di perdita pesata che penalizza maggiormente il mancato riconoscimento dei veri trattamenti, migliorando le prestazioni su questi casi difficili da trovare. 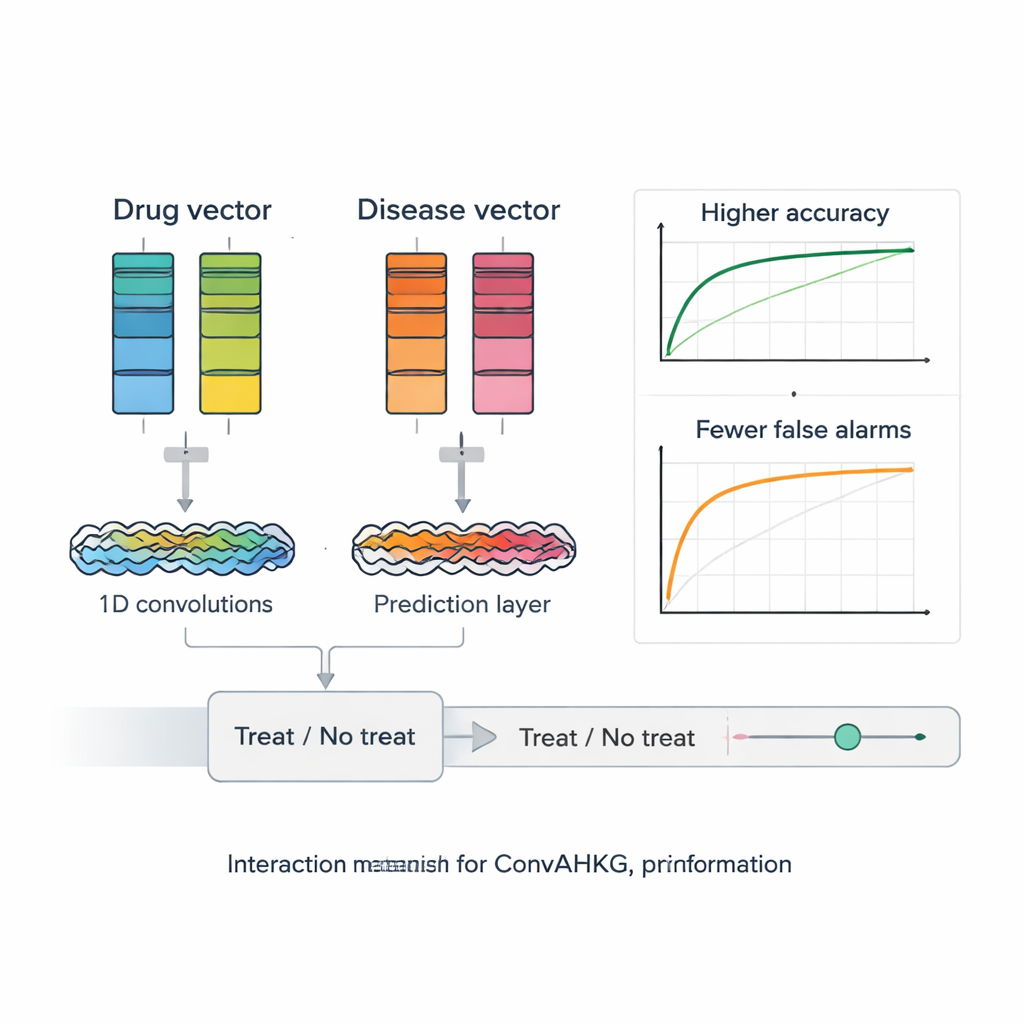
Sorpassare i metodi esistenti e individuare candidati per il cancro
I ricercatori testano rigorosamente il loro framework rispetto a diversi strumenti all’avanguardia per il riposizionamento dei farmaci che utilizzano fattorizzazione di matrici, reti neurali su grafi e autoencoder profondi. ConvAHKG raggiunge un’area sotto la curva ROC di 0,9836 e un’area sotto la curva precisione–richiamo di 0,9686, superando tutti gli approcci concorrenti sullo stesso dataset di benchmark. Applicano poi il modello al carcinoma polmonare non a piccole cellule, la forma più comune e letale di cancro polmonare a livello mondiale. ConvAHKG evidenzia diversi farmaci non precedentemente etichettati come trattamenti per questa malattia, inclusa l’anticorpo trastuzumab, che prende di mira la proteina HER2 e ha già evidenze cliniche a supporto nel cancro polmonare, così come altri agenti biologici e persino l’antibiotico classico benzilpenicillina. Simulazioni di docking suggeriscono che la benzilpenicillina possa legarsi con forza al DNA e alla topoisomerasi II alfa, un enzima spesso elevato in questi tumori, suggerendo un possibile meccanismo anticancro che merita ora verifiche sperimentali in laboratorio.
Perché questo è importante per i pazienti
In termini semplici, ConvAHKG agisce come un abile “sensale” altamente informato tra farmaci esistenti e malattie, usando una mappa dettagliata delle azioni biologiche e un potente motore di riconoscimento di pattern per prevedere quali vecchi medicinali potrebbero funzionare in nuovi contesti. Trattando i farmaci già testati per la sicurezza come blocchi riutilizzabili anziché strumenti a scopo unico, questo framework potrebbe accelerare la scoperta di terapie per condizioni come il cancro polmonare, specialmente dove lo sviluppo farmacologico convenzionale è troppo lento o costoso. Pur richiedendo ancora convalide sperimentali e cliniche accurate, lo studio mostra che combinare una ricca conoscenza biologica con l’intelligenza artificiale moderna può restringere drasticamente lo spazio di ricerca, rendendo più rapidamente accessibili trattamenti potenzialmente salvavita.
Citazione: Khodadadi AghGhaleh, M., Abedian, R., Zarghami, R. et al. ConvAHKG: Action-based hybrid knowledge graph with a dual-channel convolutional approach for drug repurposing. Sci Rep 16, 7592 (2026). https://doi.org/10.1038/s41598-026-38656-8
Parole chiave: riposizionamento dei farmaci, grafo di conoscenza, deep learning, cancro polmonare, scoperta di farmaci