Clear Sky Science · it
Trasferimento di protoni indotto dalla luce in acqua con strutture diverse: un approccio EPR per risolvere un problema classico
Perché importano i viaggi nascosti dei protoni
Ogni volta che respiri, pensi o converti la luce solare in energia utile in una cella solare, piccole particelle cariche positivamente chiamate protoni sono in movimento. Il modo in cui questi protoni si spostano attraverso l'acqua è un rompicapo vecchio di secoli, posto per la prima volta dallo scienziato Theodor Grotthuss nel 1806. Questo nuovo studio utilizza una combinazione ingegnosa di luce e misure magnetiche per osservare i protoni in acqua con strutture diverse, da soluzioni salate e affollate a miscele ghiacciate e vetrose e persino all'interno di una proteina di membrana. Il lavoro offre un modo inedito per mettere alla prova idee classiche sul moto dei protoni e per sondare ambienti difficili da studiare con altri metodi.
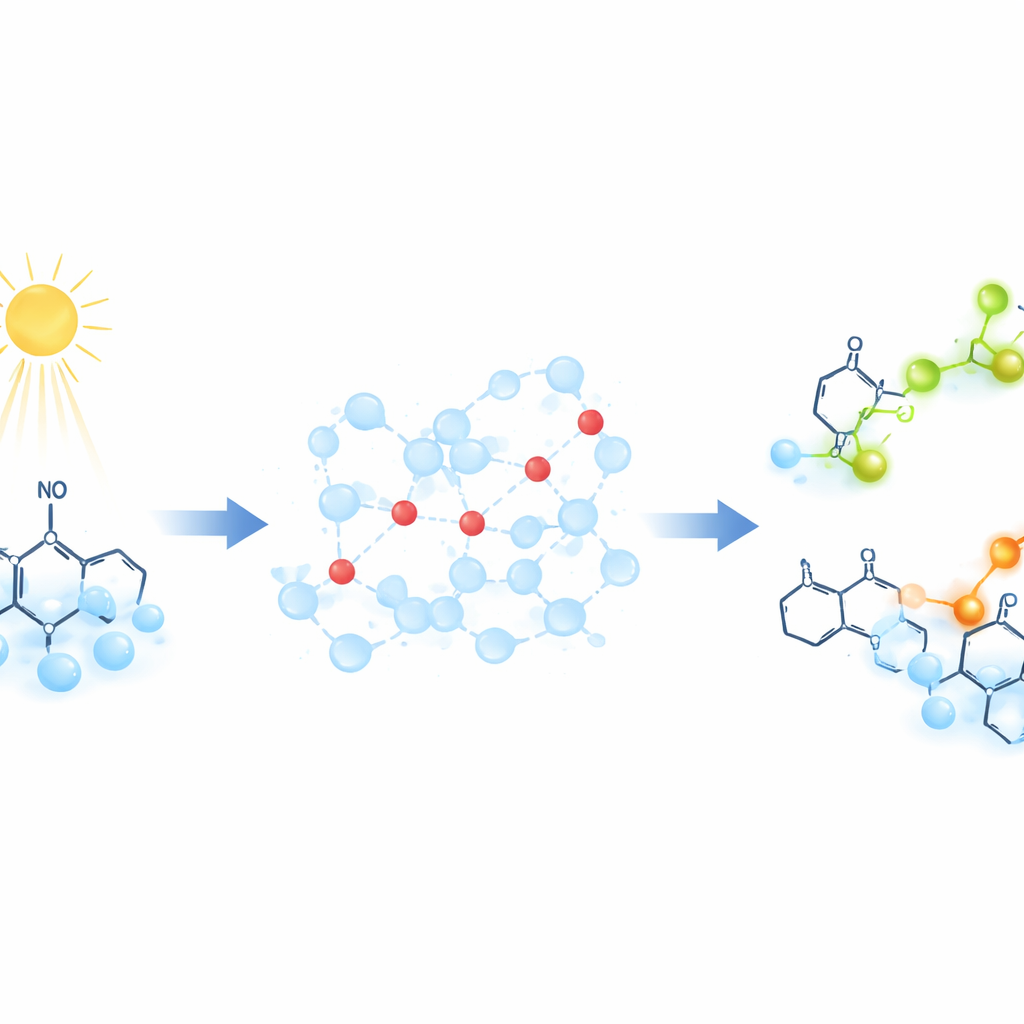
Un nuovo modo per osservare il movimento dei protoni
Invece di seguire i protoni direttamente, i ricercatori usano molecole «sonda» speciali che cambiano la loro firma magnetica quando acquisiscono un protone. Queste sonde sono radicali organici stabili il cui elettrone spaiato produce un segnale ben definito nella risonanza parametrica elettronica (EPR), una tecnica che rileva come gli elettroni spaiati rispondono a un campo magnetico. Per far partire il moto dei protoni su comando, il gruppo illumina un composto chiamato 2‑nitrobenzaldeide. Questa reazione indotta dalla luce rilascia un’esplosione di protoni in meno di un miliardesimo di secondo, abbassando improvvisamente il pH della soluzione. Man mano che i protoni si diffondono attraverso l'acqua e si legano alle sonde, il segnale EPR si sposta in funzione del tempo, permettendo agli scienziati di tracciare la velocità con cui avviene il trasferimento protonico.
Come i vicini dell'acqua rallentano o accelerano il flusso
L'acqua raramente esiste da sola; è di solito affollata da sali disciolti o altre molecole che riorganizzano sottilmente la sua rete di legami a idrogeno. Il gruppo ha testato come tali additivi influenzano il moto dei protoni confrontando acqua pura con soluzioni contenenti cloruro di potassio, urea o cloridrato di guanidinio, tutte a concentrazioni elevate. Adattando i cambiamenti EPR a semplici modelli cinetici, hanno estratto tassi apparenti per il trasferimento protonico. Hanno scoperto che in 6 molari di cloridrato di guanidinio il trasferimento protonico era circa 40 volte più lento che nell'acqua pura, mentre 8 molari di urea causavano solo un rallentamento modesto, e il cloruro di potassio produceva effetti intermedi. Poiché la velocità con cui i protoni reagiscono con le sonde è limitata da come si muovono attraverso la rete di legami a idrogeno, queste differenze indicano cambiamenti sostanziali nella struttura dell'acqua attorno agli ioni e alle molecole aggiunte.
Moto protonico in ghiaccio vetroso e all'interno delle proteine
Il metodo non è limitato all'acqua liquida ordinaria. Gli autori hanno anche studiato una miscela acqua‑glicerolo raffreddata a 160 kelvin, dove si forma un vetro rigido. La diffusione libera delle molecole è essenzialmente congelata, eppure il segnale EPR ha mostrato comunque che le sonde venivano protonate dopo l'esposizione alla luce. Questo suggerisce che il trasferimento protonico può procedere senza la diffusione classica, possibilmente tramite tunneling quantistico lungo una catena di legami a idrogeno, riecheggiando i raffinamenti moderni dell'idea di Grotthuss. Per esplorare la rilevanza biologica, il team ha attaccato un radicale sensibile al pH a un sito specifico della proteina di membrana bacteriorodopsina, al confine tra la proteina e l'acqua circostante. Quando hanno innescato il rilascio di protoni con la luce, hanno osservato una risposta EPR dipendente dal tempo da questo sito etichettato, dimostrando che il loro approccio può monitorare la consegna di protoni a una posizione definita sulla superficie proteica.
Collegare struttura, acqua e autostrade protoniche
Per comprendere meglio perché la sonda legata alla proteina si comportasse in modo simile a quella in acqua libera, i ricercatori hanno eseguito simulazioni al computer della bacteriorodopsina in membrana e di un piccolo peptide in soluzione. Hanno calcolato come le molecole d'acqua circondano il gruppo nitrossile dell'etichetta di spin e hanno trovato pattern di idratazione locale quasi identici in entrambi i casi, con solo un lieve schermamento dovuto all'ambiente di membrana. Questo significa che, almeno per il sito studiato, i protoni hanno accesso attraverso uno strato d'acqua che somiglia molto all'acqua liquida ordinaria. Gli autori mostrano anche che le loro sonde possono essere usate in esperimenti EPR risolti nel tempo, aprendo la strada al monitoraggio congiunto del moto di protoni ed elettroni in reazioni dove i due sono strettamente collegati.
Cosa ci dice questo lavoro in termini semplici
In sostanza, questo studio trasforma la luce in un colpo di pistola preciso per il moto dei protoni e poi usa sonde magnetiche sensibili per osservare quanto rapidamente quei protoni raggiungono bersagli diversi. Confrontando soluzioni saline semplici, denaturanti densi, miscele vetrose e una proteina di membrana, i ricercatori dimostrano che il flusso di protoni è fortemente modellato da come le molecole d'acqua sono disposte e dall'ambiente circostante. Il loro approccio non solo supporta l'idea che i protoni saltino lungo reti di legami a idrogeno, ma rivela anche che questo salto può persistere anche quando il moto molecolare ordinario è quasi congelato. Questo nuovo kit di strumenti potrebbe aiutare gli scienziati a scomporre come i protoni si muovono in enzimi, sistemi di conversione dell'energia e materiali innovativi, avvicinandoci al controllo di questi piccoli ma potenti vettori di carica.
Citazione: Barbon, A., Savitsky, A., Grigoriev, I. et al. Photoinduced proton transfer in differently structured water: an EPR approach to solving a classic problem. Sci Rep 16, 7983 (2026). https://doi.org/10.1038/s41598-026-38650-0
Parole chiave: trasferimento di protoni, struttura dell'acqua, risonanza parametrica elettronica, rete di legami a idrogeno, bacteriorodopsina