Clear Sky Science · it
Le cellule T attivate inducono apoptosi nelle cellule di adenocarcinoma polmonare A549 tramite influx di calcio mediato da TRPV4
Perché questa ricerca è importante per il cancro al polmone
Il cancro al polmone rimane uno dei tumori più letali, in parte perché i tumori spesso imparano a resistere ai trattamenti standard come chemioterapia e radioterapia. Negli ultimi anni sfruttare il sistema immunitario del paziente ha offerto nuove speranze. Questo studio esplora una variante di quell’idea: mostra come un tipo specifico di cellula immunitaria, le cellule T attivate, possa spingere le cellule tumorali polmonari verso l’autodistruzione facendole assorbire calcio attraverso una “porta” molecolare nota come TRPV4. Comprendere questa via potrebbe aiutare i ricercatori a progettare immunoterapie più potenti e precise.
I soldati del sistema immunitario incontrano le cellule tumorali polmonari
I ricercatori si sono concentrati sulle cellule umane di adenocarcinoma polmonare note come cellule A549, un modello ampiamente usato per il carcinoma polmonare non a piccole cellule. Hanno messo in contatto queste cellule tumorali con cellule T Jurkat, impiegate come sostituto delle cellule T citotossiche, che normalmente cercano e distruggono cellule infette o maligne. Attivando chimicamente le cellule Jurkat, il gruppo ha riprodotto lo stato altamente reattivo delle cellule T impegnate in una risposta immunitaria reale. Hanno quindi mescolato cellule T attivate o inattive con le cellule tumorali polmonari a rapporti diversi e osservato cosa accadeva nell’arco di uno-tre giorni, monitorando in particolare quante cellule tumorali sopravvivevano e quante andavano incontro alla morte programmata, o apoptosi.
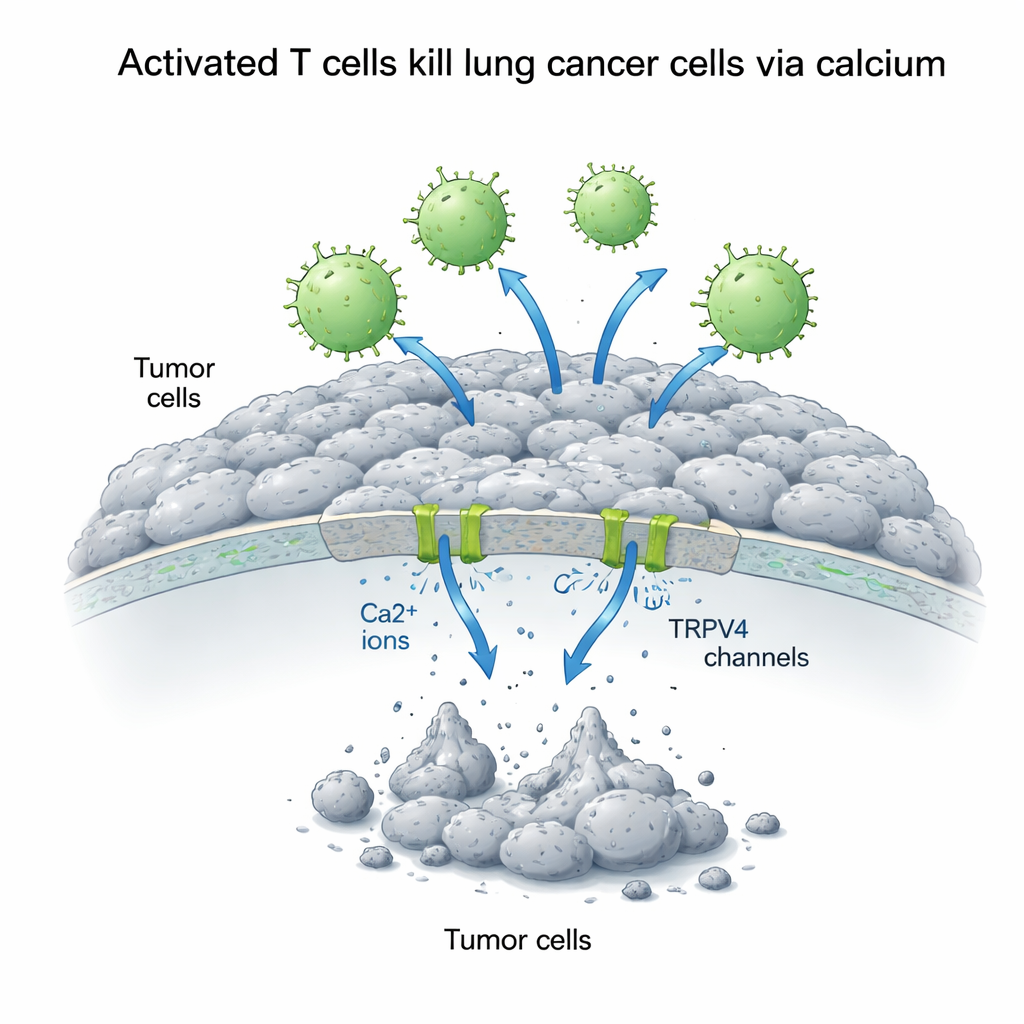
Il calcio come segnale a doppio taglio per le cellule tumorali
Il calcio intracellulare agisce come un interruttore di segnalazione versatile che può promuovere la crescita oppure innescare la morte, a seconda di come viene gestito. Gli scienziati hanno aumentato la quantità di calcio all’esterno delle cellule A549 e misurato come ciò influenzasse lo scontro tra cellule T e cellule tumorali. Sorprendentemente, il calcio extra da solo ha migliorato la crescita delle cellule tumorali polmonari, suggerendo che in condizioni di calma il calcio alimenta le vie di sopravvivenza. Ma in presenza di cellule T attivate, la situazione si è ribaltata: un maggior calcio esterno ha rafforzato in modo marcato l’uccisione mediata dalle cellule T. Nell’arco di 72 ore, la sopravvivenza delle cellule tumorali è precipitata a meno di un terzo del normale quando cellule T attivate e calcio aggiuntivo erano combinati, mentre le cellule T inattive avevano scarso effetto e potevano perfino favorire la crescita se veniva aggiunto calcio.
Una “porta” del calcio collegata allo stress e alla morte cellulare
Per capire come avvenga questo passaggio dalla crescita alla morte, il gruppo ha esaminato TRPV4, un canale proteico nella membrana cellulare che consente il flusso di calcio verso l’interno. Tramite analisi proteiche hanno scoperto che i livelli di TRPV4 aumentavano nettamente quando le cellule A549 erano esposte a calcio aggiunto, sia in presenza sia in assenza di cellule T, e risultavano massimi quando calcio e cellule T attivate erano combinati. Allo stesso tempo, le cellule tumorali mostravano chiari segni di stress ossidativo: l’equilibrio si spostava lontano dagli antiossidanti protettivi (minore capacità antiossidante totale) e verso gli ossidanti dannosi (maggiore stato ossidante totale). La citometria a flusso, una tecnica che marca le cellule con coloranti fluorescenti, ha confermato che le cellule T attivate causavano un’impennata sia nelle fasi iniziali sia in quelle tardive dell’apoptosi, soprattutto quando il calcio era abbondante. Nel complesso, queste osservazioni indicano una catena di eventi in cui i canali TRPV4 lasciano entrare più calcio, il quale a sua volta alimenta lo stress chimico intracellulare e spinge la cellula verso la morte.
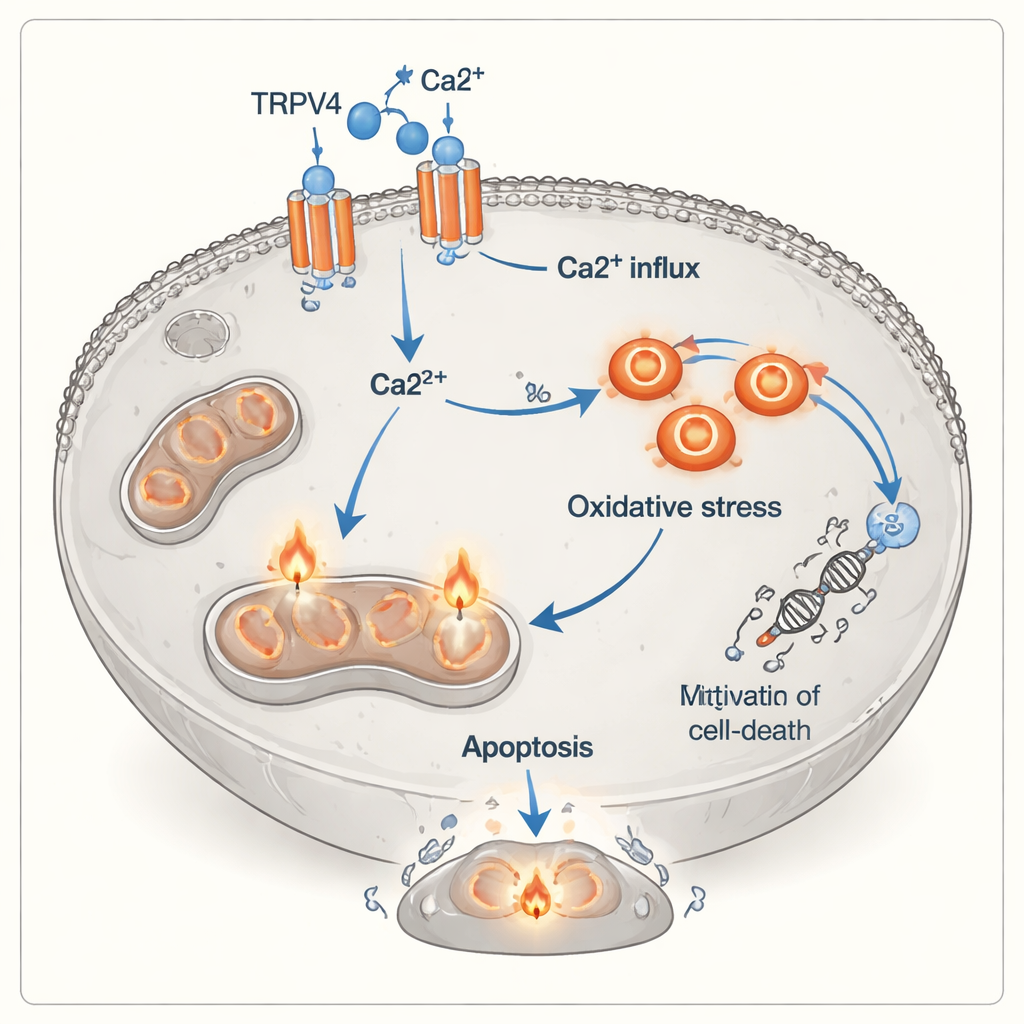
Un nuovo livello nel modo in cui le cellule immunitarie uccidono i tumori
Classicamente, le cellule T citotossiche distruggono i loro bersagli rilasciando proteine tossiche o attivando recettori della morte sulla superficie delle cellule tumorali. Questo studio suggerisce che esiste un’altra via, più indiretta: segnali provenienti dalle cellule T attivate — incluse molecole infiammatorie e il contatto stretto cellula-cellula — sembrano rendere le cellule tumorali polmonari più dipendenti da TRPV4 e più vulnerabili al sovraccarico di calcio e al danno ossidativo. In questa prospettiva, TRPV4 funziona come un interruttore di sensibilizzazione che trasforma il calcio, altrimenti promotore di crescita, in un segnale letale. Sebbene gli esperimenti siano stati condotti in colture e con una sola linea cellulare tumorale, evidenziano un possibile ponte importante tra attacco immunitario, canali ionici e la macchina interna dello stress delle cellule tumorali.
Cosa potrebbe significare per i trattamenti futuri
Per i non addetti ai lavori, la conclusione è che il successo dell’immunoterapia potrebbe dipendere non solo dal rendere le cellule T più potenti, ma anche dal rendere le cellule tumorali più facili da eliminare. Mirando a TRPV4 o a canali del calcio correlati, in futuro i medici potrebbero potenziare la capacità delle cellule T di eliminare i tumori polmonari o affinare i trattamenti per evitare danni ai tessuti sani. Il lavoro è ancora in una fase iniziale, e gli autori sottolineano la necessità di ulteriori esperimenti in modelli animali e in sistemi più complessi. Anche così, la scoperta di un asse TRPV4–calcio–stress ossidativo aggiunge un bersaglio promettente all’arsenale per migliorare le terapie basate sul sistema immunitario contro il cancro al polmone.
Citazione: Alavi, F., Kazemi-Lomedasht, F., Eftekhari, Z. et al. Activated T cells induce apoptosis in A549 lung adenocarcinoma cells via TRPV4-mediated calcium influx. Sci Rep 16, 7155 (2026). https://doi.org/10.1038/s41598-026-38589-2
Parole chiave: immunoterapia del cancro polmonare, cellule T, segnalazione del calcio, canale TRPV4, stress ossidativo