Clear Sky Science · it
Analisi frattale della vascolarizzazione del carcinoma epatocellulare mostra differenze regionali indipendenti dall’invasione vascolare
Vedere il cancro attraverso i suoi vasi sanguigni
I medici sanno che i tumori sviluppano una propria rete caotica di vasi sanguigni e che la disposizione di questi vasi può influenzare l’efficacia dei trattamenti. Nel cancro al fegato, i farmaci che mirano all’apporto di sangue fanno già parte della pratica clinica, ma le misure di laboratorio attuali contano principalmente il numero di vasi, non la loro organizzazione. Questo studio pone una domanda semplice ma potente: è possibile catturare il “pattern” dei vasi tumorali con pochi numeri e questi pattern differiscono tra tumore, tessuto circostante e il resto del fegato?
Pattern nascosti nelle reti ramificate
I ricercatori si sono concentrati sul carcinoma epatocellulare, il più comune tumore primario del fegato. Hanno esaminato campioni di tessuto di 29 pazienti i cui preparati erano stati colorati in modo che l’endotelio dei vasi apparisse marrone al microscopio. Invece di limitarsi a contare i vasi, hanno analizzato come i vasi riempiono lo spazio complessivamente, usando strumenti matematici spesso applicati a forme naturali complesse come coste o rami di alberi. Sono state usate due misure chiave: una che descrive quanto la rete vascolare è “intricata” e un’altra che descrive come sono distribuiti gli spazi vuoti tra i vasi. Insieme, questi numeri condensano la complessità visiva della rete vascolare in una forma confrontabile tra diverse regioni del fegato.
Trasformare immagini al microscopio in mappe misurabili
Per farlo, il team ha innanzitutto dovuto separare in modo affidabile i vasi dal tessuto di fondo su grandi vetrini digitali. Hanno costruito una pipeline automatizzata di elaborazione delle immagini che ha identificato i vasi colorati di marrone, rimosso il rumore e riempito gli interni dei vasi, producendo chiare mappe in bianco e nero delle reti vascolari. Queste segmentazioni automatiche sono state verificate da un patologo epatico e risultavano ben concordanti, in particolare per gli aspetti rilevanti alle misure globali di organizzazione vascolare. I vetrini sono poi stati suddivisi in molte tessere più piccole, ciascuna assegnata a una delle tre regioni: tumore, tessuto immediatamente circostante il tumore (peri-tumorale) o fegato non tumorale distante. Le tessere contenenti tessuto necrotico o importanti artefatti sono state escluse con cura, perché possono imitare pattern vascolari densi e non realistici.
Come le regioni tumorali differiscono dal resto
Su migliaia di tessere, lo studio ha riscontrato differenze chiare e statisticamente robuste nei pattern vascolari fra le tre regioni del fegato. Il tessuto epatico non tumorale mostrava la complessità più alta, comportandosi quasi come una rete che riempie lo spazio su scale maggiori. Il tessuto peri-tumorale si collocava in una posizione intermedia, mentre le regioni tumorali avevano consistentemente una complessità inferiore. Una misura correlata su come sono disposti gli spazi vuoti tra i vasi aumentava anch’essa passando dal non tumorale al peri-tumorale al tumore, indicando che i vasi associati al tumore sono più raggruppati e presentano maggiore correlazione spaziale. Fondamentale è che il fatto che il tumore avesse iniziato o meno a invadere i vasi vicini — un importante segnale clinico — non cambiava in modo misurabile questi pattern globali. L’architettura della rete vascolare era modellata principalmente dalla presenza del tumore stesso, non da questo stadio di invasione.
Perché forma e dimensione dei vasi contano
Per capire cosa sottendesse a queste differenze numeriche, gli autori hanno esaminato più da vicino le forme e le dimensioni dei singoli vasi. Nel fegato sano si osservava un evidente accumulo di molti piccoli vasi circolari, con pochi vasi più grandi. Nelle regioni tumorali, l’area vascolare totale era simile, ma i vasi erano distribuiti in modo più uniforme tra le dimensioni e più spesso allungati o irregolari. Semplici modelli hanno mostrato che una rete ricca di molti piccoli vasi tondi obbliga a utilizzare più piccole caselle quando si “copre” il pattern, il che aumenta la misura di complessità. Al contrario, una rete con meno piccoli vasi e dimensioni più uniformi appare meno intricata, anche se contiene una superficie vascolare totale simile. Questo spostamento geometrico corrisponde alla diminuzione osservata di complessità nei tumori e spiega come sottili cambiamenti nella distribuzione delle forme dei vasi possano rimodellare il pattern vascolare complessivo.
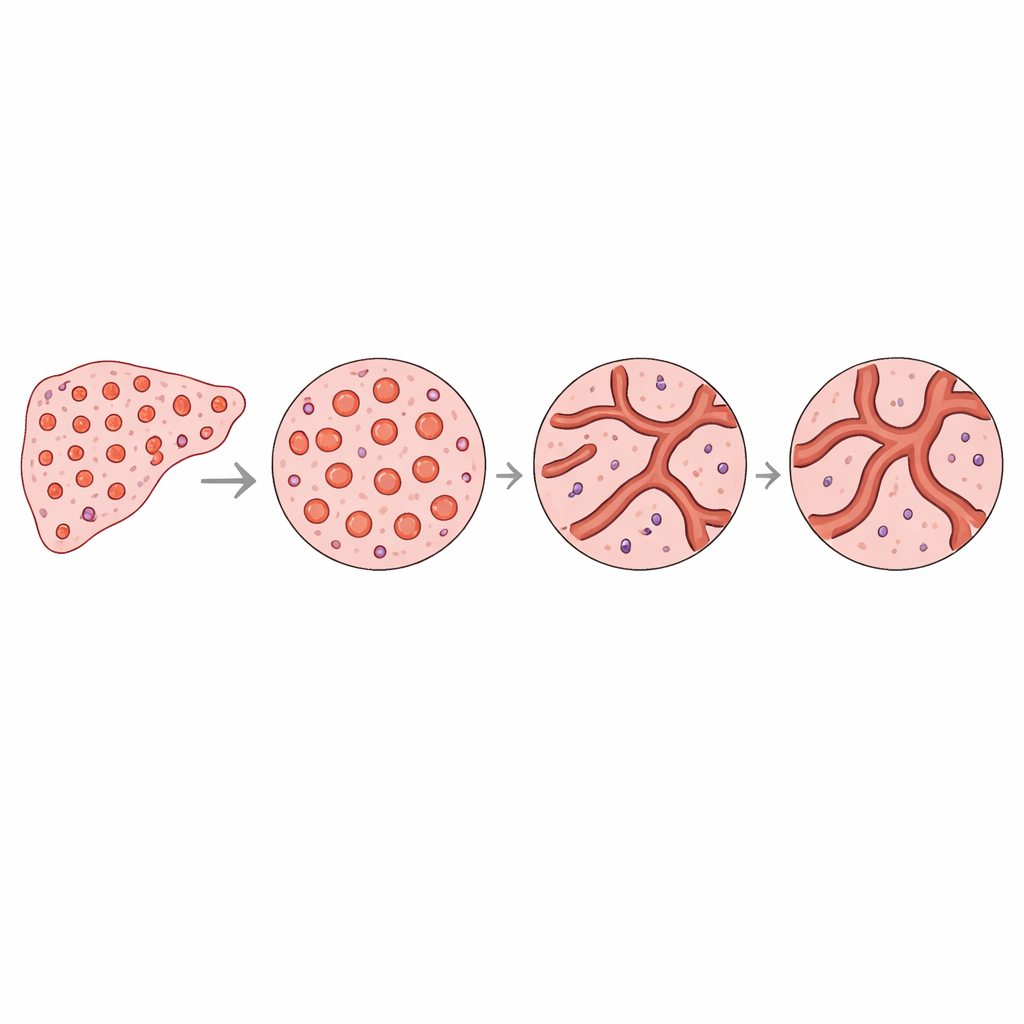
Cosa potrebbe significare per le scansioni future
Per i non specialisti, la conclusione principale è che i tumori epatici non si limitano ad aumentare il numero di vasi; li riorganizzano in modo distinto e misurabile che si estende nel tessuto circostante. Queste differenze possono essere catturate da descrittori matematici compatti che riassumono come sono disposti i vasi e gli spazi tra di essi. Il lavoro suggerisce che, in futuro, metodi di imaging avanzati potrebbero stimare questi descrittori senza biopsia, fornendo nuovi biomarcatori non invasivi di quanto si estende l’influenza di un tumore e di come è strutturato il suo apporto sanguigno. Allo stesso tempo, lo studio mostra che l’invasione microscopica dei vasi vicini non lascia necessariamente un’impronta riconoscibile sul pattern vascolare su larga scala, sottolineando che non tutti i comportamenti tumorali pericolosi sono visibili dall’architettura vascolare da sola.
Citazione: Penney, J., Nardon, V., Beaufrere, A. et al. Fractal analysis of hepatocellular carcinoma vasculature shows regional differences independent of vascular invasion. Sci Rep 16, 11049 (2026). https://doi.org/10.1038/s41598-026-38580-x
Parole chiave: vascolarizzazione del cancro al fegato, architettura vascolare frattale, carcinoma epatocellulare, microambiente tumorale, biomarcatori di imaging non invasivo