Clear Sky Science · it
Ottimizzazione di agenti leganti la galectina-3 mediante sintesi in situ di composti multipli e spettrometria di massa nativa
Perché questo è importante per i farmaci del futuro
Molti medicinali moderni agiscono legandosi a proteine nel nostro organismo, ma trovare una piccola molecola che si attacchi in modo forte e selettivo al sito giusto è un processo lento, costoso e spesso frustrante. Questo studio presenta un modo più veloce per perfezionare tali molecole direttamente in presenza della proteina bersaglio, e per identificare poi i vincitori con una tecnica di pesatura altamente sensibile. Gli autori dimostrano il loro approccio sulla galectina-3, una proteina collegata alla crescita tumorale, ottenendo un candidato promettente con caratteristiche farmaceutiche che si lega tanto saldamente quanto alcuni dei migliori composti esistenti, ma in una tasca inaspettata sulla superficie della proteina.

Rivedere il modo in cui cerchiamo lead migliori
L’ottimizzazione tradizionale dei farmaci assomiglia a un costoso gioco d’ipotesi. I chimici modificano un composto di partenza passo dopo passo, testano ogni versione e sperano di migliorare l’affinità per la proteina bersaglio. Ma le superfici proteiche sono flessibili, le molecole d’acqua interferiscono e l’evento di legame stesso può rimodellare la proteina, rendendo inaffidabili le previsioni al calcolatore. Anche quando è disponibile una struttura ad alta risoluzione, non c’è garanzia che una modifica suggerita sia utile. I metodi “guidati dal bersaglio” esistenti cercano di lasciare che sia la proteina a scegliere i suoi partner da un pool di mattoni di costruzione, tuttavia questi approcci dipendono ancora da analisi complesse e segnali indiretti per inferire quale composto si leghi davvero meglio.
Lasciare che la proteina scelga, poi pesare i vincitori
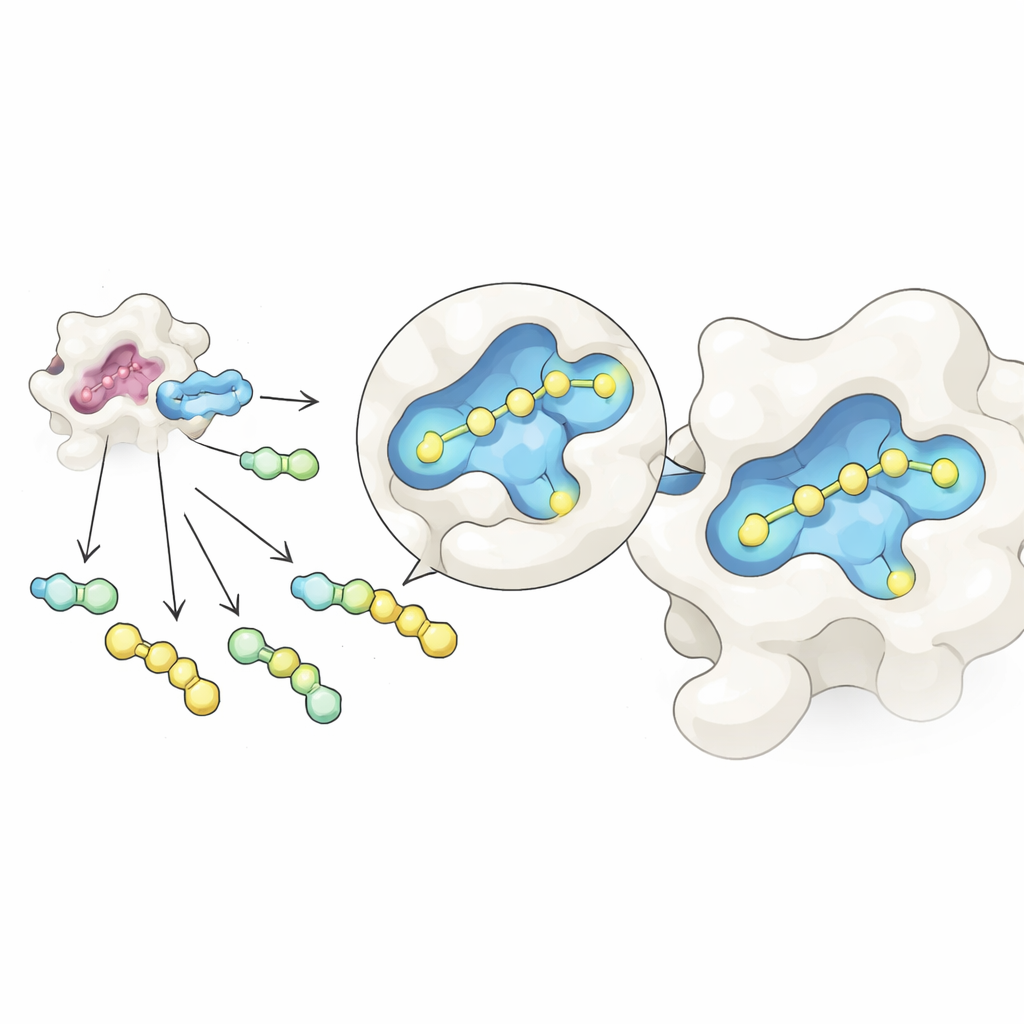
I ricercatori hanno combinato due idee in un unico flusso di lavoro snello. Prima, hanno utilizzato una reazione chimica reversibile che collega un nucleo glucidico comune a molti diversi pezzi laterali in un’unica provetta, formando una miscela di molecole correlate. Regolando con cura i rapporti di partenza, i prodotti risultanti raggiungono uno stato di equilibrio regolato da semplici leggi di concentrazione, il che aiuta a livellare le loro quantità nonostante differenze nella reattività intrinseca. Secondo, hanno esposto questa miscela alla galectina-3 ed esaminata con spettrometria di massa nativa, una forma di spettrometria di massa che mantiene intatti i complessi proteina–molecola in una soluzione delicata e simile all’acqua. Poiché ogni candidato ha una massa distinta, lo strumento può rilevare direttamente quali molecole sono effettivamente legate alla proteina, senza etichette o marcatori di riferimento.
Da miscele affollate a un legante che si distingue
Con questa configurazione, il team ha creato dozzine di leganti per la galectina-3 attaccando vari gruppi laterali a un nucleo glucidico ispirato a un inibitore noto, GB1107. Hanno suddiviso 35 diversi idrazidi in gruppi gestibili, formato tutte le combinazioni in situ e poi aggiunto la galectina-3. La spettrometria di massa nativa ha evidenziato quei composti che più spesso viaggiavano insieme alla proteina, segnalando così i principali hit. Un test successivo di stabilità termica, che misura come un composto stabilizzi la proteina al riscaldamento, ha eliminato falsi positivi dovuti a peculiarità della misura in fase gassosa. Sono rimasti tre candidati di punta, e misure dettagliate di legame basate sul calore hanno mostrato che uno, chiamato GalAldBZ20, si legava alla galectina-3 in modo particolarmente forte, nell’intervallo sub-micromolare.
Scoprire una tasca nascosta e rafforzarla
La sorpresa successiva è arrivata quando il team ha analizzato come GalAldBZ20 si posizionava sulla superficie della galectina-3. La maggior parte dei noti leganti sfrutta una tasca “alpha” vicino al sito di legame del glucosio, ma i metodi strutturali e le simulazioni al calcolatore hanno indicato che GalAldBZ20 preferiva invece una tasca vicina, denominata “beta”. La cristallografia a raggi X suggeriva questa possibilità, la risonanza magnetica nucleare in soluzione ha rivelato multiple conformazioni locali vicino a quella tasca e le simulazioni di dinamica molecolare supportavano un modello in cui un anello contenente un gruppo nitro si incastra nella sede beta. Ragionando sul fatto che fosse possibile consolidare meglio questo assetto, i chimici hanno riprogettato il legante chimico tra lo zucchero e l’anello nitro per favorire nuovi contatti polari con la proteina e ridurne la flessibilità.
Trasformare uno screening intelligente in un candidato potente
Con questa intuizione, il gruppo ha sintetizzato un piccolo set di molecole di follow-up più rigide che mantenevano lo stesso zucchero e l’anello nitro ma modificavano il connettore tra di essi. Una versione, un N-galattoside (composto 5), si è distinta: si legava alla galectina-3 circa dieci volte più saldamente rispetto all’hit originale, raggiungendo un’affinità paragonabile a GB1107, pur preferendo ancora la tasca beta. Una struttura cristallina a ultra-alta risoluzione ha mostrato una densità chiara per l’anello nitro incastrato in quella tasca, sostenuto da diversi legami a idrogeno e da un contatto cation-π con amminoacidi chiave. Quando il gruppo nitro è stato rimosso o sostituito con un semplice gruppo metile, il legame si è indebolito notevolmente, sottolineandone l’importanza. Poiché la galectina-1, una proteina correlata, è priva di questa tasca beta, il nuovo composto potrebbe alla fine offrire maggiore selettività, una caratteristica molto ricercata nel design dei farmaci.
Cosa significa per la scoperta di farmaci futura
In termini accessibili, questo lavoro dimostra che si possono miscelare molte molecole correlate, lasciare che una proteina rilevante per la malattia ne “scelga” le preferite e poi pesare direttamente quei complessi proteina–molecola per vedere quali aderiscono meglio. Applicata alla galectina-3, questa strategia ha trovato inaspettatamente e poi rafforzato il legame a una tasca poco esplorata, producendo un composto che rivaleggia con alcuni dei migliori inibitori esistenti e che potrebbe fungere da lead per nuovi farmaci anticancro. Più in generale, accoppiare chimica in situ con spettrometria di massa nativa offre una scorciatoia generale per perfezionare lead farmacologici contro proteine con molteplici siti di legame possibili, risparmiando potenzialmente tempo, materiali e sforzi nelle fasi iniziali della scoperta di farmaci.
Citazione: Hoshi, K., Konuma, T., Taguchi, R. et al. Optimization of galectin-3 binding agents by in situ multiple compound synthesis and native mass spectrometry. Sci Rep 16, 8453 (2026). https://doi.org/10.1038/s41598-026-38570-z
Parole chiave: inibitori della galectina-3, spettrometria di massa nativa, scoperta di farmaci basata su frammenti, sintesi guidata dal bersaglio, lead per farmaci antitumorali