Clear Sky Science · it
Adattamenti termoregolatori al freddo nei topi C3H/HeJ indipendenti dalla segnalazione ADRB3
Perché i topi che tollerano il freddo sono importanti per la salute umana
Mantenersi caldi può non sembrare un tema medico all’avanguardia, ma il modo in cui l’organismo affronta il freddo riguarda direttamente come usa e brucia energia. Questo studio confronta due ceppi comuni di topi da laboratorio e pone una domanda sorprendentemente rilevante: quando vengono esposti al freddo, attivano i loro “forni” interni nello stesso modo degli esseri umani? La risposta aiuta a spiegare perché alcuni farmaci anti-obesità efficaci nei topi hanno fallito nell’uomo e indica un modello murino più simile all’uomo per studiare il metabolismo.
Due tipi di topo, una sfida fredda
I ricercatori hanno confrontato i topi standard C57BL/6J, un cavallo di battaglia della ricerca metabolica, con un ceppo meno usato chiamato C3H/HeJ. Entrambi i gruppi sono stati mantenuti inizialmente intorno ai 30 °C, una temperatura alla quale i topi spendono pochissima energia per restare caldi. Poi gli animali sono stati raffreddati gradualmente fino a 10 °C, e peso corporeo, assunzione di cibo e consumo energetico sono stati misurati con precisione in gabbie metaboliche ad alta tecnologia. Interessante notare che entrambi i ceppi condividevano un “punto di comfort” per il consumo energetico minimo di circa 29–30 °C, il che significa che partivano da una baseline simile prima dell’esposizione al freddo.
Quando arriva il freddo, un ceppo fa più fatica
Quando le temperature sono scese, entrambi i tipi di topo hanno aumentato la spesa energetica, come previsto. Ma i topi C3H hanno bruciato più energia rispetto ai C57, pur mangiando quantità simili di cibo. Questo maggiore dispendio energetico non è stato solo una reazione di breve durata: è rimasto evidente sia nelle prime ore sia nei giorni successivi all’esposizione al freddo. Nonostante ciò, i C3H sono risultati più magri e con meno tessuto adiposo bruno complessivo, suggerendo che il loro grasso esistente lavorasse di più piuttosto che aumentare di volume. Anche gli esami del sangue hanno indicato che i C3H mobilizzavano più combustibile, come il glicerolo, per alimentare questa maggiore produzione di calore.
Grasso bruno e bianco collaborano per generare calore
Per capire cosa succedeva all’interno del corpo, il team ha esaminato il tessuto adiposo bruno — il classico tessuto generatore di calore — e due tipi di tessuto adiposo bianco. Nei C3H, il freddo ha fortemente aumentato l’attività dei geni legati alla termogenesi nel grasso bruno, e le proteine chiave che sostengono la combustione dei substrati e l’attività mitocondriale sono risultate più attivate. La microscopia ha rivelato cambiamenti strutturali coerenti con un tessuto più attivo. Anche il tessuto adiposo bianco ha mostrato un quadro simile: in particolare, un deposito attorno ai testicoli, normalmente lento a convertire cellule in produttrici di calore, ha mostrato una marcata attivazione nei C3H. Questo suggerisce che in questi animali non solo il grasso bruno ma anche il grasso tradizionalmente «di riserva» può essere reclutato per aiutare a mantenere la temperatura corporea.
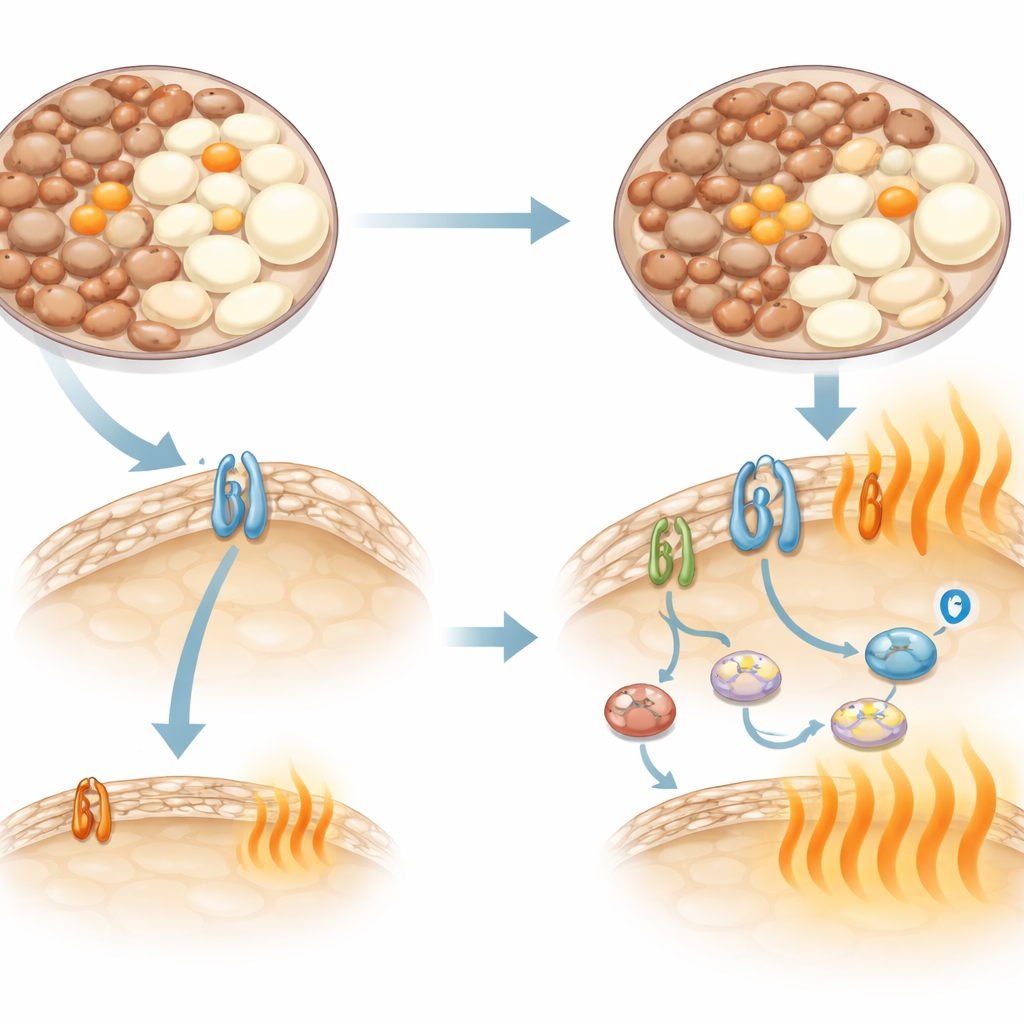
Una diversa organizzazione dei segnali nervosi al tessuto adiposo
La produzione di calore nel grasso è normalmente guidata da segnali del sistema nervoso che agiscono attraverso recettori beta-adrenergici sulle cellule adipose. Nei topi C57 standard, un recettore chiamato beta-3 svolge un ruolo importante, e i farmaci che lo stimolano aumentano fortemente il consumo energetico. I ricercatori hanno confermato questo: un composto selettivo per il beta-3 ha provocato un forte e prolungato aumento della spesa energetica nei C57. Ma nei C3H lo stesso farmaco ha avuto un effetto debole e di breve durata. Gli esami genetici spiegano il motivo: in questi topi il recettore beta-3 è espresso solo in minima parte nel tessuto adiposo. Tuttavia, quando entrambi i ceppi hanno ricevuto noradrenalina, un segnale naturale che attiva diversi recettori correlati, i C3H hanno comunque aumentato la spesa energetica. Il blocco dei recettori beta-1 e beta-2 ha in gran parte cancellato le differenze tra i ceppi, indicando che i C3H si affidano a questi recettori alternativi e ad altre vie non classiche di termogenesi invece del beta-3.
Cosa significa per lo studio del metabolismo umano
Gli esseri umani, come i topi C3H, dipendono principalmente dai recettori beta-1 e beta-2 nel tessuto adiposo bruno, non dal beta-3. Questo può spiegare perché i farmaci mirati al recettore beta-3 hanno funzionato in ceppi murini tipici ma hanno deluso nei trial clinici. Mostrando che i C3H possono montare una forte risposta termogenica indotta dal freddo con quasi nessuna segnalazione beta-3, questo studio li mette in evidenza come modello più simile all’uomo per investigare come il grasso bruci energia. Per il lettore, la conclusione è che non tutti i topi sono uguali: scegliere il ceppo giusto e la temperatura di alloggio appropriata può rendere la ricerca preclinica molto più rilevante per la salute umana reale e per future terapie contro l’obesità e le malattie metaboliche.
Citazione: Beji, S., Mouchiroud, M., Gélinas, Y. et al. Thermoregulatory adaptations to cold in C3H/HeJ mice are independent of ADRB3 signaling. Sci Rep 16, 7859 (2026). https://doi.org/10.1038/s41598-026-38538-z
Parole chiave: tessuto adiposo bruno, adattamento al freddo, segnalazione adrenergica, modelli murini, spesa energetica