Clear Sky Science · it
Inibizione mirata di HDAC8 con composti non-idrossamati [1,2,4]triazolo[4,3-a]quinolina
Nuova speranza per un tumore infantile
Il neuroblastoma è un tumore infantile aggressivo che origina dalle cellule nervose ed è spesso difficile da trattare una volta che si è diffuso. Questo studio esplora un nuovo approccio per rallentare o uccidere le cellule di neuroblastoma spegnendo un interruttore cellulare chiave chiamato HDAC8. Costruendo una nuova famiglia di molecole simili a farmaci che agiscono in modo molto selettivo su questo interruttore, i ricercatori mirano a creare terapie sia più efficaci contro i tumori sia più tollerabili per il resto dell’organismo.
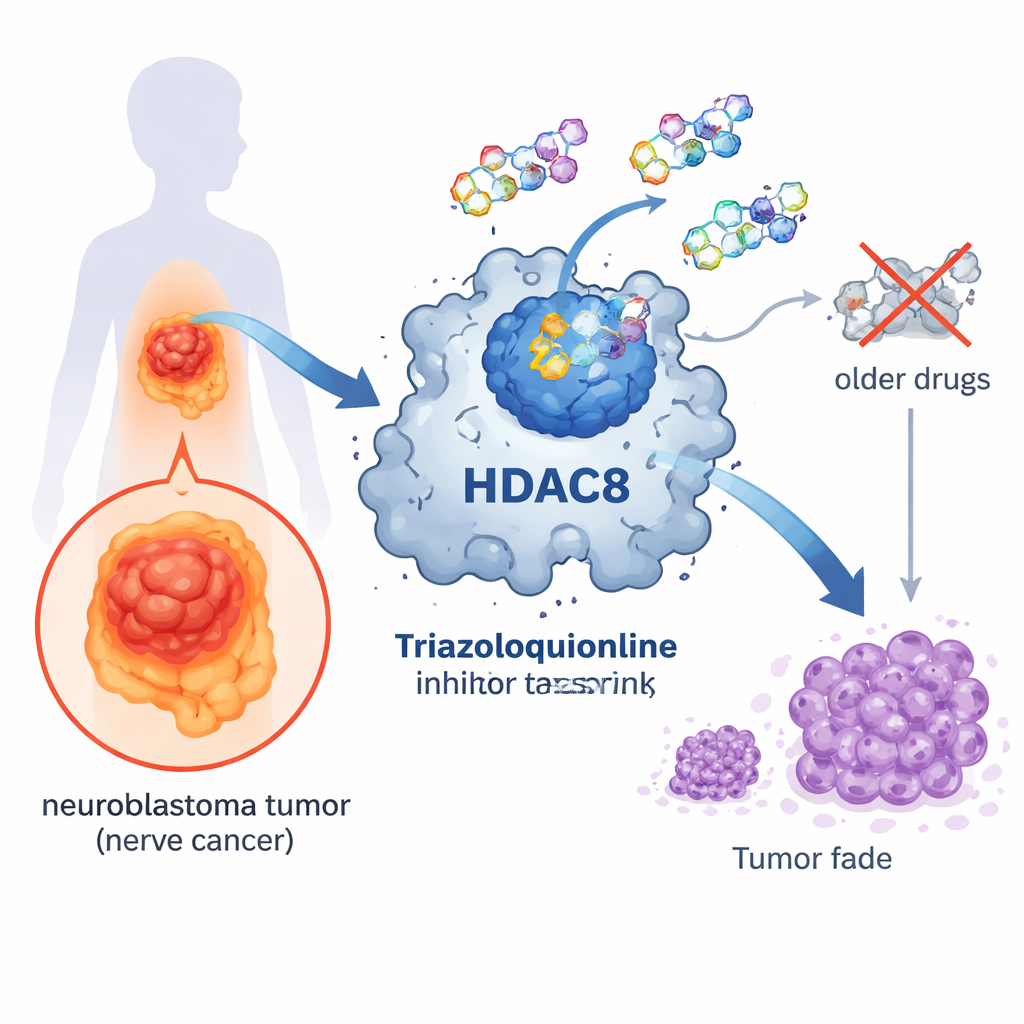
Un interruttore molecolare al centro del cancro
All’interno delle nostre cellule, i geni vengono costantemente attivati e disattivati. Un sistema di controllo importante si basa su piccole etichette chimiche chiamate gruppi acetile che si legano a proteine associate al DNA. Enzimi detti deacetilasi istoniche (HDAC) rimuovono queste etichette, comprimendo l’impacchettamento del DNA e in genere riducendo l’attività genica. HDAC8 è un membro di questa famiglia enzimatica ed è stato collegato a diversi tumori, incluso il neuroblastoma. Quando HDAC8 è iperattivo, le cellule tumorali possono crescere, sopravvivere e diffondersi più facilmente, rendendolo un bersaglio interessante per nuovi farmaci.
Limiti dei vecchi farmaci HDAC
Alcuni farmaci che bloccano le HDAC sono già approvati per alcuni tumori del sangue, ma tendono a colpire molti tipi di HDAC contemporaneamente. La maggior parte di questi medicinali utilizza un gruppo chimico idrossamato per aggrapparsi a uno ione metallico nel sito attivo dell’enzima. Pur essendo efficace, questo gruppo lega i metalli in modo così forte da poter causare effetti collaterali e limitare la capacità del farmaco di distinguere con precisione tra le diverse HDAC. Di conseguenza i pazienti possono sperimentare tossicità e le cellule normali possono essere danneggiate insieme a quelle tumorali. I ricercatori hanno quindi cercato progettazioni chimiche alternative che conservino i benefici antitumorali riducendo i danni indesiderati.
Progettare una nuova classe di inibitori mirati
In questo lavoro il team ha progettato e sintetizzato 21 nuovi composti basati su uno scheletro triazoloquinolinico, collegato tramite un legante flessibile a una regione «+alpha-amino amide» in grado di legare l’atomo di zinco nel sito attivo di HDAC8. Usando la progettazione assistita al computer, hanno scelto questa architettura per adattarsi a un stretto “canale di rilascio dell’acetato” unico di HDAC8, una caratteristica strutturale che aiuta a ottenere elevata specificità. Studi di docking dettagliati e simulazioni di dinamica molecolare hanno mostrato che diverse delle nuove molecole — in particolare quelle chiamate 9m e 9r — formano interazioni stabili e durature all’interno della tasca di HDAC8 e si legano tanto saldamente quanto, o più, di un noto inibitore di riferimento. È importante che test biochimici abbiano confermato che i migliori composti bloccano fortemente HDAC8 lasciando in gran parte intatti gli altri membri della famiglia HDAC.
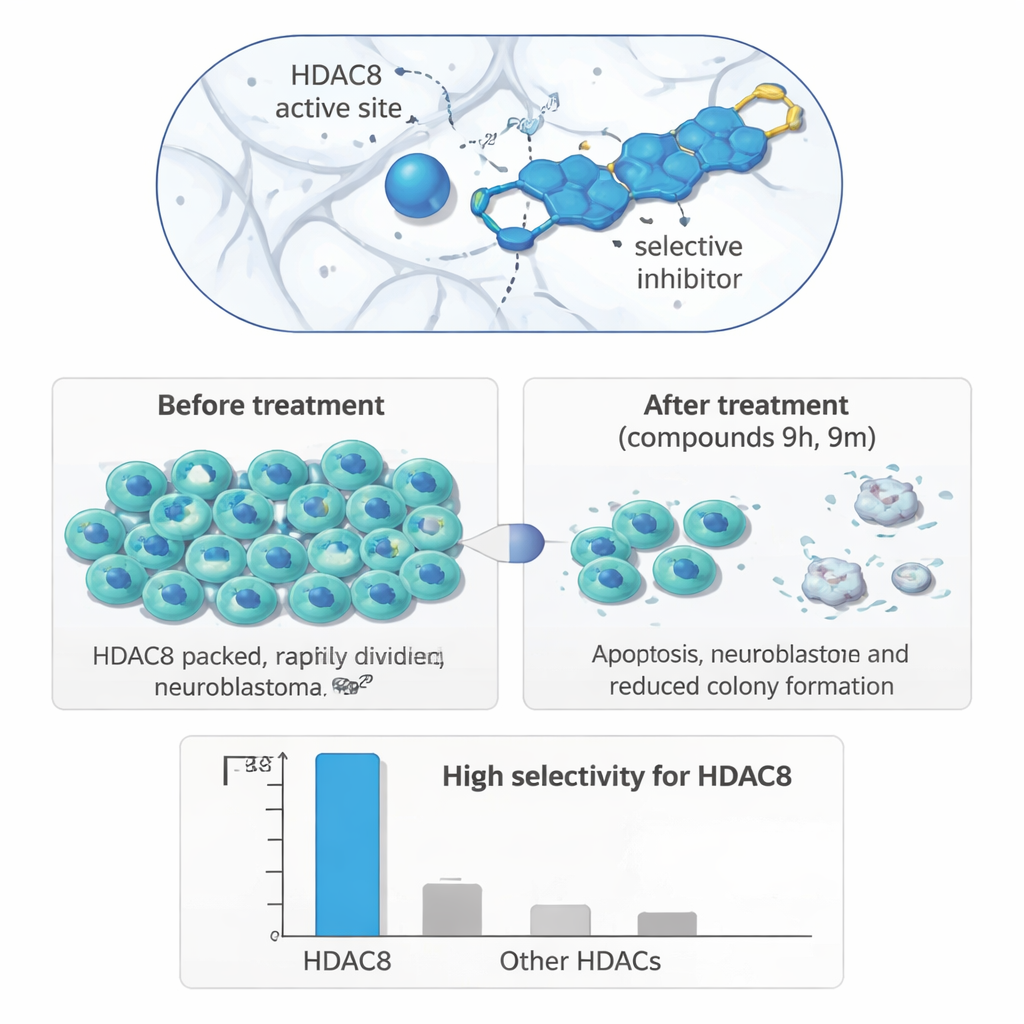
Dal provetto alle cellule tumorali
Per verificare se questo targeting enzima‑specifico si traduce in effetti biologici utili, i ricercatori hanno testato i loro composti su un pannello di linee cellulari umane. Nelle cellule di neuroblastoma (IMR‑32), due molecole, 9h e 9m, si sono distintamente evidenziate: hanno ridotto la crescita cellulare a concentrazioni micromolari e lo hanno fatto più intensamente nel neuroblastoma rispetto a cellule di tumore al seno o all’intestino, o rispetto a cellule renali non cancerose. Esperimenti a lungo termine di formazione di colonie hanno mostrato che le cellule di neuroblastoma trattate hanno perso gran parte della capacità di rigenerarsi dopo l’esposizione al farmaco. In un saggio di “wound‑healing”, che valuta la velocità con cui le cellule migrano per chiudere un graffio in uno strato cellulare, entrambi i composti hanno rallentato il movimento delle cellule di neuroblastoma, suggerendo una potenziale riduzione del potenziale metastatico.
Indagare come i composti uccidono le cellule tumorali
Esperimenti di citometria a flusso hanno rivelato che 9h e 9m inducono la morte cellulare programmata (apoptosi) nelle cellule di neuroblastoma e provocano un’accumulazione di cellule in una fase del ciclo cellulare associata a danno del DNA o morte (Sub‑G1). Per confermare che questi effetti derivino effettivamente dal blocco di HDAC8, il team ha misurato lo stato di acetilazione di una proteina chiamata SMC3, un noto bersaglio di HDAC8 coinvolto nel mantenimento dell’appaiamento delle cromatidi sorelle durante la divisione cellulare. Quando HDAC8 è inibito, l’SMC3 acetilato si accumula. Dopo il trattamento con 9h o 9m, i livelli di SMC3 acetilato sono aumentati nettamente, mentre la quantità totale di proteina SMC3 è rimasta invariata — una forte evidenza che questi composti colpiscono direttamente HDAC8 nelle cellule viventi e ne ostacolano la normale funzione nel controllo dei cromosomi.
Cosa potrebbe significare per i trattamenti futuri
Considerati nel loro insieme, la chimica, la modellazione al computer, i test enzimatici e gli esperimenti su cellule dipingono un quadro coerente: i composti triazoloquinolinici di nuova sintesi sono potenti inibitori altamente selettivi di HDAC8 in grado di frenare la crescita e la diffusione delle cellule di neuroblastoma risparmiando le altre isoforme HDAC. Poiché evitano il convenzionale gruppo idrossamato, potrebbero offrire una via più sicura per sfruttare HDAC8 come bersaglio terapeutico. Sebbene resti molto lavoro — in particolare studi su modelli animali e successivi trial clinici — questa ricerca pone una solida base per lo sviluppo di farmaci più precisi contro il neuroblastoma pediatrico e possibilmente altre patologie guidate da HDAC8.
Citazione: Bandaru, N.V.M.R., Fathima, A., Sengar, S. et al. Targeted HDAC8 inhibition with non-hydroxamate [1,2,4]triazolo[4,3-a] quinoline compounds. Sci Rep 16, 7472 (2026). https://doi.org/10.1038/s41598-026-38490-y
Parole chiave: Inibitori di HDAC8, neuroblastoma, terapia epigenetica, triazoloquinolina, farmaci oncologici mirati