Clear Sky Science · it
Correnti mediate da GluN2A e segnale del calcio in neuroni umani derivati da iPSC
Perché contano le minuscole cellule cerebrali coltivate in laboratorio
Gli scienziati ricorrono sempre più spesso a cellule cerebrali umane coltivate in laboratorio per studiare come si sviluppa il nostro cervello e per indagare cosa va storto in condizioni come autismo, epilessia e malattia di Alzheimer. Questo studio pone una domanda semplice ma cruciale: questi neuroni prodotti in laboratorio maturano e si connettono in modi che somigliano davvero al cervello umano, in particolare nel gestire un segnale chimico chiave chiamato glutammato? La risposta indica come costruire modelli di “mini-cervello” più realistici e suggerisce nuove modalità per esaminare la salute e le malattie del cervello.
Costruire neuroni da cellule riprogrammate
I ricercatori hanno iniziato da cellule staminali pluripotenti indotte umane—cellule ordinarie che sono state «riprogrammate» in uno stato di cellula staminale. Da lì, hanno indirizzato le cellule a diventare precursori neurali e infine reti di neuroni e astrociti di supporto, imitando la corteccia umana in sviluppo. Hanno confrontato due protocolli ampiamente usati, ovvero due condizioni di coltura. Una, chiamata mezzo BrainPhys, è progettata per promuovere neuroni attivi e elettricamente responsivi e tende a produrre più astrociti. L’altra, un mezzo di mantenimento neuronale più tradizionale, favorisce neuroni con un numero minore di astrociti. Nel corso di sessanta giorni, il team ha monitorato come queste colture cambiassero nell’aspetto, nell’attività genica e nei tipi cellulari, riscontrando che le colture cresciute in BrainPhys sviluppavano morfologie neuronali più elaborate e un rapporto neuroni/astrociti più vicino a quello del cervello umano reale.
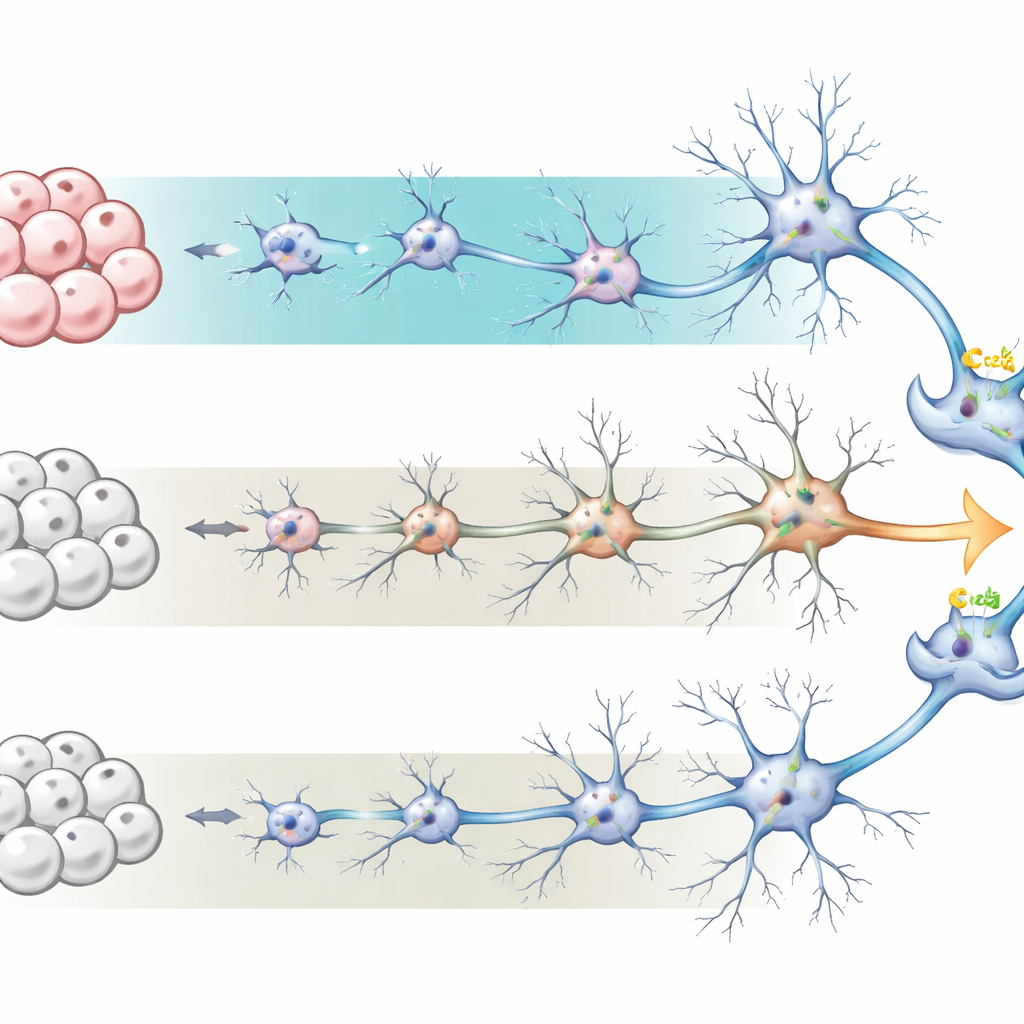
Segni che le cellule stanno maturando
Per valutare quanto i neuroni fossero «maturi», il team ha misurato l’attività genica globale mediante sequenziamento dell’RNA al giorno 60. Le cellule cresciute in BrainPhys mostravano quasi duemila geni espressi a livelli differenti rispetto al mezzo standard, molti dei quali collegati alla differenziazione neuronale, alla formazione delle sinapsi e all’attività elettrica. Anche i geni associati alla funzione degli astrociti e all’infiammazione risultavano più alti, riflettendo la maggiore popolazione di astrociti. Nel complesso, questi schemi suggeriscono che le colture BrainPhys ricapitano meglio stadi più avanzati dello sviluppo cerebrale, con punti di comunicazione tra neuroni più raffinati e un ambiente di supporto che somiglia maggiormente al tessuto vivente.
Interruttori chiave nella comunicazione chimica
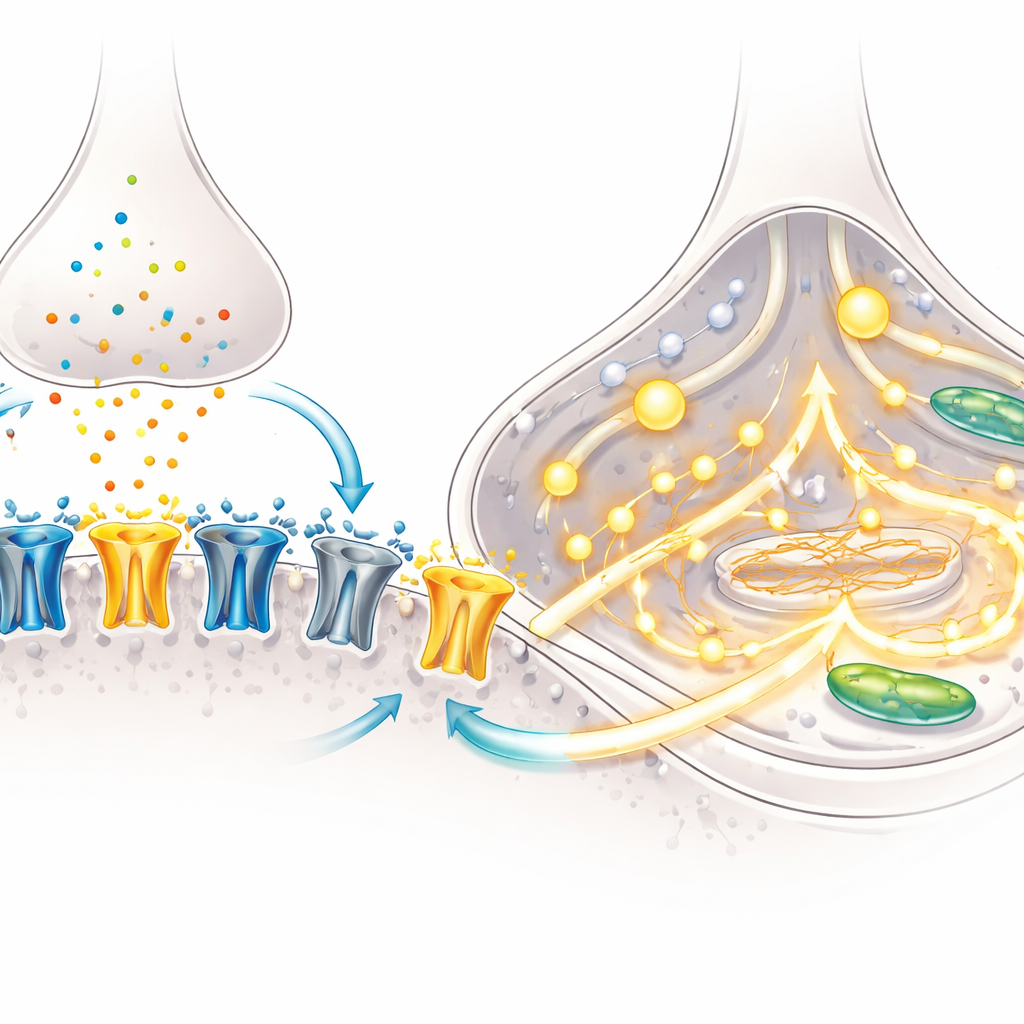
Una caratteristica distintiva della maturazione cerebrale è uno spostamento nella composizione dei recettori NMDA—porte molecolari sui neuroni che si aprono in risposta al glutammato e contribuiscono a stabilire connessioni legate all’apprendimento. All’inizio dello sviluppo domina una sottounità chiamata GluN2B; in seguito subentra GluN2A, modificando la durata e l’intensità dell’apertura dei recettori. Mediante microscopia, il team ha mostrato che nel tempo più recettori NMDA si spostano nelle sinapsi, i punti di contatto tra neuroni, specialmente nelle colture BrainPhys. Misure geniche mirate hanno rivelato una diminuzione della sottounità «giovanile» GluN2B e un aumento della sottounità «tardiva» GluN2A, indicando che i neuroni stavano compiendo questo classico cambio di sviluppo.
Seguire correnti e calcio all’interno delle cellule
I test funzionali hanno confermato che questi cambiamenti molecolari sono rilevanti. Con elettrodi a punta fine, i ricercatori hanno registrato correnti elettriche scatenate da NMDA, una sostanza che attiva selettivamente i recettori NMDA. I neuroni di entrambe le condizioni di coltura mostravano correnti robuste, ma il blocco della sottounità GluN2A riduceva tali correnti di circa la metà, dimostrando che GluN2A era ormai un attore principale nel flusso di segnale. Il gruppo ha quindi monitorato il calcio, un importante messaggero interno, usando un colorante fluorescente. Esposte a NMDA, una frazione molto maggiore di neuroni cresciuti in BrainPhys ha mostrato forti picchi di calcio, e l’ampiezza del segnale era maggiore. L’analisi genica suggerisce il perché: le colture BrainPhys hanno sovraregolato più componenti dei canali del calcio e delle vie di rilascio, dotando le cellule della capacità di tradurre l’attivazione dei recettori NMDA in segnali di calcio ampi e coordinati.
Cosa significa per lo studio dei disturbi cerebrali
Nel loro insieme, questi risultati mostrano che i neuroni umani derivati da cellule staminali possono raggiungere uno stato funzionalmente maturo in soli due mesi, specialmente quando cresciuti in condizioni che favoriscono reti attive e una miscela realistica di neuroni e astrociti. In questo stato, la sottounità «di tipo adulto» GluN2A domina le correnti dei recettori NMDA e contribuisce fortemente alla segnalazione del calcio, proprio come nel cervello umano in sviluppo. Per i non specialisti, il messaggio è che i ricercatori dispongono ora di un modello di laboratorio più fedele di come i neuroni eccitatori umani maturano, si connettono e rispondono al glutammato. Ciò rende possibile indagare come sottili variazioni genetiche o processi patologici interrompano questi interruttori finemente regolati, aprendo una finestra su condizioni che vanno dall’epilessia alla malattia di Alzheimer e orientando la progettazione e la sperimentazione di future terapie.
Citazione: Escamilla, S., Avilés-Granados, C., Peralta, F.A. et al. GluN2A-mediated currents and calcium signal in human iPSC-derived neurons. Sci Rep 16, 9736 (2026). https://doi.org/10.1038/s41598-026-38482-y
Parole chiave: Recettori NMDA, neuroni da cellule staminali, sviluppo cerebrale, segnalazione del calcio, maturazione sinaptica