Clear Sky Science · it
L’inibitore doppio di G9a e antagonista del recettore H3 dell’istamina A-366 migliora i comportamenti ripetitivi e sociali e attenua la neuroinfiammazione nei topi BTBR T + tf/J
Perché questo studio sui topi è importante per l’autismo
Le famiglie che convivono con il disturbo dello spettro autistico (ASD) spesso si trovano ad affrontare un insieme di trattamenti che alleviano solo alcuni sintomi alla volta. Questo studio esplora un nuovo composto sperimentale, chiamato A-366, progettato per agire simultaneamente su due sistemi biologici molto diversi. In un modello murino ampiamente utilizzato per comportamenti simili all’autismo, A-366 ha ridotto azioni ripetitive, migliorato l’interazione sociale e placato l’infiammazione cerebrale, suggerendo la possibilità che in futuro un singolo farmaco possa affrontare insieme diverse caratteristiche fondamentali dell’ASD.
Una condizione con molte componenti
L’ASD non è una singola malattia con una causa unica. Comporta difficoltà nella comunicazione sociale, comportamenti ripetitivi e spesso altre sfide come ansia o problemi di attenzione. Dietro questi segni esteriori si nasconde un intreccio di alterazioni nella chimica cerebrale e nella regolazione genica. I farmaci attuali, come l’antipsicotico aripiprazolo, mirano principalmente ai sistemi di messaggeri cerebrali come dopamina e serotonina e sono approvati solo per sintomi associati, come l’irritabilità. Allo stesso tempo, la ricerca ha rivelato che il modo in cui il DNA è impacchettato e marcato chimicamente all’interno delle cellule cerebrali—l’epigenetica—cambia nell’ASD, così come l’attività delle risposte immunitarie e infiammatorie del cervello. Questi molteplici livelli suggeriscono che un approccio “un bersaglio alla volta” potrebbe essere troppo limitato.
Colpire sia gli interruttori genici sia i messaggeri cerebrali
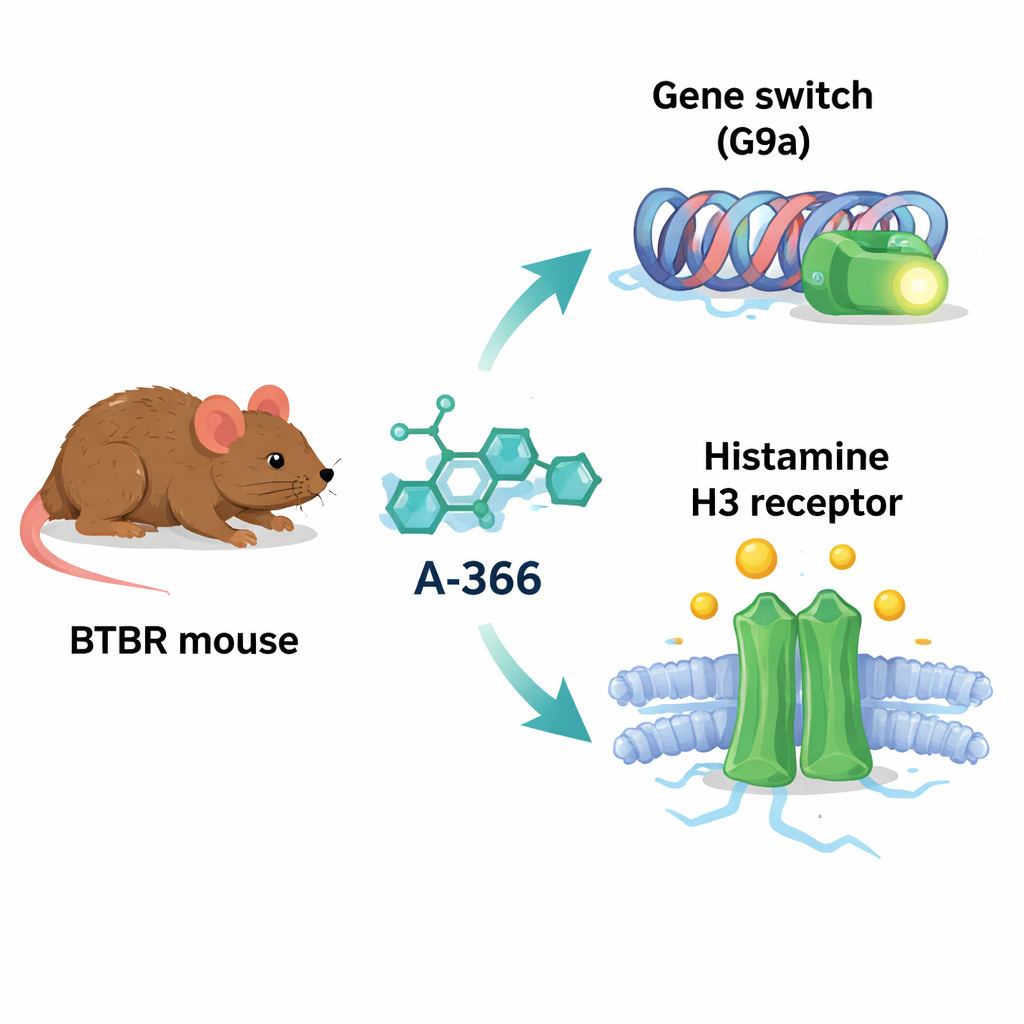
A-366 è stato sviluppato originariamente per bloccare una proteina chiamata G9a, un enzima che aggiunge marcature chimiche alle proteine istoniche e tende a reprimere l’espressione genica. In diversi disturbi cerebrali, l’attività di G9a e i suoi segni sono aumentati, potenzialmente silenziando geni importanti per l’apprendimento, la memoria e un corretto cablaggio cerebrale. In modo intrigante, la forma chimica di A-366 somiglia anche a quella di farmaci che bloccano il recettore H3 dell’istamina, un interruttore che controlla il rilascio di istamina e di altri neurotrasmettitori ed è stato collegato ad attenzione, veglia e comportamento sociale. A causa di questa sovrapposizione, gli autori hanno ipotizzato che A-366 potesse funzionare come un “agente doppio”: alleviando il dannoso silenziamento genico tramite l’inibizione di G9a e al contempo potenziando la segnalazione dell’istamina bloccando i recettori H3.
Mettere alla prova A-366 in topi con tratti autistico-simili
Il team ha lavorato con topi BTBR T+tf/J, una linea che mostra naturalmente bassa socievolezza, marcati comportamenti ripetitivi di pulizia e scavo e infiammazione cerebrale elevata—caratteristiche che riecheggiano aspetti chiave dell’ASD. I topi BTBR maschi hanno ricevuto iniezioni giornaliere di A-366 per tre settimane a tre dosi differenti e il loro comportamento è stato confrontato con topi C57 tipici e con topi BTBR trattati o con pitolisant (un antagonista standard del recettore H3) o con aripiprazolo. In diversi compiti, A-366 ha ridotto in modo dose-dipendente lo scavo ripetitivo, il distruggere materiale e l’auto-pulizia, e ha migliorato le prestazioni nel test dello Y-maze per la memoria di lavoro spaziale. In un test sociale a tre camere, A-366 non solo ha ristabilito la preferenza dei topi per trascorrere tempo con un altro topo rispetto a una gabbia vuota, ma alla dose più alta ha portato i punteggi sociali al livello dei topi tipici e ha superato gli effetti di pitolisant e aripiprazolo.
Calmare l’infiammazione e confermare i bersagli
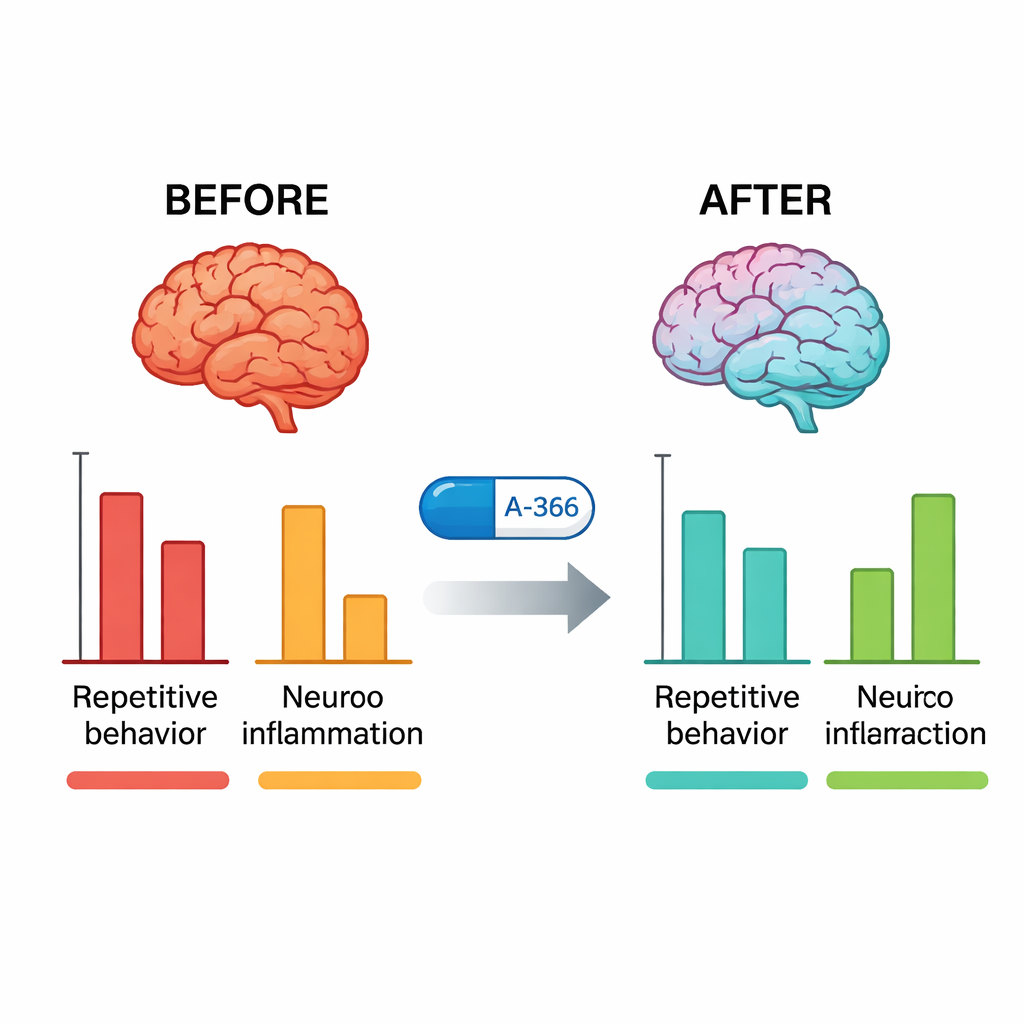
Dopo i test comportamentali, i ricercatori hanno esaminato i cervelli dei topi. Nei BTBR non trattati, l’attività di G9a nell’ippocampo e nel cervelletto era marcatamente più alta rispetto ai topi tipici. Il trattamento con A-366 ha ridotto nettamente questa attività verso valori normali, mentre il solo pitolisant non l’ha fatto, confermando che A-366 coinvolge effettivamente il suo bersaglio epigenetico. Allo stesso tempo, molecole infiammatorie chiave—TNF-α, IL-6 e IL-1β—erano fortemente elevate nei BTBR e sono state significativamente ridotte da A-366, più di quanto osservato con aripiprazolo. Quando gli scienziati hanno aggiunto un farmaco che attiva i recettori H3 (RAMH) oltre ad A-366, i benefici comportamentali e antiinfiammatori sono stati solo parzialmente invertiti, mentre la diminuzione dell’attività di G9a è rimasta. Questo schema supporta un meccanismo combinato: un sollievo epigenetico stabile tramite l’inibizione di G9a insieme a un contributo mediato dall’istamina tramite il blocco dei recettori H3.
Cosa potrebbe significare per i trattamenti futuri
Per un non specialista, questi risultati suggeriscono che potrebbe essere possibile progettare farmaci che agiscano contemporaneamente sia sul “software” sia sul “sistema di messaggistica” del cervello. In questo modello murino di comportamenti simili all’autismo, A-366 ha attenuato azioni ripetitive, migliorato l’impegno sociale e ridotto i segni di infiammazione cerebrale cronica agendo simultaneamente per allentare i dannosi spegnimenti genici e modulare la segnalazione dell’istamina. A-366 in sé è stato sviluppato per altre malattie e richiederebbe ottimizzazione e ampi test di sicurezza prima di qualsiasi uso umano. Tuttavia, fornisce un progetto per una nuova classe di farmaci multi-target mirati alla biologia complessa dell’ASD, dove finora affrontare un’unica via alla volta ha offerto sollievo limitato.
Citazione: Hajar, M., Jayaprakash, P., Stark, H. et al. The dual G9a inhibitor and histamine H3 receptor antagonist A-366 improves repetitive and social behaviors and attenuates neuroinflammation in BTBR T + tf/J mice. Sci Rep 16, 7105 (2026). https://doi.org/10.1038/s41598-026-38481-z
Parole chiave: disturbo dello spettro autistico, terapia epigenetica, recettore H3 dell’istamina, neuroinfiammazione, modello murino