Clear Sky Science · it
aFGF salva i fibroblasti senescenti indotti dall'iperglicemia e migliora la guarigione delle ferite diabetiche regolando la via SIRT1/STAT3
Perché le ferite a guarigione lenta sono importanti
Per molte persone con diabete, un piccolo taglio al piede o alla gamba può trasformarsi in una ferita ostinata che persiste per mesi, talvolta portando a infezioni o perfino all'amputazione. Queste lesioni croniche non sono solo un problema di superficie: le cellule della pelle che dovrebbero ricostruire il tessuto danneggiato spesso invecchiano prematuramente e smettono di funzionare correttamente. Questo studio esplora un approccio promettente per “ringiovanire” alcune di queste cellule usando un segnale di riparazione naturale, con l'obiettivo di aiutare le ferite diabetiche a chiudersi più rapidamente e in modo più completo.
Cellule che invecchiano troppo presto
La pelle sana dipende dai fibroblasti—cellule di supporto che vivono negli strati più profondi della pelle—per moltiplicarsi, spostarsi nella ferita e depositare la nuova impalcatura per il tessuto. Nel diabete, la glicemia elevata a lungo termine e le molecole danneggiate dallo zucchero spingono questi fibroblasti in uno stato chiamato senescenza cellulare. I fibroblasti senescenti non si dividono più bene, producono meno delle proteine strutturali necessarie alla riparazione e invece rilasciano un cocktail di fattori che promuovono l'irritazione e alimentano l'infiammazione continua. Gli autori mostrano che nei ratti diabetici, la pelle intorno a una ferita contiene più di questi fibroblasti invecchiati e meno delle proteine di matrice utili, correlando con un processo di guarigione significativamente più lento.
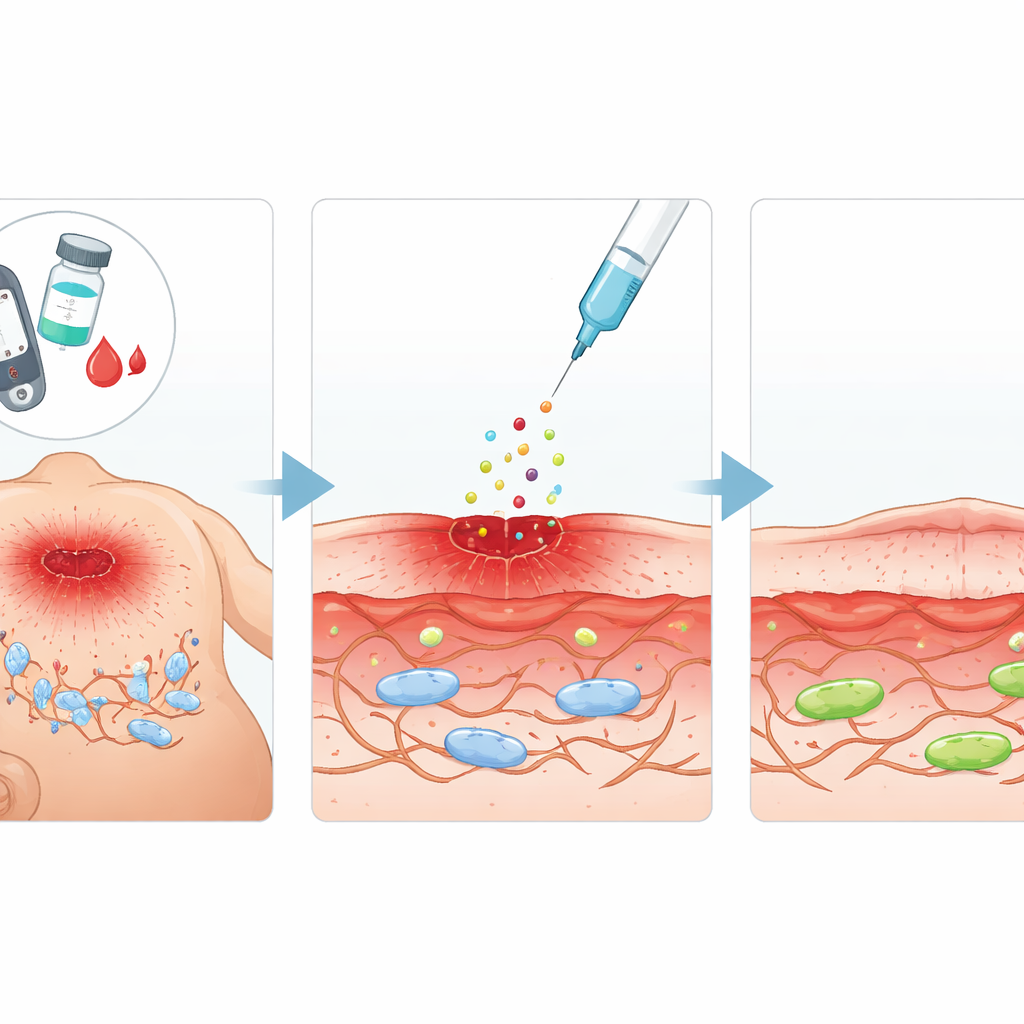
Un segnale di riparazione promettente
Il team si è concentrato sul fattore di crescita dei fibroblasti acido (aFGF), una proteina naturale nota per stimolare la crescita cellulare e la riparazione dei tessuti. Si sono chiesti se l'aFGF potesse non solo aumentare l'attività dei fibroblasti, ma anche invertire i cambiamenti simili all'invecchiamento causati dall'elevato zucchero. Nei ratti diabetici hanno creato ferite cutanee standardizzate e iniettato aFGF intorno all'area lesa ogni pochi giorni. Rispetto agli animali diabetici non trattati, i ratti trattati con aFGF hanno mostrato una più rapida riduzione della superficie della ferita, una migliore ricostruzione del tessuto sottostante e livelli inferiori di marcatori che segnalano la senescenza cellulare. In esperimenti di laboratorio paralleli, su una linea cellulare di fibroblasti murini esposta a glucosio molto elevato, l'aFGF ha ripristinato la capacità delle cellule di dividersi e migrare—due comportamenti essenziali per la chiusura di una ferita.
Calmare lo stress ossidativo all'interno delle cellule
L'iperglicemia fa più che fornire alle cellule carburante in eccesso: favorisce anche la sovrapproduzione di specie reattive dell'ossigeno, molecole instabili che danneggiano proteine, lipidi e DNA. Questo stress ossidativo è un importante innesco perché i fibroblasti diventino senescenti. I ricercatori hanno misurato diversi indicatori standard di questo stress nel loro modello cellulare, includendo sottoprodotti dannosi e l'attività degli enzimi antiossidanti propri della cellula. In condizioni di alto glucosio i fibroblasti mostravano più danni e difese antiossidanti più deboli. Quando è stato aggiunto l'aFGF, l'equilibrio è cambiato: i marcatori nocivi sono diminuiti e gli enzimi protettivi sono diventati più attivi. Ciò suggerisce che l'aFGF aiuta a ripristinare un ambiente interno più sano, rendendo meno probabile che i fibroblasti scivolino in uno stato di invecchiamento permanente.
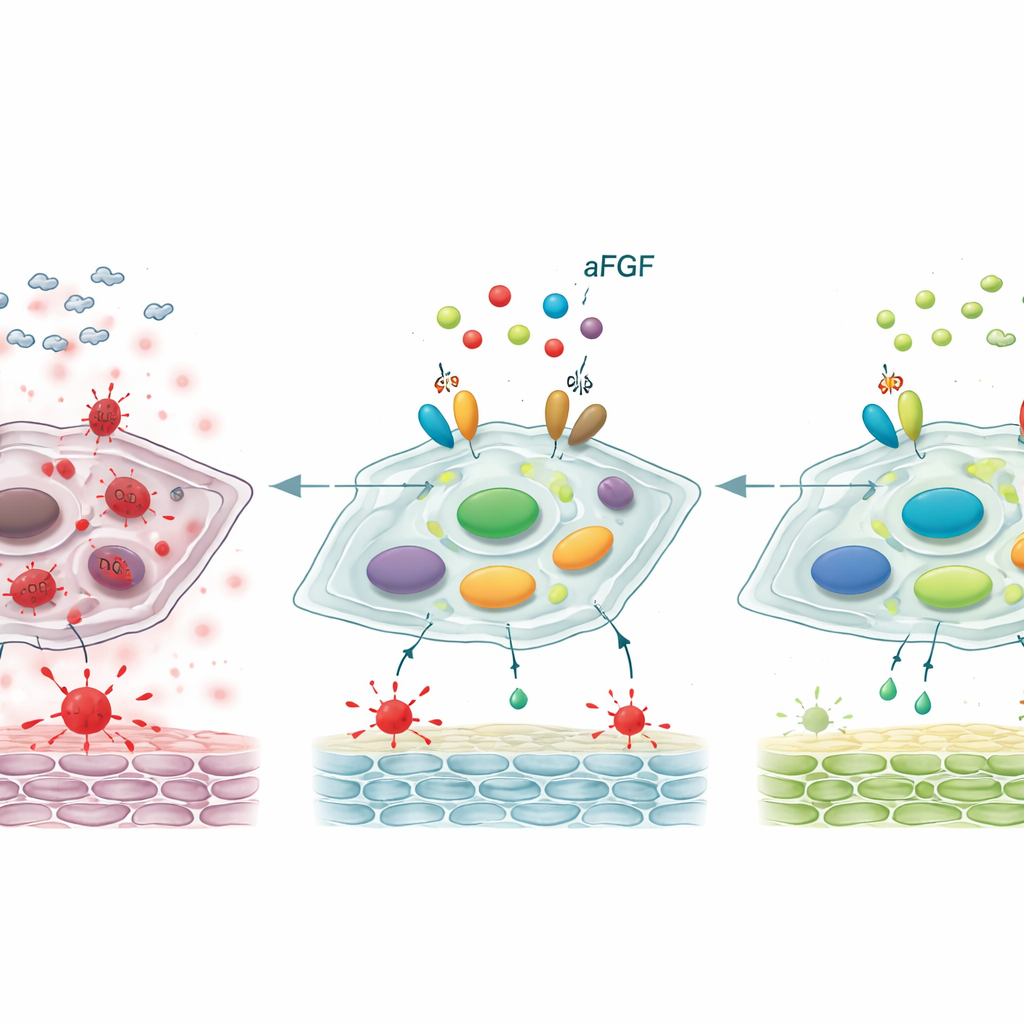
Ripristinare un interruttore di controllo chiave
Approfondendo, gli scienziati hanno esaminato un asse di controllo molecolare che coinvolge due proteine, SIRT1 e STAT3, che insieme influenzano se i fibroblasti restano giovanili o diventano senescenti. Nelle ferite diabetiche e nelle cellule trattate con alto glucosio, i livelli di SIRT1, un guardiano associato alla resistenza allo stress, risultavano ridotti, mentre la forma attivata di STAT3—un promotore di comportamenti infiammatori e legati all'invecchiamento—era aumentata. Il trattamento con aFGF ha invertito questo schema: SIRT1 è aumentato e STAT3 attivato è diminuito. Quando il team ha bloccato SIRT1 con un inibitore specifico, l'aFGF ha in larga misura perso la capacità di ridurre lo stress ossidativo, attenuare i marcatori di senescenza e accelerare la chiusura delle ferite nei ratti. Questo indica che gli effetti benefici dell'aFGF dipendono fortemente dal risveglio di SIRT1, che a sua volta mette freno a STAT3 e al programma di invecchiamento dannoso che controlla.
Cosa potrebbe significare per i pazienti
Nel complesso, i risultati suggeriscono che l'aFGF fa più che semplicemente stimolare la crescita cellulare. Sembra salvare i fibroblasti sovraccaricati nelle ferite diabetiche da un ciclo distruttivo di invecchiamento, attenuando lo stress ossidativo e ripristinando un interruttore molecolare chiave in modo che queste cellule possano nuovamente contribuire alla ricostruzione del tessuto. Pur essendo lavori condotti su ratti e cellule in coltura, e nonostante le ferite diabetiche reali siano ancora più complesse dei modelli usati qui, i risultati indicano l'aFGF come un candidato promettente per future terapie. Se benefici simili saranno confermati nell'uomo, una terapia con aFGF mirata potrebbe un giorno aiutare le ulcere croniche diabetiche a guarire più rapidamente, riducendo dolore, rischio di infezione e la probabilità di complicanze gravi.
Citazione: Wang, X., Lu, M., Jia, S. et al. aFGF rescues high glucose-induced senescent fibroblasts and improves diabetic wound healing by regulating SIRT1/STAT3 pathway. Sci Rep 16, 7856 (2026). https://doi.org/10.1038/s41598-026-38480-0
Parole chiave: guarigione delle ferite diabetiche, invecchiamento dei fibroblasti, stress ossidativo, terapia con fattori di crescita, via SIRT1 STAT3