Clear Sky Science · it
Esplorare i profili di espressione genica alla base dei fenotipi delle differenze dello sviluppo sessuale mediante analisi del trascrittoma
Perché questa ricerca ci riguarda tutti
La maggior parte di noi impara a scuola che il sesso biologico è determinato in modo semplice e binario: i cromosomi XX portano alla formazione di ovaie, gli XY alla formazione di testicoli. Questo studio mette in discussione quell'immagine ordinata. Leggendo quali geni sono attivi o inattivi nelle gonadi di persone con differenze dello sviluppo sessuale (DSD), i ricercatori rivelano una storia più sfumata in cui lo sviluppo sessuale umano assomiglia meno a un interruttore e più a uno spettro. Il loro lavoro offre una finestra su come si formano i corpi, perché alcune persone non rientrano nelle categorie tipiche maschile o femminile e come la medicina potrebbe comprendere e prendersi cura di loro in modo più adeguato.
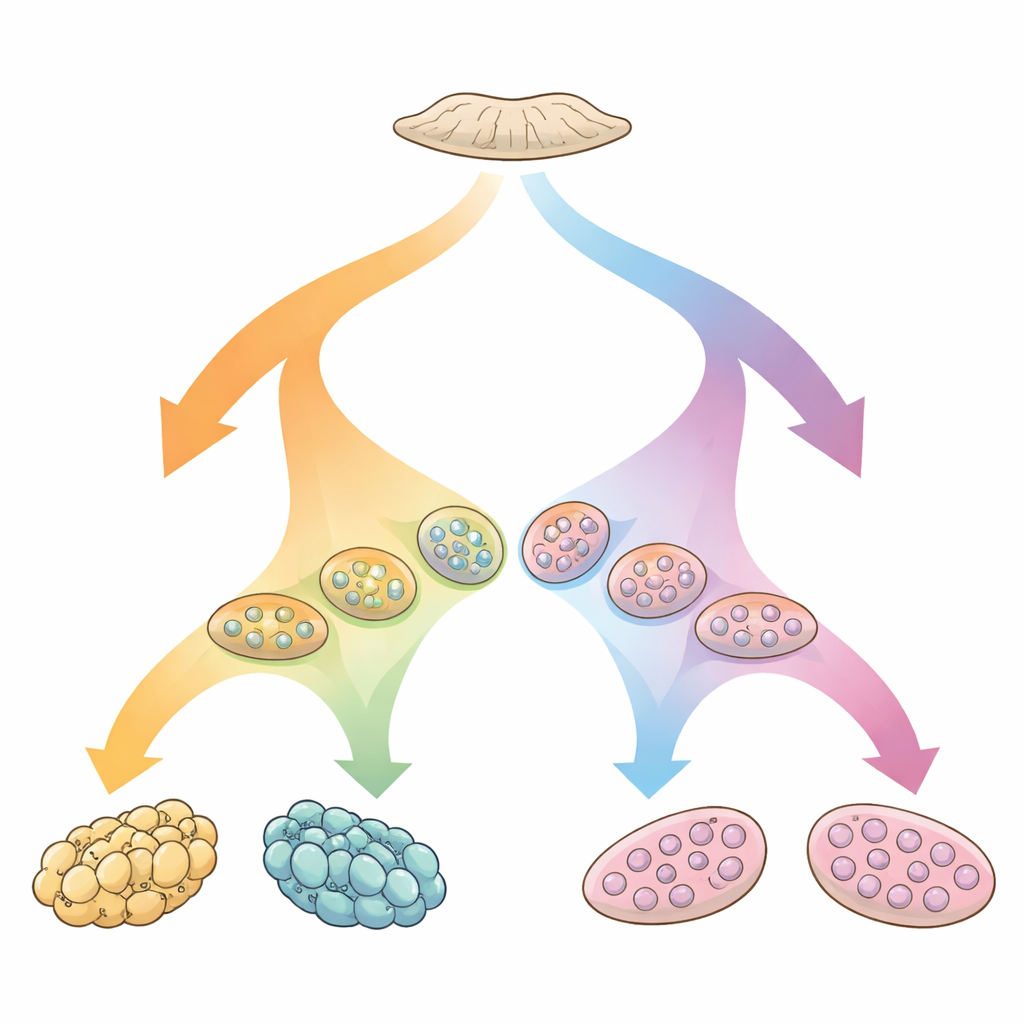
Un punto di partenza flessibile nei primi stadi della vita
Le gonadi iniziano la loro esistenza come una struttura “bipotente” flessibile che può diventare testicoli o ovaie. Una rete di geni e segnali spinge gradualmente questo tessuto in una direzione o nell'altra, plasmando infine la produzione ormonale e l'anatomia visibile. Quando una qualsiasi parte di questa rete viene perturbata, il risultato può essere una DSD, in cui cromosomi, gonadi e anatomia non coincidono nei modi usuali. Molte di queste condizioni restano ancora inspiegate a livello di DNA. Il gruppo dietro questo studio ha ipotizzato che osservare direttamente l'attività genica all'interno del tessuto gonadico potesse rivelare schemi che i test genetici classici non colgono, facendo luce su come questi organi effettivamente scelgono, o non riescono a scegliere, un percorso.
Ascoltare l'attività genica nelle gonadi
I ricercatori hanno analizzato tessuto gonadico di 11 individui con diverse condizioni DSD: disgenesia gonadica parziale, insensibilità completa agli androgeni e una forma chiamata DSD ovotesticolare, in cui una persona presenta tessuto di tipo testicolare e di tipo ovarico. Utilizzando il sequenziamento dell'RNA, hanno misurato i livelli di attività di decine di migliaia di geni e hanno confrontato questi schemi con dati di riferimento provenienti da testicoli e ovaie sani in fasi fetali, infantili e adulte. Un metodo di visualizzazione che raggruppa i campioni per somiglianza nei geni chiave dello sviluppo sessuale ha mostrato che i campioni DSD non si collocavano nettamente nei cluster maschili o femminili. Invece occupavano una zona intermedia, formando un proprio cluster tra testicoli e ovaie tipici. Alcuni campioni si avvicinavano di più al gruppo testicolare, altri a quello ovarico, suggerendo un range graduato di identità gonadiche.
Segnali misti all'interno delle gonadi
Quando il team ha esaminato i geni ben noti che indirizzano le gonadi verso testicolo o ovaio, ha scoperto che questi “cartelli” spesso non rientravano nei loro intervalli usuali. In individui 46,XY con disgenesia gonadica parziale o insensibilità agli androgeni, i geni necessari per lo sviluppo testicolare sano e la produzione di spermatozoi risultavano attenuati, mentre geni coinvolti in processi di sviluppo più generali erano aumentati, coerentemente con una formazione testicolare bloccata o incompleta. In persone 46,XX con DSD ovotesticolare, il quadro era ancora più misto: geni che normalmente promuovono lo sviluppo testicolare risultavano parzialmente attivati, mentre diversi geni associati all'ovaio erano ridotti. L'analisi su larga scala dei percorsi biologici ha fatto eco a questo schema. I processi specifici del testicolo, come la formazione degli spermatozoi, la divisione cellulare e il metabolismo energetico, erano indeboliti in molti casi 46,XY, mentre nei casi 46,XX ovotesticolari si osservava l'attivazione simultanea di percorsi legati sia al testicolo sia all'ovaio, rispecchiando le strutture miste viste al microscopio.
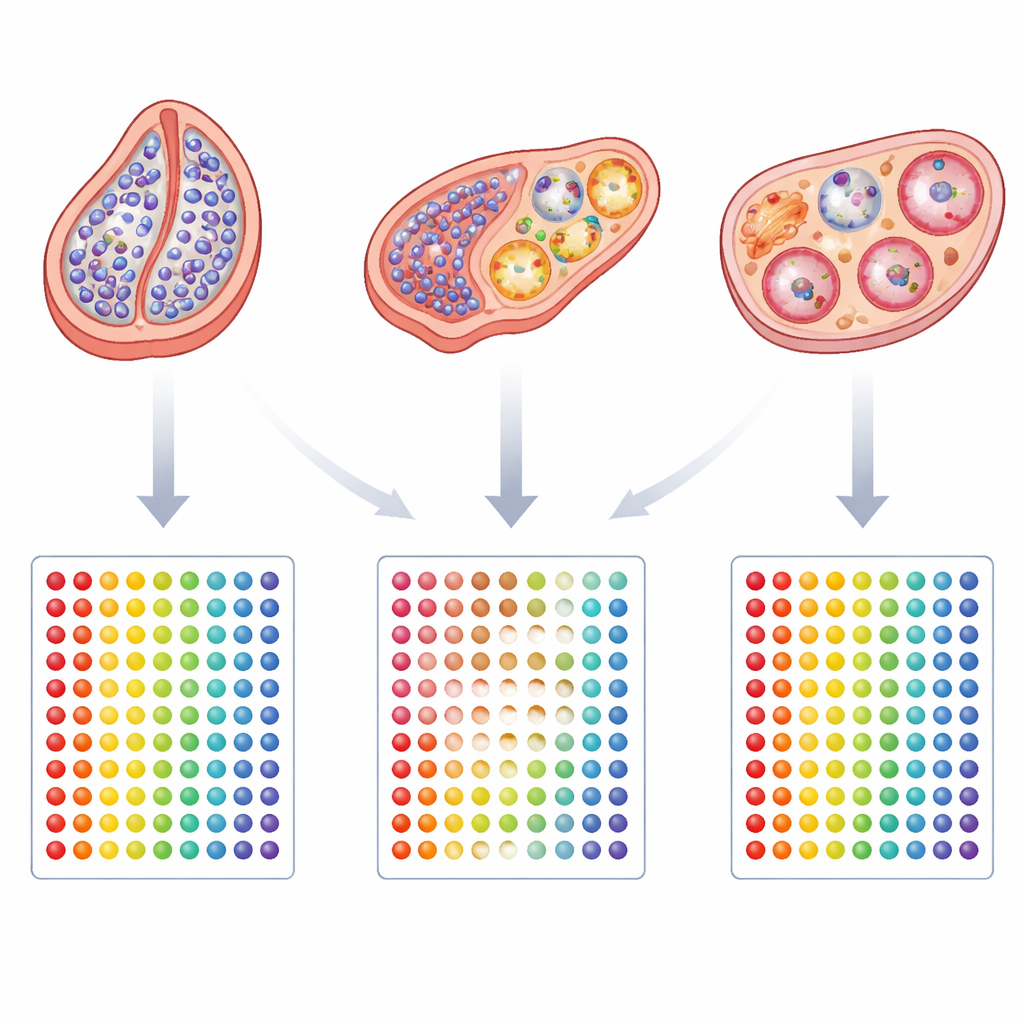
Un tema condiviso tra diverse condizioni
Nonostante la diversità delle presentazioni cliniche, è emersa una caratteristica ricorrente: una ridotta attività di un gene chiamato CBX2, che aiuta a organizzare il modo in cui il DNA è impacchettato e controlla ampi gruppi di geni determinanti il sesso. Esperimenti su animali avevano già mostrato che la perturbazione di questo regolatore può sfumare il confine tra sviluppo testicolare e ovarico. La sua costante downregulation in tutti i gruppi DSD suggerisce che l'instabilità a questo livello regolatorio possa favorire lo scostamento delle gonadi da un'identità chiaramente testicolare o ovarica verso uno stato intermedio. Lo studio evidenzia inoltre che alcuni pazienti più giovani mostrano ancora segnali di flessibilità nello sviluppo, con segnali più marcati nei percorsi di crescita e nelle prime fasi delle cellule germinali rispetto agli adulti, suggerendo che il timing può influenzare quanto fermamente la sorte gonadica venga consolidata.
Riconsiderare l'interruttore semplice
Per un osservatore non esperto, questa ricerca indica che le gonadi umane non si limitano a commutare tra due impostazioni fisse. Piuttosto, seguono uno spettro di schemi di attività genica che può posizionarsi in stati fortemente testicolari, fortemente ovarici o intermedi. Per le persone con DSD, questo significa che ciò che conta biologicamente non è solo il corredo cromosomico o l'aspetto esterno del corpo, ma anche come il loro tessuto gonadico si è sviluppato a livello molecolare. Mappando questi paesaggi interni, lo studio sostiene il superamento di una visione strettamente binaria dello sviluppo sessuale e per l'integrazione di test basati sull'RNA accanto al sequenziamento del DNA nel lavoro clinico futuro. Così facendo, offre una comprensione più sfumata e fondata sulla biologia del sesso, più aderente alla reale diversità osservata nei pazienti.
Citazione: Fabbri-Scallet, H., Calonga-Solís, V., Guerra-Júnior, G. et al. Exploring the underlying gene expression profiles of differences of sex development phenotypes through transcriptome analysis. Sci Rep 16, 8801 (2026). https://doi.org/10.1038/s41598-026-38435-5
Parole chiave: spettro dello sviluppo sessuale, trascrittoma gonadico, differenze dello sviluppo sessuale, profilazione dell'espressione genica, DSD ovotesticolare