Clear Sky Science · it
Scoperta in silico di un inibitore multi-target derivato da composti naturali per la terapia della malattia di Huntington
Un nuovo punto di vista su una malattia cerebrale devastante
La malattia di Huntington è un disturbo cerebrale raro ma devastante che progressivamente priva le persone del movimento, delle capacità cognitive e dell’indipendenza. I farmaci disponibili oggi possono alleviare alcuni sintomi, ma non arrestano né ribaltano la malattia. Questo studio esplora un nuovo approccio guidato dal calcolo per cercare terapie: individuare un singolo composto naturale capace di agire su più punti deboli del processo patologico contemporaneamente — un metodo che potrebbe risultare più efficace rispetto ai farmaci mirati a un solo bersaglio.
Perché la malattia di Huntington è così difficile da trattare
La malattia di Huntington è causata da un gene difettoso che porta al progressivo deterioramento dei neuroni, di solito a partire dalla mezza età. Nelle fasi iniziali, le persone possono notare cambiamenti dell’umore, piccoli movimenti involontari o lievi difficoltà nella pianificazione e nell’attenzione. In un arco di 10–12 anni, questo può evolvere in gravi problemi motori, perdita della parola, demenza e totale dipendenza dai caregiver. Gli scienziati sanno che molti processi cellulari vanno in tilt nella malattia di Huntington: la produzione di energia si indebolisce, proteine dannose si aggregano e i segnali chimici tra le cellule diventano tossici. Poiché così tante vie sono compromesse contemporaneamente, una strategia «un proteina, un farmaco» ha faticato a produrre risultati concreti.
Tre punti critici nel cervello
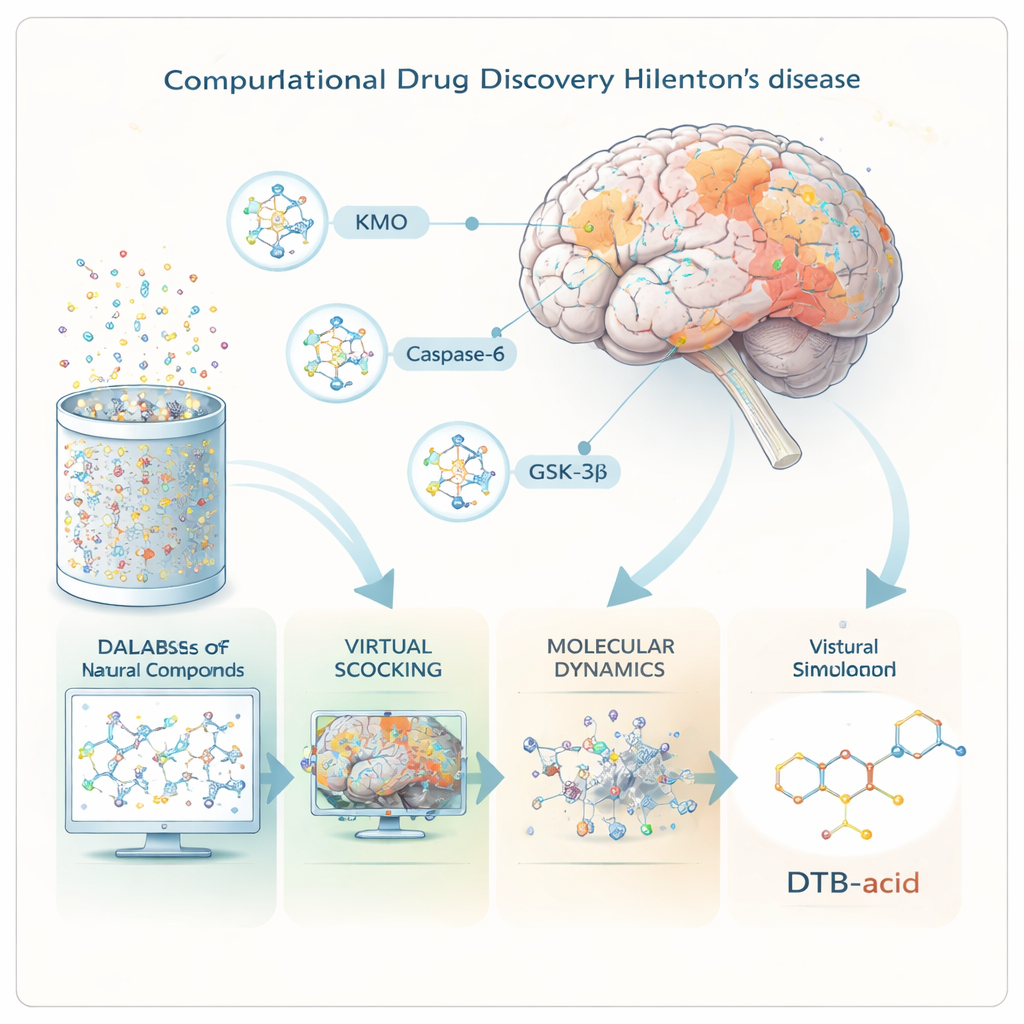
I ricercatori si sono concentrati su tre proteine che occupano punti di controllo chiave nella malattia di Huntington. La prima, KMO, regola la degradazione dell’amminoacido triptofano verso sottoprodotti tossici o protettivi; quando questo equilibrio si sposta verso i tossici, i neuroni ne risentono. La seconda, Caspasi-6, taglia la proteina huntingtina mutata in frammenti più piccoli e altamente tossici che si accumulano precocemente nella malattia. La terza, GSK-3β, è un enzima di segnalazione associato ad aggregati proteici anomali e morte cellulare in diversi disturbi cerebrali. Trovando una molecola che possa ridurre simultaneamente l’attività dannosa di tutte e tre, il team sperava di progettare una terapia più in linea con la complessità della malattia.
Setacciare la libreria della natura con i supercalcolatori
Invece di mescolare sostanze in provetta, gli scienziati hanno lavorato interamente «in silico», usando software avanzati per modellare il comportamento delle molecole. Hanno iniziato con oltre 695.000 composti naturali estratti da un database pubblico, preparando ciascuno in forma tridimensionale. Strumenti di screening virtuale potenti hanno quindi previsto quali composti erano in grado di attraversare la barriera emato-encefalica, comportarsi come veri farmaci nell’organismo ed evitare principali problemi di sicurezza. Solo circa 60.000 hanno superato questi filtri e sono stati testati, al computer, per quanto potessero adattarsi comodamente nelle tasche di legame delle tre proteine target.
Una molecola spicca: DTB-acido
Da questa ricerca enorme, una molecola — chiamata DTB-acido, un alcaloide naturale correlato all’acido matrinico — è emersa come la più promettente. Studi di docking dettagliati hanno mostrato che il DTB-acido può formare contatti forti e ben posizionati all’interno di tutte e tre le proteine. Successivamente, il team ha eseguito lunghe simulazioni di dinamica molecolare, che imitano il moto degli atomi in acqua nel tempo, per verificare se il composto sarebbe rimasto stabile invece di allontanarsi. In 100 miliardesimi di secondo di moto simulato, i complessi proteina–farmaco sono rimasti stabili. Calcoli energetici aggiuntivi hanno suggerito che il legame con KMO fosse particolarmente forte, mentre un’analisi separata delle molecole d’acqua nei siti di legame ha indicato che le interazioni con GSK-3β erano anche termodinamicamente favorevoli.
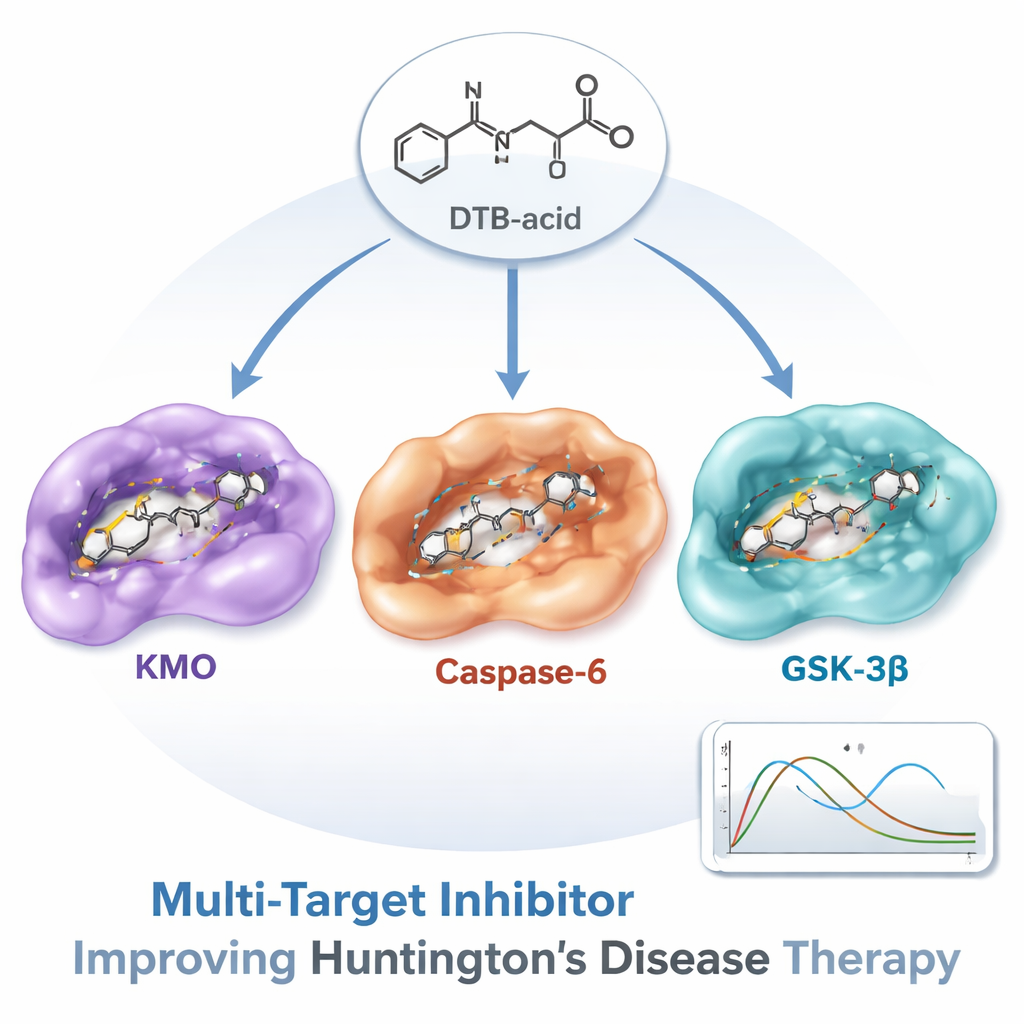
Dal colpo in silico al futuro farmaco
Naturalmente, una molecola che appare promettente su uno schermo è solo un primo passo. Gli autori sottolineano che il DTB-acido deve ancora essere testato in cellule e animali per confermare che raggiunge il cervello, colpisce i bersagli previsti e protegge effettivamente i neuroni senza effetti collaterali dannosi. Pur così, questo lavoro dimostra una strada potente ed efficiente per scoprire farmaci multi-target per malattie cerebrali complesse. Per i non specialisti, il messaggio chiave è che invece di trattare la malattia di Huntington con una serie di farmaci separati e strettamente mirati, potrebbe essere possibile progettare un singolo composto accuratamente tarato come il DTB-acido che affronta contemporaneamente diversi fattori di danno — offrendo nuova speranza per rallentare o modificare il corso di questo disturbo implacabile.
Citazione: Zheng, B., Banday, M., Gangwar, S. et al. In silico discovery of natural compound-derived multi-target inhibitor for Huntington’s disease therapy. Sci Rep 16, 7716 (2026). https://doi.org/10.1038/s41598-026-38430-w
Parole chiave: Malattia di Huntington, farmaco multi-target, scoperta di farmaci computazionale, composti naturali, neurodegenerazione