Clear Sky Science · it
Screening integrato multi-database per predire la prognosi e identificare bersagli di immunoterapia nei pazienti con carcinoma epatocellulare
Perché questo è importante per le persone con cancro al fegato
Il carcinoma epatocellulare, la forma più comune di cancro primario del fegato, causa centinaia di migliaia di decessi ogni anno. Molti pazienti con lo stesso stadio di malattia rispondono in modo molto diverso ai trattamenti, in particolare alle moderne immunoterapie che mirano a liberare il sistema immunitario dell’organismo. Questo studio pone una domanda semplice ma cruciale: possiamo leggere l’attività genica di un tumore come un’impronta digitale per prevedere chi avrà un decorso peggiore, chi risponderà ai farmaci a base immunitaria e quali geni potrebbero essere i migliori nuovi bersagli terapeutici?
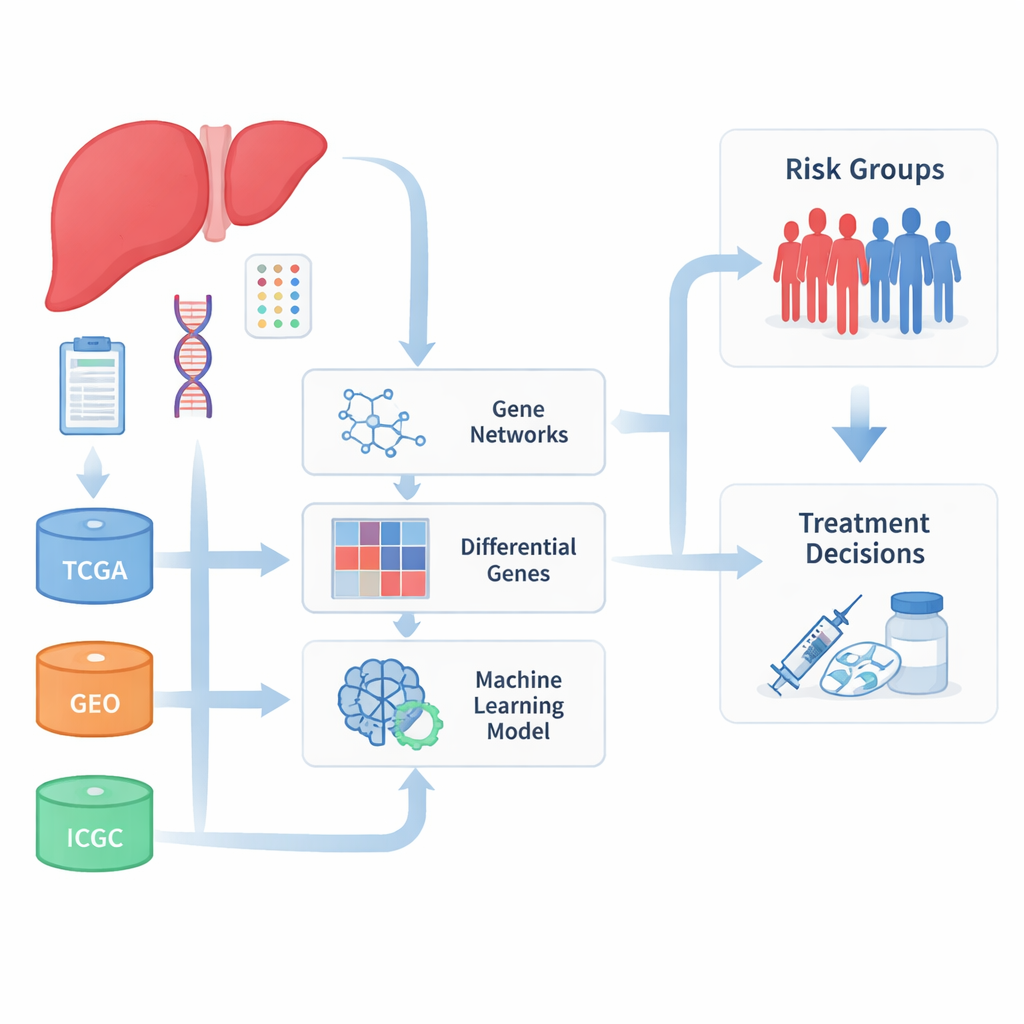
Mettere insieme molti dataset
I ricercatori hanno cominciato raggruppando grandi raccolte di campioni di carcinoma epatocellulare provenienti da vari database internazionali che archiviano l’attività genica tumorale e gli esiti clinici. Combinando dati da The Cancer Genome Atlas, dall’International Cancer Genome Consortium e da diversi studi presenti nel Gene Expression Omnibus, hanno costituito un insieme di pazienti molto più ampio e diversificato di quanto potrebbe fare un singolo ospedale o progetto. Poiché questi dataset sono stati prodotti in laboratori diversi e con metodi differenti, il gruppo ha dedicato inizialmente notevoli sforzi a correggere le differenze tecniche, in modo che fossero segnali biologici reali e non rumore di laboratorio a orientare i risultati.
Trovare pattern genici legati all’esito
Con i dati puliti a disposizione, il team ha cercato gruppi di geni che tendessero ad accendersi e spegnersi insieme e che fossero anche correlati agli esiti clinici dei pazienti. Usando un approccio in stile rete, hanno raggruppato migliaia di geni in moduli e si sono poi concentrati su quei moduli più fortemente legati al comportamento del tumore e alla sopravvivenza dei pazienti. Hanno inoltre confrontato i tumori con il tessuto non tumorale per identificare geni chiaramente più o meno attivi nel cancro. L’intersezione tra queste due visuali ha prodotto un insieme di 93 geni che risultavano sia alterati nel carcinoma epatocellulare sia strettamente connessi a caratteristiche chiave della malattia, molti dei quali coinvolti nel metabolismo dei farmaci e nella gestione di sostanze tossiche da parte del fegato.
Costruire un punteggio di rischio a dieci geni
Per trasformare queste liste geniche in qualcosa che i medici possano eventualmente usare, gli autori si sono rivolti all’apprendimento automatico. Hanno testato più di cento combinazioni di algoritmi per la selezione delle caratteristiche e per la previsione della sopravvivenza, valutandoli in base a quanto accuratamente separavano i pazienti in gruppi con esito migliore o peggiore su più coorti indipendenti. Da questa vasta ricerca hanno distillato una firma compatta di dieci geni che insieme formavano un punteggio di rischio. I pazienti con punteggi alti avevano sistematicamente una sopravvivenza globale, libera da malattia e libera da progressione più breve, sia nei dataset principali sia nei gruppi di validazione esterni. Tra questi geni, TYMS è emerso come un forte indicatore di prognosi sfavorevole, mentre APOL3 e FBXO2 sono stati collegati a esiti più favorevoli.
Indizi dal vicinato immunitario del tumore
Lo studio è andato oltre la predizione per chiedersi perché questi geni siano importanti. Utilizzando diversi strumenti computazionali, il team ha stimato quali tipi di cellule immunitarie fossero presenti in ciascun tumore e quanto il punteggio a dieci geni fosse correlato a quel paesaggio immunitario. I tumori ad alto rischio tendevano a mostrare pattern immunitari e cambiamenti genici associati a un maggior carico mutazionale e a segni di fuga immunitaria, inclusi legami con molecole checkpoint ben note come PD-1 e CTLA-4. Hanno inoltre esaminato i profili di mutazione reali e riscontrato che i tumori ad alto rischio presentavano alterazioni più frequenti in driver classici del cancro come TP53. Infine, esami del sangue in pazienti e volontari sani hanno confermato che TYMS era aumentato e FBXO2 ridotto nelle persone con carcinoma epatocellulare, supportando l’idea che questi geni siano biologicamente attivi nella malattia e non semplici artefatti statistici.
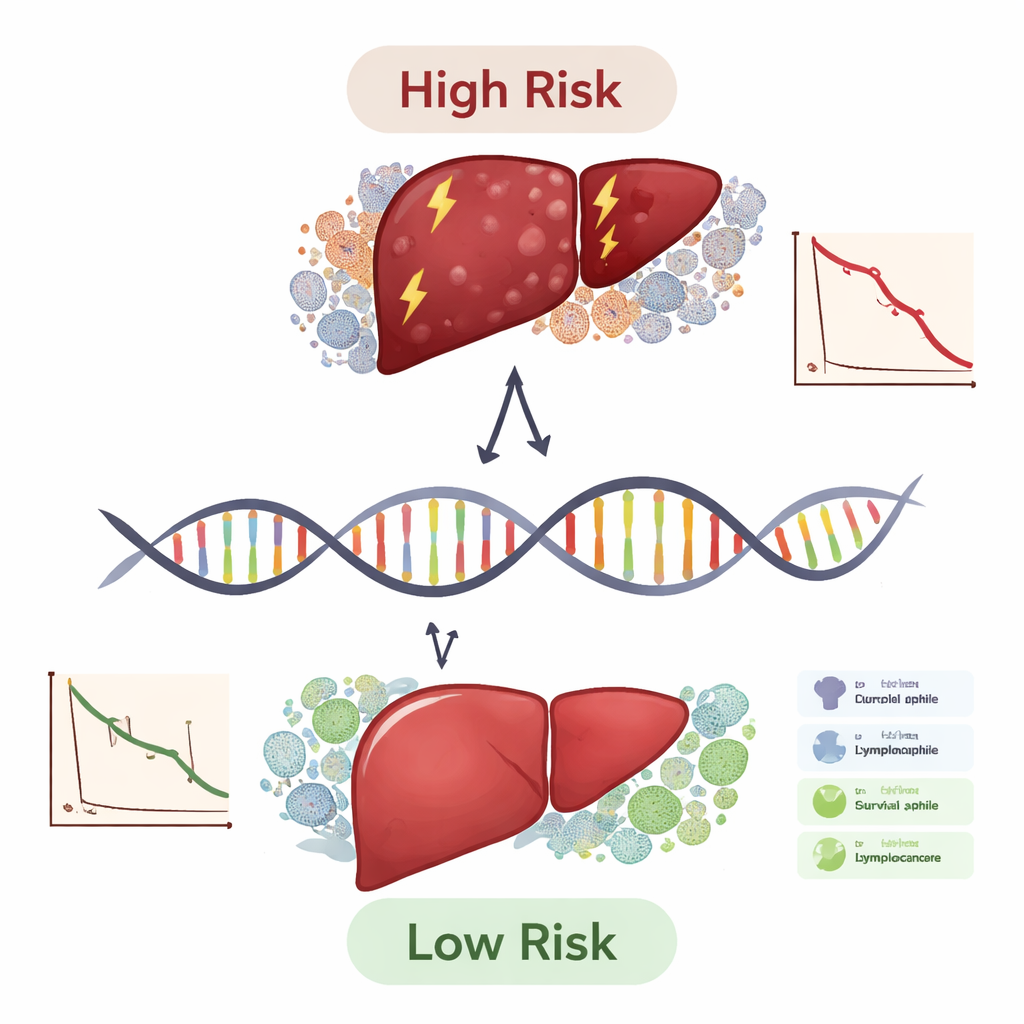
Cosa significa per pazienti e medici
In termini pratici, questo lavoro offre un modello per usare un piccolo pannello di geni per classificare i pazienti con carcinoma epatocellulare in gruppi di rischio e per suggerire chi potrebbe beneficiare maggiormente dei trattamenti immunoterapici. Il punteggio a dieci geni non è ancora un test pronto per la clinica, ma ha avuto prestazioni migliori rispetto ai soli sistemi di stadiazione standard ed è rimasto utile attraverso diversi sottogruppi di pazienti. Proprio come i pannelli per il colesterolo guidano la prevenzione delle malattie cardiache, un pannello genico come questo potrebbe un giorno aiutare gli oncologi a scegliere terapie più aggressive per i pazienti ad alto rischio, risparmiare ai pazienti a basso rischio effetti collaterali non necessari e indirizzare gli sviluppatori di farmaci verso nuovi bersagli come TYMS, APOL3 e FBXO2. Saranno necessari studi prospettici più ampi e esperimenti di laboratorio, ma questa analisi integrata segna un passo significativo verso una cura del carcinoma epatocellulare più personalizzata e guidata dalla biologia.
Citazione: Zhou, L., Zhang, W., Liu, Z. et al. Integrated multi-dataset screening to predict prognosis and identify immunotherapy gene targets in hepatocellular carcinoma patients. Sci Rep 16, 7014 (2026). https://doi.org/10.1038/s41598-026-38424-8
Parole chiave: carcinoma epatocellulare, firma genica, immunoterapia, prognosi, microambiente tumorale