Clear Sky Science · it
CNOT2 /c-Myc/STAT3 segnala in modo critico coinvolto nell'apoptosi mediata dalla glicolisi indotta da benzil isotiocianato nel carcinoma epatocellulare
Un ingrediente anti-cancro nel tuo piatto
Il benzil isotiocianato, abbreviato BITC, è una sostanza naturale presente in verdure comuni come broccoli, cavoli e cavolo riccio. Sebbene i medici sappiano da tempo che chi consuma più di questi alimenti tende ad avere tassi di tumore inferiori, i meccanismi con cui specifici componenti vegetali rallentano o uccidono le cellule tumorali sono ancora in fase di definizione. Questo studio analizza come il BITC influenzi cellule di carcinoma epatocellulare in laboratorio e mette in luce un legame sorprendente tra il modo in cui le cellule tumorali metabolizzano lo zucchero e la loro induzione all'autodistruzione.
Perché il cancro al fegato ha bisogno di opzioni migliori
Il cancro al fegato è uno dei tumori più letali a livello mondiale, e il carcinoma epatocellulare è la sua forma più comune. Anche con chirurgia, chemioterapia e farmaci mirati, molti tumori recidivano o smettono di rispondere alle terapie. Una ragione è che le cellule tumorali riorganizzano l'uso dell'energia: invece di fare affidamento principalmente sull'ossigeno nei loro mitocondri, bruciano grandi quantità di zucchero molto rapidamente in un processo spesso chiamato “effetto Warburg”. Questo uso distorto dello zucchero aiuta le cellule tumorali a crescere più velocemente e a resistere alla morte. Trovare modi sicuri per interrompere questa linea di approvvigionamento energetico, specialmente usando molecole derivate dagli alimenti, è una strategia attraente.
Testare un composto vegetale sulle cellule di cancro al fegato
I ricercatori hanno trattato due linee cellulari umane di carcinoma epatocellulare, SK-Hep1 e Huh7, con dosi crescenti di BITC. All'aumentare della dose, il numero di cellule sopravvissute è diminuito, dimostrando che il BITC è tossico per queste cellule nelle condizioni testate. Analizzando più nel dettaglio cosa accadeva all'interno delle cellule, hanno osservato i segni classici della morte cellulare programmata, o apoptosi. Proteine chiave che normalmente esistono in una forma “inattiva” prima di essere clivate durante l'apoptosi, come PARP e caspasi-3, sono risultate ridotte nelle loro forme intatte, o “pro-”. I test di citometria a flusso hanno inoltre mostrato un aumento delle cellule nella frazione sub-G1 del ciclo cellulare e più cellule positive per Annexin V, entrambi indicatori che le cellule tumorali stavano andando incontro ad apoptosi attiva piuttosto che a semplice danno.
Spegnere la brama di zucchero del cancro
Il gruppo ha quindi esaminato se il BITC stesse alterando l'effetto Warburg. Hanno misurato le proteine che aiutano le cellule tumorali a consumare zucchero e convertirlo in energia e lattato—in particolare HK2, PKM2 e LDH. Il trattamento con BITC ha ridotto i livelli di tutte e tre nelle due linee cellulari e ha diminuito la quantità di lattato rilasciata e di glucosio consumato dal mezzo di coltura. In altre parole, il BITC ha reso le cellule di carcinoma epatocellulare meno efficaci nell'alimentare il loro motore glicolitico ad alta velocità. Quando gli scienziati hanno aggiunto piruvato, un prodotto a valle della degradazione degli zuccheri che può ancora alimentare il metabolismo cellulare, molti effetti del BITC sono stati invertiti: le cellule hanno recuperato livelli più alti di PARP, caspasi-3 e degli enzimi della glicolisi. Questo recupero suggerisce che l'interferenza con l'elaborazione dello zucchero è una componente chiave del modo in cui il BITC induce la morte cellulare.
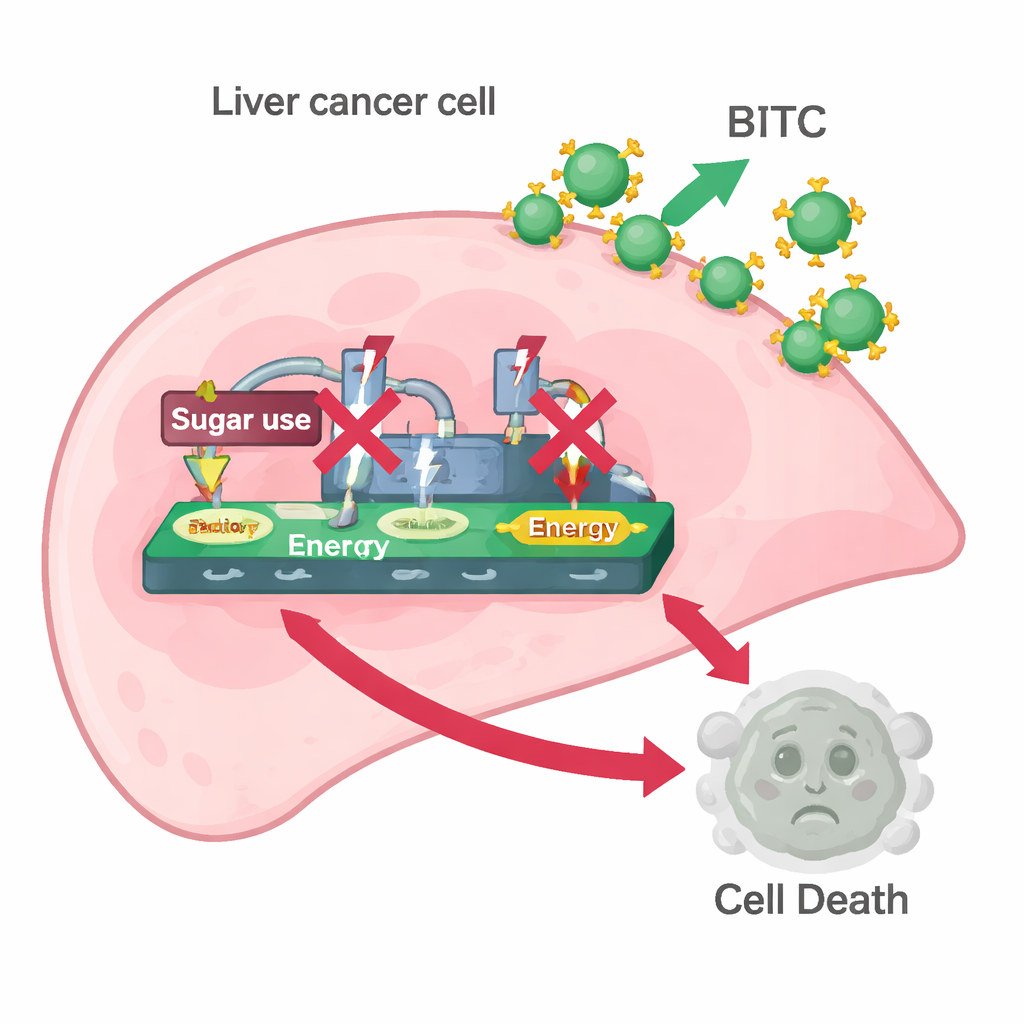
Sciogliere gli interruttori di controllo all'interno della cellula
Per capire livelli di controllo più profondi, i ricercatori si sono concentrati su un trio di segnali: CNOT2, c-Myc e STAT3. Queste proteine promuovono crescita, sopravvivenza e il riprogrammamento metabolico in molti tumori. Dati provenienti da pazienti con carcinoma epatocellulare hanno mostrato che CNOT2 tende a essere più elevato in persone con esiti peggiori. In laboratorio, il trattamento con BITC ha diminuito la forma attiva e fosforilata di STAT3, il suo attivatore a monte JAK1, la proteina promotrice della crescita c-Myc e lo stesso CNOT2. L'uso di strumenti genetici per ridurre i livelli di CNOT2 o STAT3 ha reso l'effetto citotossico del BITC ancora più marcato, abbassando ulteriormente PARP e caspasi-3. Esperimenti di binding proteico hanno rivelato che il BITC interrompeva anche le interazioni fisiche tra CNOT2 e STAT3 e tra CNOT2 e c-Myc. Quando CNOT2 o c-Myc venivano artificialmente sovraespressi, il BITC perdeva gran parte della sua capacità di sopprimere gli enzimi glicolitici e indurre l'apoptosi, sottolineando come questo asse di segnalazione funzioni come un interruttore maestro che collega il metabolismo degli zuccheri alla sopravvivenza.
Cosa potrebbe significare per le terapie future
Nel complesso, i risultati dipingono un quadro coerente: il BITC aggredisce le cellule di carcinoma epatocellulare tagliando la loro preferita linea di carburante a base di zucchero e attivando interruttori di morte cellulare che dipendono dall'asse CNOT2/c-Myc/STAT3. Bloccando sia i segnali di crescita sia l'uso dello zucchero, il BITC spinge le cellule tumorali oltre una soglia metabolica verso l'apoptosi. Questi risultati provengono da esperimenti in colture cellulari, non da pazienti, e sono state studiate solo due tipologie cellulari di cancro al fegato, quindi sono necessari molti altri studi su animali e in clinica. Tuttavia, la ricerca rafforza l'idea che alcuni composti presenti nelle verdure di uso quotidiano potrebbero essere raffinati o combinati con altri trattamenti per affamare più precisamente i tumori epatici incoraggiandone al contempo l'autodistruzione.
Citazione: Koh, W., Park, SY., Kim, B. et al. CNOT2 /c-Myc/STAT3 signaling is critically involved in glycolysis mediated apoptosis of benzyl isothiocyanate in hepatocellular carcinoma. Sci Rep 16, 7000 (2026). https://doi.org/10.1038/s41598-026-38416-8
Parole chiave: cancro del fegato, benzil isotiocianato, metabolismo tumorale, apoptosi, verdure crocifere