Clear Sky Science · it
Analisi algoritmica della struttura dei tumori odontogenici misti
Perché contano i piccoli tumori della mascella
La maggior parte di noi pensa ai denti solo quando fanno male o devono essere otturati, ma i tessuti che formano i denti possono occasionalmente dare origine a tumori rari. Queste formazioni, chiamate tumori odontogenici, sono poco comuni ma importanti perché possono danneggiare le mascelle e risultare difficili da diagnosticare al microscopio. Questo studio si chiede se gli algoritmi moderni possano misurare l’architettura di questi tumori con precisione tale da aiutare i patologi a distinguere lesioni simili e a comprendere meglio il loro comportamento.
Crescite rare che imitano denti in formazione
I tumori odontogenici insorgono solo nelle regioni delle mascelle destinate a formare i denti. Il gruppo si è concentrato su un piccolo insieme denominato tumori odontogenici misti, che contengono sia lo strato cellulare che normalmente dà origine allo smalto (epitelio) sia il tessuto di supporto per la formazione del dente (ectomesenchima). All’interno di questo gruppo, tre lesioni—tumore odontogenico primordiale (POT), fibroma ameloblastico (AF) e odontoma in sviluppo (DO)—possono assomigliarsi notevolmente tra loro e ai normali abbozzi dentari, le strutture iniziali da cui si sviluppano i denti. Il POT è particolarmente nuovo per la scienza, essendo stato riconosciuto formalmente dall’Organizzazione Mondiale della Sanità solo nel 2017, e rimane così raro che ogni caso aggiuntivo è rilevante per raffinare la sua definizione.
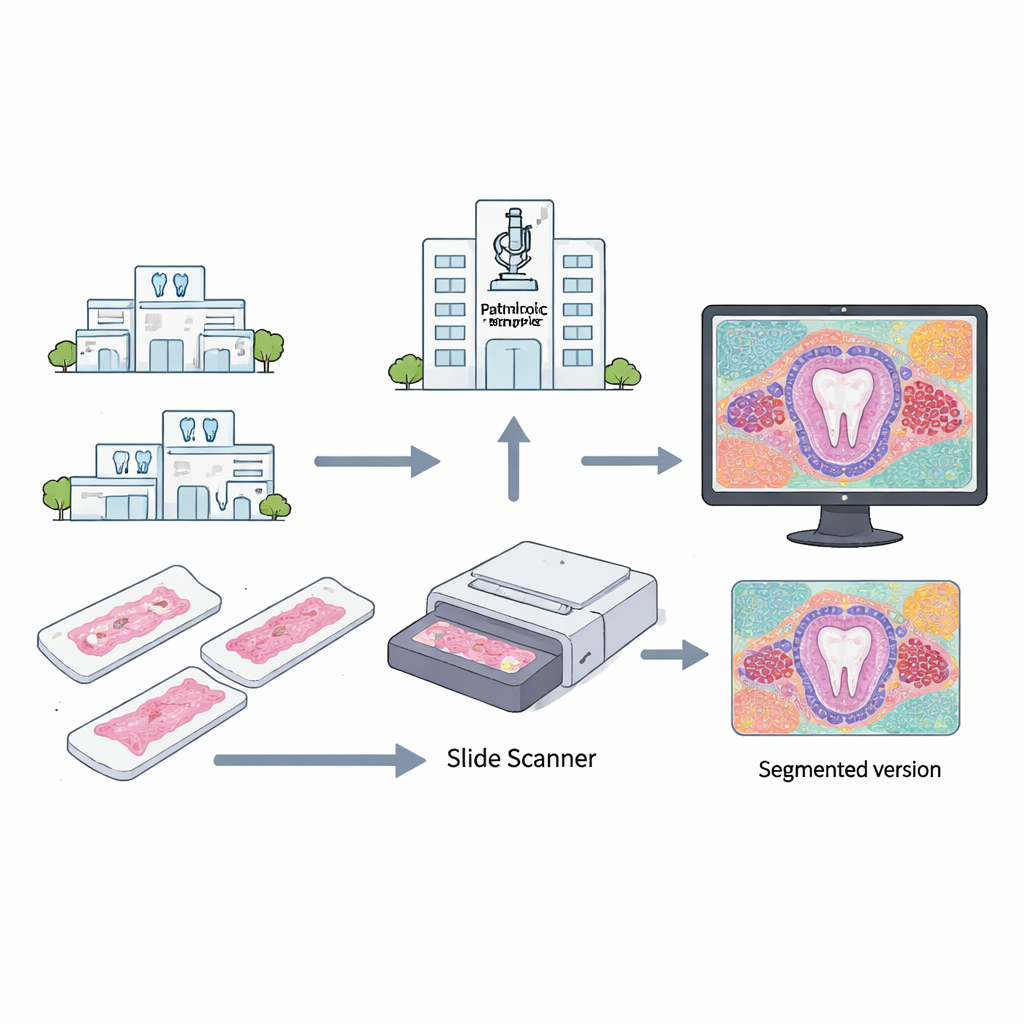
Trasformare i vetrini in mappe misurabili
Per andare oltre i limiti dell’osservazione a occhio sui vetrini, i ricercatori hanno digitalizzato campioni bioptici di 15 tumori odontogenici misti (cinque ciascuno di POT, AF e DO) e cinque abbozzi dentari normali. Dopo la colorazione del tessuto con le tecniche abituali, hanno scansionato i vetrini ad alto ingrandimento e utilizzato software di analisi delle immagini per localizzare ogni nucleo cellulare. Da lì, strumenti matematici noti come trasformate watershed hanno definito una sorta di “zona di influenza” attorno a ciascun nucleo, creando migliaia di “cellule virtuali” le cui dimensioni e forme potevano essere misurate automaticamente. Impilando e allineando le immagini, il team ha anche esaminato quanto fossero compatti i nuclei a diverse profondità al di sotto degli strati superficiali del tessuto.
Cosa hanno visto gli algoritmi dentro i tumori
Nel POT, le mappe di densità derivate dal computer hanno confermato un marcato affollamento cellulare appena sotto lo strato superficiale di epitelio, con i nuclei più compatti nel terzo superiore del tessuto e un assottigliamento verso il centro. Questo schema—chiamato condensazione subepiteliale—era presente nella maggior parte dei campioni di POT ma assente in una minoranza che non mostrava la banda densa. I nuclei nel tessuto di supporto erano leggermente più grandi rispetto a quelli dell’epitelio, ma entrambi i compartimenti avevano forme arrotondate simili. Quando il team ha confrontato le cellule virtuali tra tutte le entità, ha rilevato che le cellule virtuali epiteliali erano sempre le più piccole, riflettendo la loro maggiore densità di impacchettamento, mentre le regioni più profonde contenevano cellule virtuali molto più grandi. L’odontoma in sviluppo ha mostrato la maggiore dispersione nelle aree delle cellule virtuali epiteliali, con valori medi generalmente maggiori rispetto alle altre lesioni, mentre il fibroma ameloblastico tendeva ad avere i valori più piccoli.
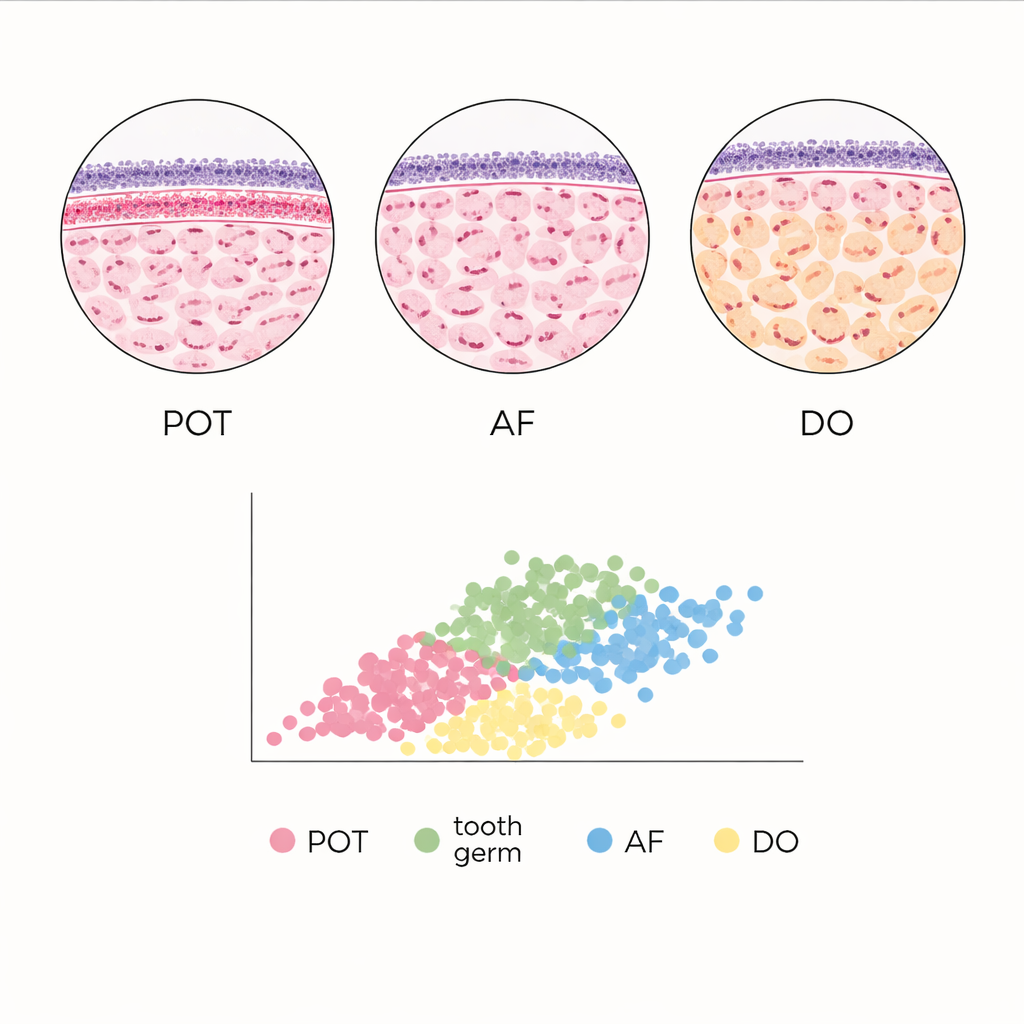
Lo sviluppo dentario normale come riferimento
Per contestualizzare questi tumori, gli autori li hanno confrontati con abbozzi dentari normali catturati nelle prime fasi di sviluppo a “cap” e “bell”. In alcune regioni, l’architettura del POT privo della banda subepiteliale condensata somigliava molto a quella degli abbozzi dentari: le aree medie delle cellule virtuali epiteliali non risultavano statisticamente diverse. Al contrario, l’odontoma in sviluppo e il fibroma ameloblastico mostravano firme quantitative distinte, incluse menoplici stratificazioni di cellule virtuali e distribuzioni diverse delle aree cellulari epiteliali, nonostante talvolta imitassero lo sviluppo dentario all’aspetto microscopico. Queste differenze misurabili suggeriscono che, anche quando i tessuti appaiono simili all’occhio, la loro organizzazione spaziale sottostante può rivelare indizi diagnostici sottili.
Cosa significa per i pazienti e per i patologi
Lo studio dimostra che l’analisi algoritmica delle “cellule virtuali” può catturare schemi architettonici che supportano l’idea del tumore odontogenico primordiale come tipo distinto di lesione mandibolare, una lesione che in alcune aree si comporta come un abbozzo dentario precoce e attivamente interagente. Allo stesso tempo quantifica in che modo altri tumori odontogenici misti differiscono per dimensione e stratificazione dei loro compartimenti epiteliali. Per i pazienti, questo non modifica ancora il trattamento, ma indica un futuro in cui misurazioni assistite dal computer integrano la patologia tradizionale, specialmente in biopsie piccole o ambigue. Gli autori sottolineano che il loro set di dati è ancora limitato e che sono necessari studi multicentrici su più ampia scala prima che tali metodi possano orientare routinariamente la diagnosi, ma il lavoro illustra come gli strumenti digitali possano trasformare le impressioni qualitative del patologo in numeri riproducibili.
Citazione: Pereira-Prado, V., Sicco, E., Silveira, F.M. et al. Algorithmic analysis of the structure of mixed odontogenic tumors. Sci Rep 16, 7538 (2026). https://doi.org/10.1038/s41598-026-38399-6
Parole chiave: tumori odontogenici, tumore odontogenico primordiale, patologia digitale, analisi virtuale delle cellule, sviluppo del dente