Clear Sky Science · it
Modello prognostico basato sul machine learning di geni legati alla staminalità e all’angiogenesi per prevedere prognosi e infiltrazione immunitaria nei pazienti con HCC
Perché questa ricerca conta per i pazienti con tumore al fegato
Il carcinoma epatocellulare, la forma più comune di tumore al fegato, spesso recidiva o si diffonde anche dopo il trattamento. Questo studio esplora le ragioni di tali recidive e come i medici potrebbero prevedere meglio quali pazienti sono a maggior rischio. Combinando grandi dataset genetici con il machine learning moderno, i ricercatori hanno sviluppato uno strumento che collega due caratteristiche chiave del cancro — la “staminalità” (cellule che si comportano come semi ostinati) e la crescita di nuovi vasi — alle probabilità di sopravvivenza dei pazienti e alla loro probabile risposta alle terapie immunitarie.
“Cellule-seme” del cancro e nuovi vasi sanguigni
Molti tumori contengono un piccolo gruppo di cellule che agiscono come semi. Queste cellule staminali tumorali possono autorinnovarsi, resistere ai trattamenti e riavviare il tumore dopo interventi chirurgici o chemioterapia. Allo stesso tempo, i tumori devono formare nuovi vasi sanguigni per portare ossigeno e nutrienti e poter così crescere e metastatizzare. Lavori recenti mostrano che questi due processi sono intrecciati: le cellule con caratteristiche staminali rilasciano segnali che favoriscono l’angiogenesi, mentre un microambiente ricco di vasi aiuta la sopravvivenza di quelle cellule-seme. Capire e mirare congiuntamente a questa partnership è particolarmente importante nel carcinoma epatocellulare, che è altamente vascolarizzato e incline alle recidive.
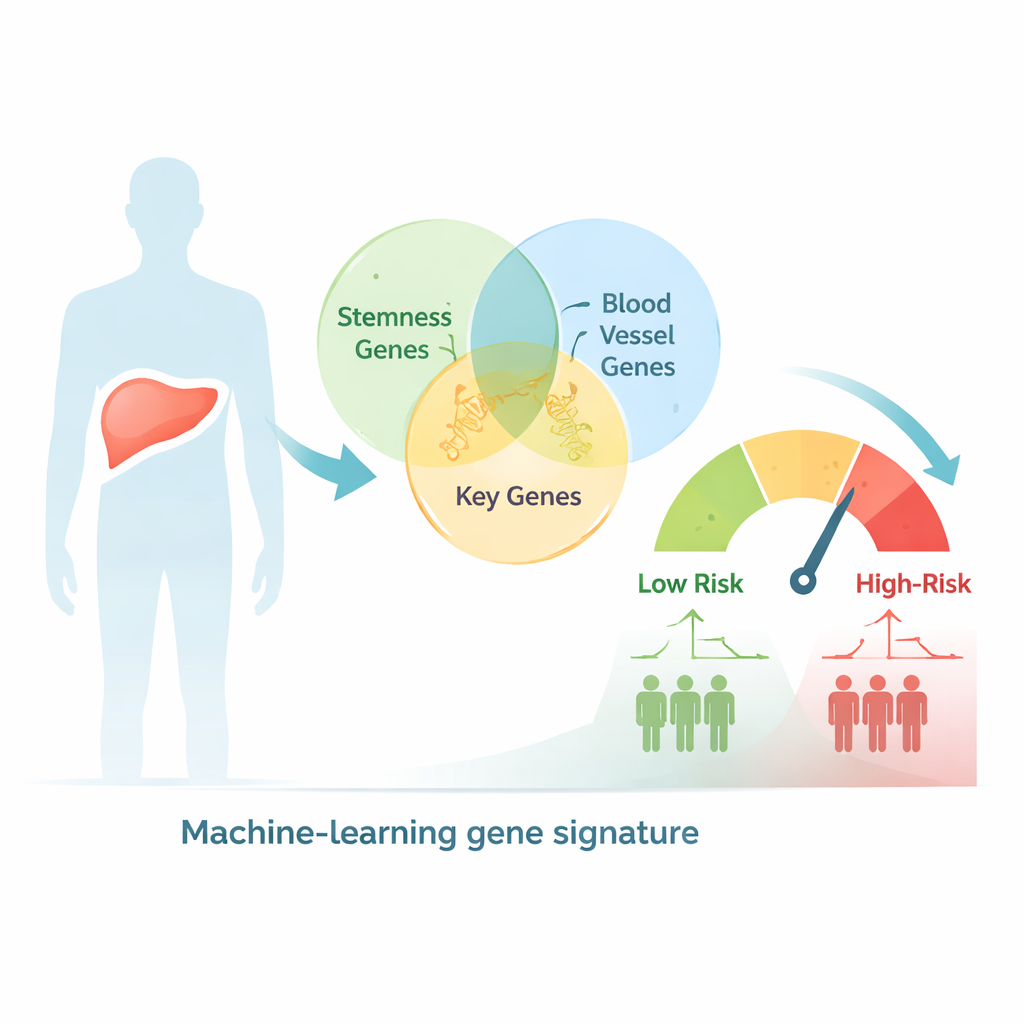
Usare i big data per classificare i pazienti per rischio
I ricercatori hanno iniziato cercando in un ampio database genico umano i geni collegati sia al comportamento staminale sia alla formazione di vasi, ottenendo oltre 2.600 candidati sovrapposti. Hanno poi esaminato campioni di tumore al fegato provenienti da centinaia di pazienti i cui profili di espressione genica e gli esiti clinici erano registrati in banche dati pubbliche. Con test statistici e metodi di clustering hanno raggruppato i pazienti in due sottotipi genetici che mostravano differenze chiare in stadio, dimensione del tumore e sopravvivenza, suggerendo che i segnali combinati di staminalità e angiogenesi catturano aspetti biologici significativi in questa malattia.
Costruzione di un punteggio di rischio a nove geni
Dal vasto insieme di geni, il gruppo ha utilizzato un approccio di machine learning per ridurre il numero a soli nove geni chiave la cui attività combinata prevedeva meglio la durata di sopravvivenza dei pazienti. Questi nove geni sono stati usati per calcolare un punteggio di rischio per ciascun individuo. I pazienti il cui tumore presentava un punteggio elevato avevano una sopravvivenza globale significativamente più breve, sia nel dataset originale sia in un gruppo indipendente di pazienti con carcinoma epatocellulare usato per la validazione. L’accuratezza del modello è risultata competitiva o superiore a molti strumenti esistenti e, quando il punteggio è stato combinato con semplici informazioni cliniche come lo stadio tumorale in un grafico chiamato nomogramma, la previsione della sopravvivenza a 1, 3 e 5 anni è ulteriormente migliorata.
Collegamenti con il sistema immunitario e la risposta al trattamento
Il team ha inoltre valutato cosa rivelasse il punteggio a nove geni sull’ambiente immunitario del tumore. I tumori a basso rischio tendevano a essere più “infiammati”, con livelli più alti di varie cellule immunitarie e segnali più forti di vie d’attacco. I tumori ad alto rischio, al contrario, mostravano pattern coerenti con l’evasione immunitaria e tassi più elevati di mutazioni in geni importanti come TP53. Utilizzando strumenti computazionali consolidati che stimano la possibile risposta ai moderni farmaci immunoterapici, lo studio ha suggerito che i pazienti a basso rischio potrebbero rispondere meglio agli inibitori dei checkpoint immunitari rispetto a quelli ad alto rischio. Sebbene queste predizioni debbano ancora essere testate in contesti terapeutici reali, indicano un modo pratico per identificare i pazienti che potrebbero beneficiare maggiormente di tali farmaci.
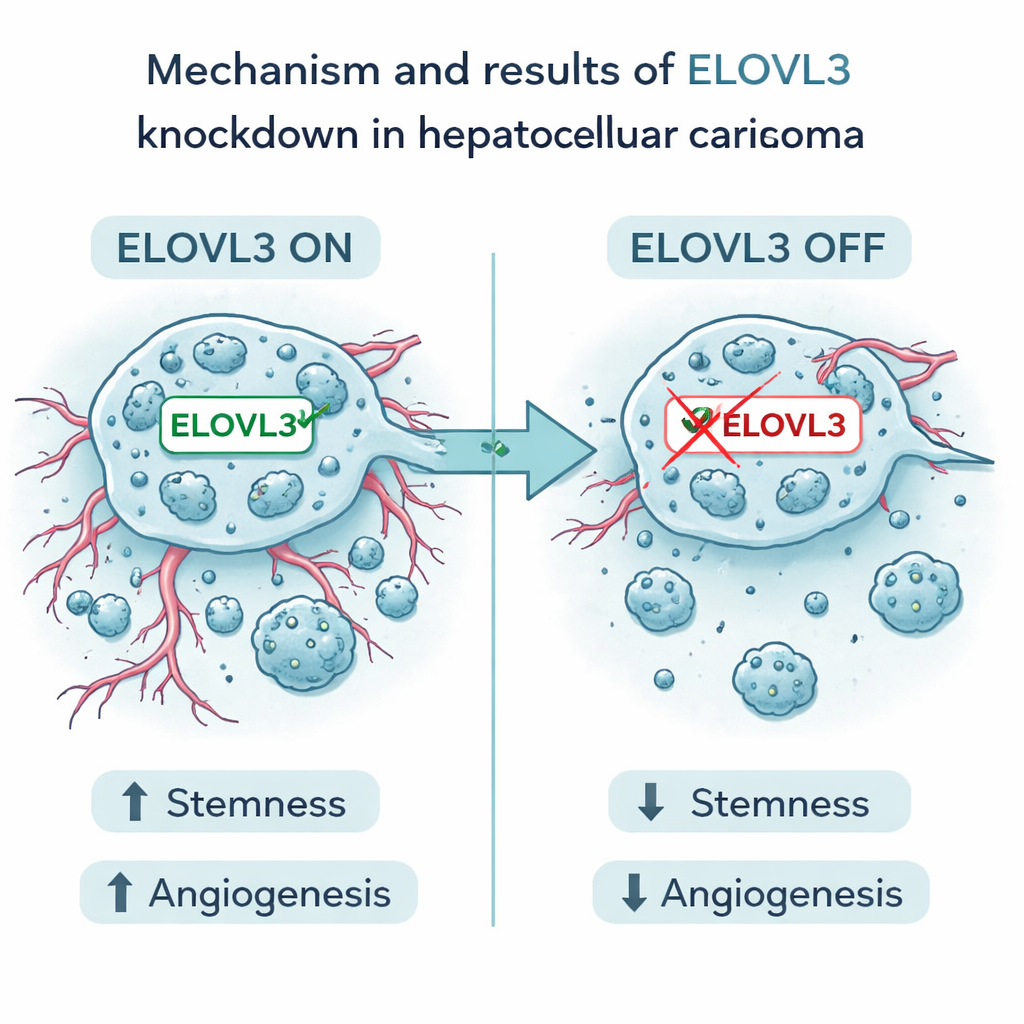
Focus su un bersaglio promettente
Tra i nove geni, uno chiamato ELOVL3 è emerso in modo particolare. Livelli elevati di questo gene erano associati a una sopravvivenza peggiore. In esperimenti di laboratorio, gli autori hanno ridotto l’espressione di ELOVL3 in cellule umane di carcinoma epatocellulare. Ciò ha reso le cellule meno capaci di formare aggregati con caratteristiche staminali e ha abbassato i livelli di noti marker di staminalità. Ha inoltre ridotto la produzione e il rilascio di due importanti fattori pro‑angiogenici, VEGFA e FGF2. Le cellule tumorali hanno mostrato minore crescita, migrazione e invasione e, in modelli murini, i tumori con ELOVL3 ridotto erano più piccoli e mostravano meno segni di aggressività. Questi risultati supportano l’idea che ELOVL3 favorisca sia il comportamento rigenerativo delle cellule tumorali sia la loro capacità di costruire una rete vascolare di supporto.
Cosa potrebbe significare per le cure future
In termini semplici, questo lavoro porta due messaggi principali. Primo, un semplice punteggio a nove geni ricavato da campioni tumorali può classificare i pazienti con carcinoma epatocellulare in gruppi a rischio più alto e più basso e suggerire come potrebbero rispondere alle terapie basate sul sistema immunitario. Secondo, uno dei geni in quel punteggio, ELOVL3, sembra trovarsi al crocevia tra la capacità del cancro di rigenerarsi e quella di sviluppare nuovi vasi, rendendolo un interessante bersaglio farmacologico futuro. Sebbene il modello e il bersaglio richiedano conferme in studi clinici prospettici, aprono la strada a una cura del cancro al fegato più personalizzata e a strategie combinate che blocchino sia le “cellule-seme” tumorali sia il loro apporto vascolare.
Citazione: Cheng, F., Shi, Y., Gao, X. et al. Machine learning-based prognostic model of stemness and angiogenesis-related genes for predicting prognosis and immune infiltration in patients with HCC. Sci Rep 16, 7271 (2026). https://doi.org/10.1038/s41598-026-38379-w
Parole chiave: carcinoma epatocellulare, cellule staminali tumorali, angiogenesi, firma genica prognostica, ELOVL3